
【题目】电解原理在化学工业中有广泛应用。如图表示一个电解池,装有电解液a,X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
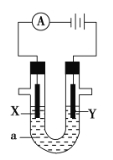
(1)若X、Y都是惰性电极,a是AgNO3溶液,实验开始时,同时在两边各滴入几滴石蕊试液,则
①电解池中Y电极上的电极反应式为 。在Y电极附近观察到的实验现象是 ;检验该电极反应产物的方法是 。
②X电极上的电极反应式为 。
(2)如要用电解方法精炼粗镍,电解液a选用Ni(NO3)2溶液,则:
①X电极的材料是 ,电极反应式为 ;
②Y极的材料是 ,电极反应式为 。
【答案】(1)①2H2O-4e-=4H++O2↑(3分);有无色气体放出,溶液变红(3分);
用带火星的木条检验,木条复燃。(3分)②4Ag++4e-=4Ag(3分)
(2)纯镍(1.5分);Ni2++2e-=Ni(3分)粗镍(1.5分);Ni-2e-=Ni2+(3分)
【解析】
试题分析:(1)①和电源的负极相连的电极X是阴极,Y是阳极,该电极上氢氧根放电生成氧气,电极反应式为2H2O-4e-=4H++O2↑;生成氧气,所以该电极附近氢离子浓度增大,酸性增强,溶液变红色;检验氧气的方法是用带火星的木条检验,木条复燃。
②X是阴极,溶液中的银离子放电,电极反应式为4Ag++4e-=4Ag;
(2)①精炼粗镍时,X为阴极,是纯镍,电极反应为溶液中的镍离子得到电子生成镍,电极反应为Ni2++2e-=Ni。
②Y是阳极,电极材料是粗镍,电极反应式为Ni-2e-=Ni2+。


科目:高中化学 来源: 题型:
【题目】已知反应A+3B2C+D在某段时间内以A的浓度变化表示的化学反应速度为1molL﹣1min﹣1 , 则此段时间内以C的浓度变化表示的化学反应速率为( )
A.0.5molL﹣1min﹣1
B.1molL﹣1min﹣1
C.2molL﹣1min﹣1
D.3molL﹣1min﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学设计实验以探究元素性质的递变规律,实验装置如图所示:
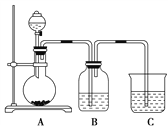
实验Ⅰ:根据元素最高价含氧酸的酸性强弱探究元素非金属性递变规律。
已知A装置的烧瓶里装有大理石,分液漏斗里装有稀HNO3,B装置中装有饱和碳酸氢钠溶液,C装置中装有Na2SiO3溶液,试回答:
(1)A中反应的离子方程式为____________,C中可观察到的现象是________。
(2)B装置的作用是______________。
(3)根据实验现象推知,碳酸、硝酸、原硅酸的酸性强弱顺序是________,由此得出碳、氮、硅三种元素非金属性的强弱顺序是________________。
实验Ⅱ:已知常温下高锰酸钾与浓盐酸混合可产生氯气,利用该装置探究氯元素和溴元素的非金属性强弱。
(4)写出B装置中发生反应的离子方程式:__________________________。
(5)C装置的作用是_______________________。
(6)实验结论:氧化性:________,非金属性:________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知铅元素有+2价、+4价两种常用价态,铅及其化合物可用于耐酸设备及X射线防护等。
(1)我国古代炼丹中经常使用到红丹(用X表示),在一定条件下,与过量硝酸能发生非氧化还原反应:X+4HNO3===PbO2+2Pb(NO3)2+2H2O(已配平)。
①PbO2中铅元素的化合价是________,PbO2不是碱性氧化物,判断的依据是_________________________________________________。
②X的化学式是________。
(2)PbO2可由PbO与次氯酸钠溶液反应制得,反应的离子方程式为____________________________________________。
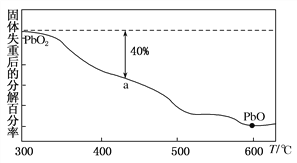
(3)PbO2在加热的过程中发生分解生成PbO和O2,其失重曲线如图所示,已知失重曲线上的a点为样品分解40%的残留固体。若a点固体组成表示为PbOx,则x=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 正丁烷和异丁烷均有两种一氯取代物
B. 乙烯和苯都能与H2发生加成反应,说明二者的分子中均含碳碳双键
C. 乙醇与金属钠能反应,且在相同条件下比水与金属钠的反应更剧烈
D. 乙醛能被还原成乙醇,但不能被氧化成乙酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A. ![]() 的溶液中:Na+、K+、AlO2-、NO3-
的溶液中:Na+、K+、AlO2-、NO3-
B. 含有大量Fe3+的溶液中:NH4+、I-、Cl-、K+
C. pH=7的溶液中:NH4+、Al3+、SO42-、NO3-
D. 0.1mol·L-1Na2SO3的溶液中:H+、Ca2+、Fe2+、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I、现有含CaO杂质的CaC2试样。设计以下实验,测定CaC2试样的纯度。(反应方程式为:CaC2+2H2O→Ca(OH)2+C2H2↑),请从下图中选用适当的装置,完成该实验。
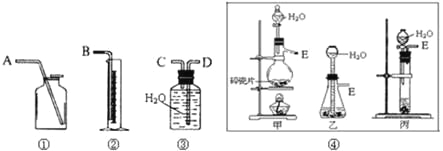
(1)制取C2H2最好选④中的 装置(填“甲”“乙”或“丙”),所选用装置的连接顺序是 (填各接口A~E的顺序)。
(2)若实验时称取的试样为1.4g,产生的乙炔在标准状况下的体积为448mL,此试样中CaC2的质量分数为 。(保留3为有效数字)

II、某同学在实验室从如图标签的试剂瓶中取少许钠进行燃烧实验,实验后 发现还有少许黑色固体生成。从反应物及实验操作猜测:
该黑色物质可能为碳与另一种氧化物组成的混合物。
根据题意和图示回答下面问题:
(1)装置图⑤中A的名称 。
(2)此氧化物可能是 或 (写化学式)。
(3)对黑色固体物质的组成作如图⑥所示研究
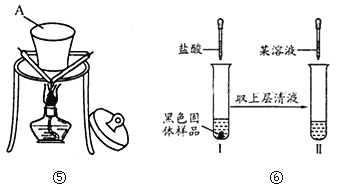
①实验I中加入盐酸溶液的目的是 。
②仅通过实验II,用最简步骤能快速确定黑色氧化物的组成,请完善该设计。(限选试剂:稀盐酸、KSCN溶液、10%H2O2溶液)
实验操作 | 预期现象与结论 | 相关离子方程式 |
取少量实验I中的澄清溶液,加入试剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是

A. 图I装置中通入N2和O2的作用是相同的
B. 图Ⅱ中甲、乙两装置产生喷泉的原理一样
C. 图Ⅲ①装置中镁片是原电池的负极;②装置中镁片是原电池的正极
D. 图Ⅳ分液漏斗盛硝酸能证明非金属性N>C>Si,盛硫酸能证明非金属性S>C>Si
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com