
【题目】能源是人类生存和发展的重要支柱,化学在能源的开发与利用方面起着十分重要的作用。某学习小组按如下图所示装置探究化学能与电能的相互转化:
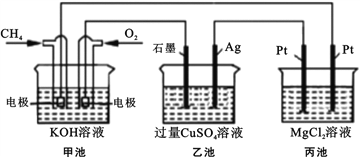
(1) 甲池是_____装置,通入CH4气体的电极上的反应式为_____。乙池中SO42- 移向_____电极(填“石墨”或“Ag”)
(2) 当甲池消耗标况下33.6LO2时,电解质KOH的物质的量变化_____mol,乙池若要恢复电解前的状态则需要加入_____g _____(填物质名称)。
(3) 丙池中发生的电解反应的离子方程式为_____。
【答案】 原电池(或化学能转化为电能) CH4 –8e-+ 10OH- ═ CO32-+ 7H2O 石墨 1.5 240 氧化铜 (或372,碳酸铜) Mg2+ +2Cl-+2H2O ![]() Mg(OH)2↓+ H2↑+ Cl2↑
Mg(OH)2↓+ H2↑+ Cl2↑
【解析】(1)由图可看出甲图为燃料电池装置,是原电池,通入甲烷的电极为负极,反应式为CH4 –8e-+ 10OH-=CO32-+ 7H2O,通入氧气的电极为正极,乙图和丙图为电解池,与电池的正极相连的石墨为阳极,与电池的负极相连的Ag电极为阴极,乙池中SO42- 移向石墨极(阳极)。(2)原电池正极反应式为:2O2+8e-+4H2O=8OH-,总反应为:CH4 +2O2+ 2OH-=CO32-+ 3H2O,当甲池消耗标况下33.6L(1.5mol)O2时,消耗1.5molKOH,转移6mol电子,则乙池生成3molCu和1.5molO2,根据原子守恒,若要恢复电解前的状态则需要加入氧化铜:3mol×80g/mol=240g,或碳酸铜:3mol×124g/mol=372g。(3)丙池中惰性电极电解氯化镁溶液,电解反应的离子方程式为Mg2+ +2Cl-+2H2O ![]() Mg(OH)2↓+ H2↑+ Cl2↑。
Mg(OH)2↓+ H2↑+ Cl2↑。


 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案科目:高中化学 来源: 题型:
【题目】取两份铝片,第一份与足量盐酸反应,第二份与足量烧碱溶液反应,同温同压下放出相同体积的气体,则两份铝片的质量之比为( )
A. 1:6 B. 2:3 C. 3:2 D. 1:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C三种物质随着X的变化,Y发生相应的变化,其变化关系如图所示。

(1)若X表示的是物质的量,则Y表示的不可能是_____(填序号,下同)
①物质的量 ②物质的体积 ③物质所含分子或原子的数目 ④物质的摩尔质量
(2)若A、B、C均为气体且压强恒定时,X表示的是温度,则Y表示的可能是______。
①气体的质量 ②气体的分子数 ③气体的体积 ④气体的摩尔质量
(3)若A、B、C均为气体,Y表示在相同条件下气体的体积,X表示的是气体的质量。
①相同条件下A、B、C三种气体的密度由大到小的顺序是_____(用字母A、B、C表示,下同)。
②A、B、C三种气体的摩尔质量由大到小的顺序是__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
氯吡格雷是一种血小板聚集抑制剂,该药物以![]() 为原料的合成路线如图:
为原料的合成路线如图:
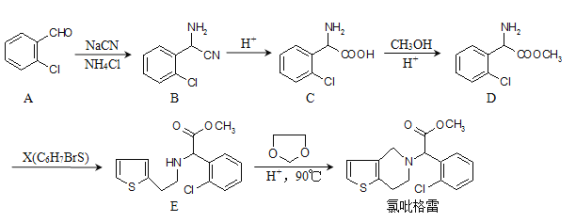
请根据以上信息,结合自己掌握的知识和具有的经验回答下列问题:
(1)分子C中无氧官能团的名称为____________。 命名为__________。
命名为__________。
(2)D→E的反应类型是_________反应。
(3)X的结构简式为___________________。
(4)下列叙述正确的是________(填序号)。
A.A物质中所有原子均可共面 B.C物质可发生取代、氧化、还原反应
C.![]() 在水中溶解度小 D.E中有两个手性碳原子
在水中溶解度小 D.E中有两个手性碳原子
(5)分子C在一定条件下生成一种含有3个六元环的产物的化学方程式为_____________。
(6)同时满足下列两个条件的B的同分异构体共有_____种(不包括B)。
①与B含有相同的官能团;②苯环上的取代基不超过2个。
(7)已知:![]() ,则由乙醇、甲醇为有机原料制备化合物
,则由乙醇、甲醇为有机原料制备化合物![]() 需要经历的反应类型有______(填序号)。
需要经历的反应类型有______(填序号)。
①加成反应 ②消去反应 ③取代反应 ④氧化反应 ⑤还原反应
写出制备化合物![]() 的最后一步反应:______________________。
的最后一步反应:______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na、Mg、Al的有关性质的叙述正确的是( )
A.还原性:Na>Mg>Al
B.第一电离能:Na<Mg<Al
C.电负性:Na>Mg>Al
D.碱性:NaOH<Mg(OH)2<Al(OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于碱金属单质的描述正确的是( )
A. 碱金属都可以保存在煤油中
B. 碱金属与水反应,均浮在水面上
C. 在空气中加热均可生成多种氧化物
D. 硬度小、密度小、熔点低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某校环保小组学生处理污水样品时,需要配制450mL0.1mol/L硫酸。
(1)如图所示仪器中,配制上述溶液肯定不需要的仪器是_____(填字母),除图中已有仪器外,配制上述溶液还需要的玻璃仪器是______(填仪器名称)。

(2)如果用5.0mol/L的硫酸来配制上述硫酸,则需该硫酸的体积为_____。
(3)在容量瓶的使用方法中,下列操作正确的是____(填字母)。
A.使用容量瓶前检查它是否漏水
B.容量瓶用水洗净后,再用待配溶液润洗
C.配制溶液时,如果试样是固体,把称好的试样用纸条小心倒入容量瓶中,缓慢加水接近标线l~2cm处,用滴管加蒸馏水至标线
D.定容后,盖好瓶塞,用食指顶住瓶塞,另一只手托住瓶底,把容量瓶反复倒转多次,摇匀
(4)定容时,若仰视刻度线,则所配溶液物质的量浓度___(填“偏大”“偏小”“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.原子晶体中可能存在极性共价键
B.干冰升华时分子内共价键发生断裂
C.原子晶体的熔点比分子晶体的熔点低
D.离子晶体中只含离子键,不含共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素周期表中某区域的一些元素通常用来制造农药,这些元素是( )
A. 左下方区域的金属元素 B. 金属元素和非金属元素分界线附近的元素
C. 稀有气体元素 D. 右上方区域的非金属元素
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com