
| HCl |
| NH3?H2O |
| △ |

| HCl |
| NH3?H2O |
| △ |
| HCl |
| NH3?H2O |
| △ |
| ||
| ||
| 0.39g |
| 78g/mol |
| 0.015mol |
| 2mol/L |
| 0.78g |
| 78g/mol |
| 0.035mol |
| 2mol/L |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
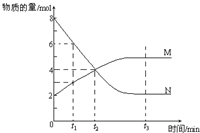 在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )
在一定温度下,容器内某一反应中M、N的物质的量随反应时间变化的曲线如图,下列表述中正确的是( )| A、反应的化学方程式为:2 N?M |
| B、t2时,正逆反应速率相等,达到平衡 |
| C、t3时,正反应速率大于逆反应速率 |
| D、t1时,N的浓度是M浓度的2倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、聚氟乙烯属于有机物 |
| B、聚氟乙烯是加聚反应的产物 |
| C、聚氟乙烯溶于水,易与空气中的氧气反应 |
| D、聚氟乙烯中碳元素的质量分数为37.5% |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、硅酸是不挥发性酸,因此不能由盐酸制得 |
| B、氢氟酸能和玻璃发生化学反应,所以氢氟酸要存放在塑料瓶中 |
| C、水玻璃有黏性,所以要存放在带橡胶塞的试剂瓶中 |
| D、烧碱溶液会腐蚀玻璃并生成硅酸钠,所以烧碱溶液要存放在带橡胶塞的试剂瓶里 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
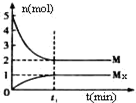 E是非金属性最强的元素,M是E的气态氢化物,在固定体积的密闭容器中,气体M存在如下关系:xM(g)?Mx(g),反应物和生成物的物质的量随时间的变化关系如图.下列说法正确的是( )
E是非金属性最强的元素,M是E的气态氢化物,在固定体积的密闭容器中,气体M存在如下关系:xM(g)?Mx(g),反应物和生成物的物质的量随时间的变化关系如图.下列说法正确的是( )| A、该反应的化学方程式是2HF?(HF)2 | ||
B、t1时刻,保持温度不变,再充入1molM,重新达到平衡时,
| ||
| C、平衡时混合气体的平均摩尔质量是33.3 | ||
| D、M的沸点比同主族下一周期元素的气态氢化物沸点低 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com