
【题目】已知X、Y、Z、W四种元素分别是元素周期表中三个连续短周期的元素,且原子序数依次增大。X、W同主族, Y、Z为同周期的相邻元素。W原子的质子数等于Y、Z原子的最外层电子数之和。Y与X形成的分子中有3个共价键。![]() 原子的最外层电子数是次外层电子数的3倍,试推断:
原子的最外层电子数是次外层电子数的3倍,试推断:
(1)X、Z两种元素的元素符号: X__________、Z__________。
(2)由以上元素中两两形成的化合物中,溶于水显碱性的气态氢化物的电子式为__________,它的共价键属于__________(填“极性”或“非极性”)键;含有离子键和非极性共价键的化合物的电子式为__________;含有极性共价键和非极性共价键的化合物的电子式为_______。
(3)由X、Y、Z所形成的常见离子化合物是__________(写化学式),该化合物与W的最高价氧化物对应的水化物的浓溶液加热时反应的离子方程式为__________;W的单质与水反应时,水作__________(填“氧化剂”或“还原剂”)。
(4)用电子式表示W与Z形成W2Z化合物的过程:__________。
【答案】H O 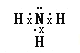 极性
极性 ![]()
![]() NH4NO3 NH4++OH-
NH4NO3 NH4++OH-![]() NH3↑+H2O 氧化剂
NH3↑+H2O 氧化剂 ![]()
【解析】
X、Y、Z、W四种元素分别是元素周期表中连续三个短周期的元素,且原子序数依次增大,Z原子最外层电子数是次外层电子数的3倍,最外层电子数不超过8个,所以Z元素是O元素;Y、Z为同周期的相邻元素,Y与X形成的分子中有3个共价键,X的原子序数最小且能和Y形成共价键,则X和Y都是非金属元素,Y的原子序数小于8,所以Y是N元素,X是H元素;X、W同主族,W原子的质子数等于Y、Z原子最外层电子数之和,则W是Na元素,结合对应单质和化合物的性质解答该题.
X、Y、Z、W四种元素分别是元素周期表中连续三个短周期的元素,且原子序数依次增大,Z原子最外层电子数是次外层电子数的3倍,最外层电子数不超过8个,所以Z元素是O元素;Y、Z为同周期的相邻元素,Y与X形成的分子中有3个共价键,X的原子序数最小且能和Y形成共价键,则X和Y都是非金属元素,Y的原子序数小于8,所以Y是N元素,X是H元素;X、W同主族,W原子的质子数等于Y、Z原子最外层电子数之和,则W是Na元素;
(1)由以上分析可知X为H,Z为O;
(2)由以上元素两两形成的化合物中:溶于水显碱性的气态氢化物是氨气,氨气的电子式为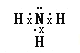 ,氮原子和氢原子之间的共价键是极性键;含有离子键和非极性共价键的化合物为过氧化钠,过氧化钠的电子式为
,氮原子和氢原子之间的共价键是极性键;含有离子键和非极性共价键的化合物为过氧化钠,过氧化钠的电子式为![]() ;含有极性共价键和非极性共价键的化合物是双氧水,双氧水分子的电子式为
;含有极性共价键和非极性共价键的化合物是双氧水,双氧水分子的电子式为![]() ;
;
(3)由X、Y、Z所形成的常见离子化合物是NH4NO3,W的最高氧化物的水化物为NaOH,二者反应的离子方程式为NH4++OH-![]() NH3↑+H2O,X与W形成的化合物是NaH,氢化钠和水反应生成氢氧化钠和氢气,该反应中水得电子作氧化剂;
NH3↑+H2O,X与W形成的化合物是NaH,氢化钠和水反应生成氢氧化钠和氢气,该反应中水得电子作氧化剂;
(4)钠和氧气反应生成氧化钠,该反应中钠失电子发生氧化反应,氧气得电子发生还原反应,其形成过程可表示为:![]() 。
。


 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案科目:高中化学 来源: 题型:
【题目】某同学利用氯酸钾分解制氧气的反应,测定氧气的摩尔质量,实验步骤如下:
①把适量的氯酸钾粉末和少量二氧化锰粉末混合均匀,放入干燥的试管中,准确称量,质量为a g。
②装好实验装置。
③检查装置气密性。
④加热,开始反应,直到产生一定量的气体。
⑤停止加热(如图所示,导管出口高于液面)。
⑥测量收集到的气体的体积。
⑦准确称量试管和残留物的质量为b g。
⑧测量实验室的温度。
⑨把残留物倒入指定的容器中,洗净仪器,放回原处,把实验桌面收拾干净。
⑩处理实验数据,求出氧气的摩尔质量。

回答下列问题:
(1)如何检查装置的气密性? 。
(2)以下是测量收集到的气体体积必须包括的几个步骤:
①调整量筒内外液面高度使之相同;②使试管和量筒内的气体都冷却至室温;③读取量筒内气体的体积。这三步操作的正确顺序是 (请填写步骤代号)。
(3)测量收集到的气体体积时,如何使量筒内外液面的高度相同? 。
(4)如果实验中得到的氧气体积是c L(已换算为标准状况),水蒸气的影响忽略不计,氧气的摩尔质量的计算式为(含a、b、c,不必化简)M(O2)= 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,取铝土矿(含有![]() 、FeO、
、FeO、![]() 、
、![]() 等物质)用硫酸浸出后的溶液,分别向其中加入指定物质,反应后的溶液中能大量共存的一组离子正确的是
等物质)用硫酸浸出后的溶液,分别向其中加入指定物质,反应后的溶液中能大量共存的一组离子正确的是
A. 加入过量NaOH溶液:![]()
B. 加入过量氨水:![]()
C. 通入过量![]() :
:![]()
D. 通入过量![]() :
:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下述实验中均有红棕色气体产生,对比分析所得结论不正确的是( )
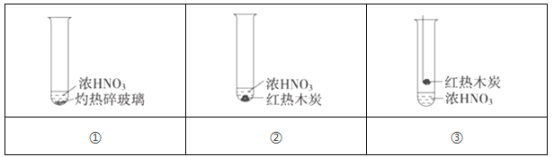
A. 由①中的红棕色气体,推断浓硝酸受热易分解,应保存在低温阴暗处
B. 红棕色气体不能表明②中木炭与浓硝酸发生了反应
C. 由③说明浓硝酸具有挥发性,生成的红棕色气体为还原产物
D. ③的气体产物中检测出CO2,由此说明木炭一定与浓硝酸发生了反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知![]() ,将0.1mol
,将0.1mol![]() 通入100mL含等物质的量HBr与
通入100mL含等物质的量HBr与![]() 的混合溶液中,有一半的HBr被氧化,则下列说法正确的是
的混合溶液中,有一半的HBr被氧化,则下列说法正确的是
A. 物质的还原性:![]()
B. HBr与![]() 的物质的量浓度均为
的物质的量浓度均为![]()
C. 通入0.1mol![]() 发生反应的离子方程式为:
发生反应的离子方程式为:![]()
D. 若再通入0.05mol![]() ,恰好能将HBr和
,恰好能将HBr和![]() 完全氧化
完全氧化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)假设甲烷与氯气反应充分,且只产生一种有机物,请写出化学方程式:______________________。
(2)若题目中甲烷与氯气的体积比为1:1,则得到的产物为________。
A.CH3Cl、HCl B.CCl4、HCl C.CH3Cl、CH2Cl2 D.CH3Cl、CH2Cl2、CHCl3、CCl4、HCl
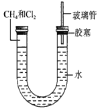
(3)经过几个小时的反应后,U形管右端的水柱变化是___________。
A.升高 B.降低 C.不变 D.无法确定
(4)若水中含有Na2SiO3,则在U形管左端会观察到_________________________。
(5)右端玻璃管的作用是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上通常采取CO(g)和![]() (g)合成
(g)合成![]() (g)
(g)
(1)已知某温度和压强下
①![]()
![]()
②![]()
![]()
③![]()
![]()
则在相同温度和压强下,CO(g)与![]() (g)合成
(g)合成![]() (g)的热化学方程式__________。
(g)的热化学方程式__________。
若反应生成6.4g甲醇,则转移电子的物质的量为__________。
(2)可利用甲醇燃烧反应设计一个燃料电池。如图,用Pt作电极材料,用氢氧化钾溶液作电解质溶液,在两个电极上分别充入甲醇和氧气。
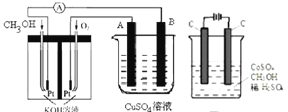
①写出燃料电池负极的电极反应式__________。
②若利用该燃料电池提供电源,与图右边烧杯相连,在铁件表面镀铜,则铁件应是__________极(填“A”或“B”);当铁件的质量增重6.4g时,燃料电池中消耗氧气的标准状况下体积为__________L。
(3)电解法可消除甲醇对水质造成的污染,原理是:通电将![]() 氧化成
氧化成![]() ,然后将甲醇氧化成CO和
,然后将甲醇氧化成CO和![]() (用石墨烯除去
(用石墨烯除去![]() )现用如图所示装置模拟上述过程,则
)现用如图所示装置模拟上述过程,则![]() 在阳极的电极反应式为__________。除去甲醇的离子方程式为__________。
在阳极的电极反应式为__________。除去甲醇的离子方程式为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将50g溶质质量分数为w1,物质的量浓度为c1 的较浓氨水沿玻璃棒加人到u mL水中,稀释后得到溶质质量分数为w2,物质的量浓度为c2的稀氨水。若c1 =2c2,则:
A. w1>2w2,u>50 B. w1<2w2,u<50 C. w1=2w2,u<50 D. w1<2w2,u>50
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】温度为T1时,将气体X和气体Y各1.6mol充入10L恒容密闭容器中,发生反应X(g)+Y(g)![]() 2Z(g),一段时间后达到平衡。反应过程中测定的数据如表:下列说法正确的是
2Z(g),一段时间后达到平衡。反应过程中测定的数据如表:下列说法正确的是
t/min | 2 | 4 | 7 | 9 |
n(Y)/mol | 1.2 | 1.1 | 1.0 | 1.0 |
A. 反应0~4 min的平均速率υ(Z)=0.25 mol/(Lmin)
B. T1时,反应的平衡常数K1=1.2
C. 其他条件不变,9 min后,向容器中再充入1.6 molX,平衡向正反应方向移动,再次达到平衡时X的浓度减小,Y的转化率增大
D. 其他条件不变,降温到T2达到平衡时,平衡常数K2=4,则此反应的△H<0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com