
����Ŀ����![]() Ϊ�����ӵ���������ֵ������˵����ȷ����( )
Ϊ�����ӵ���������ֵ������˵����ȷ����( )
A.100g 46%����ˮ��Һ�к���OH����ĿΪ1.5NA
B.1.7g��NH3��13CH4��ɵĻ�������к���������ΪNA
C.0.1molL-1��Al2(SO4)3��Һ�к�Al3+����ĿС��0.2 NA
D.��ӦCH4 + 2NO + O2 = CO2 + N2 + 2H2O��ÿ���ı�״����22.4L NO����Ӧ��ת�Ƶĵ�����ĿΪ2 NA
���𰸡�B
��������
Aѡ�100g 46%���ͼ�46g���ͣ����ʵ���Ϊ0.5mol�������к���OH����ĿΪ1.5NA��������ˮ��Ҳ�����ǻ�����A����
Bѡ�NH3��13CH4Ħ��������ͬ����Ϊ17gmol-1����������Ϊ10������1.7g��NH3��13CH4��ɵĻ���������ʵ���Ϊ0.1mol����������к���������ΪNA����B��ȷ��
Cѡ���Һ���δ֪�������Һ�к�Al3+����Ŀ�����㣬��C����
Dѡ���ӦCH4 + 2NO + O2 = CO2 + N2 + 2H2O�����ݷ�Ӧ����ʽ�ó���2molNO��Ӧת��8 mol���ӣ�ÿ���ı�״����22.4L NO��1molNO����Ӧ��ת�Ƶĵ�����ĿΪ4NA����D����
������������ΪB��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������й��л���ͬ���칹��˵���в���ȷ����( )
A.����ʽΪC4H8��ͬ���칹�干��(�����������칹)5��
B.��������ȡ������3��
C.����ʽΪC5H10O2��ͬ���칹��������������8��
D.![]() ��һ��ȡ������4��
��һ��ȡ������4��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��Ӧ��3A(g)+B(g)![]() C(s)+4D(g) ��H��0��ͼ��a��b���߱�ʾ��һ�������£�D�����������ʱ��ı仯��������з�����ȷ���ǣ� ��
C(s)+4D(g) ��H��0��ͼ��a��b���߱�ʾ��һ�������£�D�����������ʱ��ı仯��������з�����ȷ���ǣ� ��
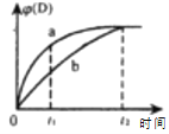
A.b����t2��v��(B)=4 v��(D)
B.a����t1ʱ��v��(A)>3 v��(B)
C.�����¶ȣ���ʹ����b��Ϊ����a
D.��С��Ӧ�������������ʹ����a��Ϊ����b
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ʵ��������������ԭ�����͵��ǣ� ��
A. FeCl3+3KSCN![]() Fe(SCN)3+3KClƽ����ϵ�м�������KSCN���壬��Һ��ɫ����
Fe(SCN)3+3KClƽ����ϵ�м�������KSCN���壬��Һ��ɫ����
B. ��ҵ�ϳɰ��У�������Һ������
C. A��B��֧�Թ��зֱ��������5%��H2O2��Һ����B�Թ��м���2��3��FeCl3��Һ��B���Թ��в������ݿ�
D. ���ڷ�Ӧ2NO2(g)![]() N2O4(g) ��H<0�������¶ȿ�ʹ��ϵ��ɫ����
N2O4(g) ��H<0�������¶ȿ�ʹ��ϵ��ɫ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��һ���Ʊ�������茶���[(NH4)3Fe(C2O4)3]�Ĺ����������£�
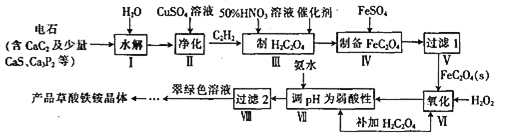
�ش��������⣺
(1)CaC2�ĵ���ʽΪ__________
(2)��������Ҫ�dz�ȥH2S��PH3���������塣�ڳ�PH3ʱ��PH3������ΪH3PO4��CuSO4����ԭΪCu���÷�Ӧ���������뻹ԭ�������ʵ���֮��Ϊ____________
(3)��������H2C2O4ʱ��Ҫ��������Ļ�ԭ����ΪNO���÷�Ӧ�Ļ�ѧ����ʽΪ______________�������Ũ�ȼ���Ӧ�¶ȶ����˹��ߣ�����Ϊ____________.
(4)������1����Գ�������ϴ�Ӽ������Ƿ�ϴ�Ӹɾ���������____________________
(5)��������VII���Ӳ����Ŀ����______________________.
(6)����VIII����Һ�Ƶò�Ʒ�IJ���Ϊ____________��____________�����ˡ�ϴ�ӡ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����и���������ָ�������£�һ���ܴ����������(����)
A.��ʹ��ɫʯ����ֽ���ɫ����Һ�У�K����Na����CO![]() ��NO
��NO![]()
B.ˮ�������c(H��)��1��10��12 mol/L����Һ�У�Na����Mg2����Cl����SO![]()
C.��ʹ�⻯�ص�����ֽ��������Һ�У�Na����NH![]() ��S2����Br��
��S2����Br��
D.c(H��)��1��10��1 mol/L����Һ�У�Cu2����Al3����SO![]() ��NO
��NO![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������N2H4���ʹ������ƣ�NaH2PO2��������ǿ��ԭ�ԣ������Ź㷺����;��
(1)��֪����N2H4(1)+O2(g)��N2(g)+2H2O(g) ��H1=-621.5kJmol-1
��N2O4(1)��N2(g)+2O2(g) ��H2=+204.3kJmol-1
����ȼ�ϵ�ȼ�շ�ӦΪ2N2H4(1)+N2O4(1)��3N2(g)+4H2O(g) ��H=__��
(2)��֪��ӦN2H4(g)+2Cl2(g)![]() N2(g)+4HCl(g)��T��ʱ����2L�����ܱ������м���2molN2H4(g)��4molCl2(g)�����Cl2��HCl��Ũ����ʱ��Ĺ�ϵ��ͼ��ʾ��
N2(g)+4HCl(g)��T��ʱ����2L�����ܱ������м���2molN2H4(g)��4molCl2(g)�����Cl2��HCl��Ũ����ʱ��Ĺ�ϵ��ͼ��ʾ��

��0��10min�ڣ���N2(g)��ʾ��ƽ����Ӧ����v(N2)=__��
��M��ʱ��N2H4��ת����Ϊ__����ȷ��0.1��%��
��T��ʱ���ﵽƽ�������������м���1.2molN2H4(g)��0.4molCl2(g)��0.8molN2(g)��1.2molHCl(g)����ʱƽ��__��������ƶ����������ƶ������ƶ�������
(3)�ٴ����ᣨH3PO2����һԪ�ᣬ�����£�1.0molL-1��NaH2PO2��ҺpHΪ8����������Ka=__��
���ô�������ͨ�����������Ʊ������ᣬװ����ͼ��ʾ������ĤA����__���������ӡ��������ӡ�������Ĥ���缫N�ĵ缫��ӦʽΪ___��

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���Ż�������ָ������������������̼ԭ�ӵĶ����������[1��1��0]����(![]() )�����һ�֡����й��ڸû������˵���������
)�����һ�֡����й��ڸû������˵���������
A. ��1��3-����ϩ��Ϊͬ���칹��
B. ���ȴ��ﹲ��4��
C. ̼̼��ֻ�е����ұ˴�֮��ļн���45����90������
D. ÿһ��̼ԭ�Ӿ���������ֱ��������ԭ�ӹ��ɵ��������ڲ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��NA��ʾ�����ӵ�������ֵ������˵����ȷ����
A.2.0gCO2��SO2�Ļ����������У����е�������ΪNA
B.7.1gCl2��100mL1.0mol��L��1NaOH��Һ��Ӧ��ת�Ƶ�����Ϊ0.1NA
C.17gNH3��48gO2�ڴ��������³�ַ�Ӧ���õ�NO������ΪNA
D.��״���£�2.24LCH4��C3H6��������У����м��Լ���Ϊ0.5NA
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com