
【题目】在4L密闭容器中充入6molA气体和5molB气体,一定条件下发生反应:3A(g)+B(g)![]() 2C(g)+xD(g),达到平衡时,生成了2molC,经测定,D的浓度为0.5mol/L,下列判断正确的是( )
2C(g)+xD(g),达到平衡时,生成了2molC,经测定,D的浓度为0.5mol/L,下列判断正确的是( )
A.B的转化率为20%B.平衡时A的浓度为1.50mol/L
C.x=1D.达到平衡时,在相同温度下容器内混合气体的压强是反应前的85%
科目:高中化学 来源: 题型:
【题目】(15分)含碳物质的价值型转化,有利于“减碳”和可持续性发展,有着重要的研究价值。请回答下列问题:
(1)已知CO分子中化学键为C≡O。相关的化学键键能数据如下:
化学键 | H—O | C≡O | C=O | H—H |
E/(kJ·mol1) | 463 | 1075 | 803 | 436 |
CO(g)+H2O(g)![]() CO2(g)+H2(g) ΔH=___________kJ·mol1。下列有利于提高CO平衡转化率的措施有_______________(填标号)。
CO2(g)+H2(g) ΔH=___________kJ·mol1。下列有利于提高CO平衡转化率的措施有_______________(填标号)。
a.增大压强 b.降低温度
c.提高原料气中H2O的比例 d.使用高效催化剂
(2)用惰性电极电解KHCO3溶液,可将空气中的CO2转化为甲酸根(HCOO),然后进一步可以制得重要有机化工原料甲酸。CO2发生反应的电极反应式为________________,若电解过程中转移1 mol电子,阳极生成气体的体积(标准状况)为_________L。
(3)乙苯催化脱氢制取苯乙烯的反应为:![]() (g)+CO2(g)
(g)+CO2(g)![]()
![]() (g)+CO(g)+H2O(g),其反应历程如下:
(g)+CO(g)+H2O(g),其反应历程如下:
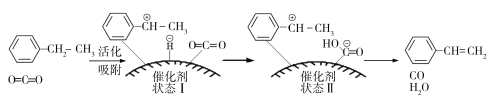
①由原料到状态Ⅰ____________能量(填“放出”或“吸收”)。
②一定温度下,向恒容密闭容器中充入2 mol乙苯和2 mol CO2,起始压强为p0,平衡时容器内气体总物质的量为5 mol,乙苯的转化率为_______,用平衡分压代替平衡浓度表示的化学平衡常数Kp=_______。[气体分压(p分)=气体总压(p总)×气体体积分数]
③乙苯平衡转化率与p(CO2)的关系如下图所示,请解释乙苯平衡转化率随着p(CO2)变化而变化的原因________________________________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】光电池在光照条件下可产生电流,如图装置可以实现光能源的充分利用,双极性膜可将水解离为H+和OH-,并实现其定向通过。下列说法不正确的是( )
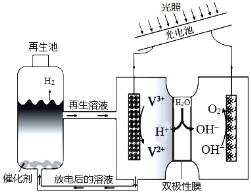
A.该装置可利用光能实现水的分解
B.光照过程中阴、阳极区溶液中的pH均基本不变
C.再生池中的反应为2V2++2H+![]() 2V3++H2↑
2V3++H2↑
D.每有1molOH-通过双极性膜,可产生5.6L(标准状况)的O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(14分)药物H在人体内具有抑制白色念球菌的作用,H可经下图所示合成路线进行制备。
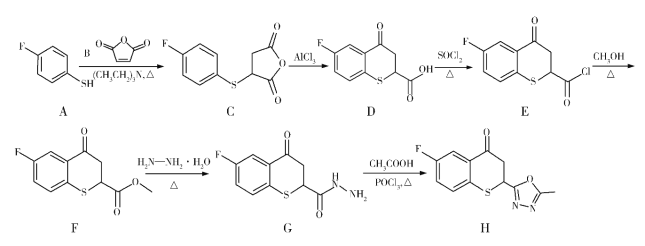
已知:硫醚键易被浓硫酸氧化。
回答下列问题:
(1)官能团SH的名称为巯(qiú)基,SH直接连在苯环上形成的物质属于硫酚,则A的名称为________________。D分子中含氧官能团的名称为________________。
(2)写出A→C的反应类型: _____________。
(3)F生成G的化学方程式为_______________________________________。
(4)下列关于D的说法正确的是_____________(填标号)。(已知:同时连接四个各不相同的原子或原子团的碳原子称为手性碳原子)
A.分子式为C10H7O3FS
B.分子中有2个手性碳原子
C.能与NaHCO3溶液、AgNO3溶液发生反应
D.能发生取代、氧化、加成、还原等反应
(5)M与A互为同系物,分子组成比A多1个CH2,M分子的可能结构有_______种;其中核磁共振氢谱有4组峰,且峰面积比为2∶2∶2∶1的物质的结构简式为_____________。
(6)有机化合物K(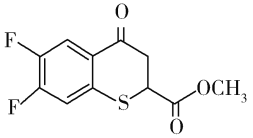 )是合成广谱抗念球菌药物的重要中间体,参考上述流程,设计以
)是合成广谱抗念球菌药物的重要中间体,参考上述流程,设计以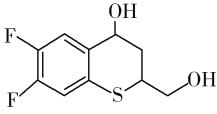 为原料的合成K的路线。_____________
为原料的合成K的路线。_____________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸亚铁晶体俗称绿矾(FeSO4 7H2O),重铬酸钠晶体俗称红矾钠(Na2Cr2O7·2H2O),它们都是重要的化工产品。工业上以铬铁矿[主要成分是[Fe(CrO2)2]为原料制备绿矾和红矾钠的工艺流程如图所示。
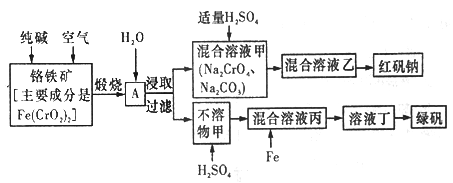
请回答下列问题:
(1)已知Fe(CrO2)2中铬元素的化合价为+3价,则Fe(CrO2)中铁元素的化合价为______________。
(2)化学上可将某些盐写成氧化物的形式,如Na2SiO3写成Na2O·SiO2,则Fe(CrO2)2可写成__________。
(3)煅烧铬铁矿时,矿石中的Fe(CrO2)2转变成可溶于水的Na2CrO4,反应的化学方程式如下:
4Fe(CrO2)2+8Na2CO3+7O2![]() 2Fe2O3+8Na2CrO4+8CO2
2Fe2O3+8Na2CrO4+8CO2
①该反应中还原剂与氧化剂的物质的量之比为________________。
②为了加快该反应的反应速率,可采取的措施是_________________(填一种即可)。
⑷己知CrO42-在氢离子浓度不同的酸性溶液中有不同的反应。如:
2CrO42-+2H+=Cr2O72-+H2O 3CrO42-+4H+=Cr3O102-+2H2O
①往混合溶液甲中加入硫酸必须适量的原因是________________。
②混合溶液乙中溶质的化学式为______________________。
(5)写出Fe与混合溶液丙反应的主要离子方程式_________________。检验溶液丁中无Fe3+的方法是:_____________。从溶液丁到绿巩的实验操作为蒸发浓缩、___________、过滤、洗涤、干燥。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由化合物A合成黄樟油(E)和香料F的路线如下(部分反应条件己略去):
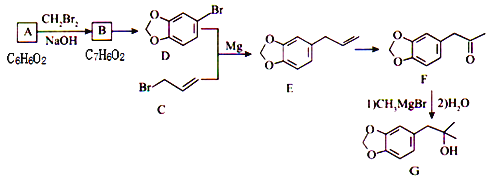
请回答下列问题:
(1)下列有关说法正确的是______________(填选项字母)。
a 化合物A核磁共振氢谱为两组峰
b CH2Br2只有一种结构
c 化合物E能发生加聚反应得到线型高分子
d 化合物B能发生银镜反应,也能与NaOH溶液反应
(2)由B转化为D所需的试剂为________________。
(3) D含有的官能团名称为________________。
(4)写出A→B的化学反应方程式:_______________。
(5)满足下列条件的E的同分异构体W有__________种(不含立体异构),其中核磁共振氢谱为五组峰且峰面积之比是1:2:2:2:3的结构简式为_________。
①1molW与足量NaOH溶液反应,能消耗2molNaOH
②能发生银镜反应
③苯环上只有两个取代基,能发生聚合反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下,向a L密闭容器中加入1 mol X气体和2 mol Y气体,发生如下反应:X(g)+2Y(g)![]() 2Z(g),此反应达到平衡的标志是( )
2Z(g),此反应达到平衡的标志是( )
A. 单位时间内消耗0.1 mol X的同时生成0.2 mol Z
B. v正(X) =v逆(Z)
C. 容器内X、Y、Z的浓度之比为1∶2∶2
D. 容器内压强不随时间变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂-铜空气燃料电池容量高、成本低,具有广阔的发展前景。该电池通过一种复杂的铜腐蚀―现象产生电能,其中放电过程为2Li+Cu2O+H2O=2Cu+2Li++2OH,下列说法错误的是
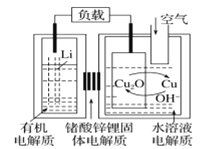
A.放电时,正极的电极反应式为O2+2H2O+4e=4OH
B.放电时,Li+透过固体电解质向右移动
C.通空气时,铜被腐蚀,表面产生Cu2O
D.整个反应过程中,氧化剂为O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】①![]() 与
与![]() ;②O2与O3;③正丁烷(CH3CH2 CH2 CH3)与异丁烷
;②O2与O3;③正丁烷(CH3CH2 CH2 CH3)与异丁烷![]() ;④甲烷(CH4)与丙烷(C3H8)。
;④甲烷(CH4)与丙烷(C3H8)。
(1)互为同位素的是______(填序号,下同)。
(2)互为同系物的是______。
(3)互为同分异构体的是______。
(4)互为同素异形体的是______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com