
【题目】下列各组离子在溶液中能大量共存的是( )
A.H+、SO42-、NO3-、Fe2+
B.Mg2+、Cl-、NO3-、OH-
C.Ba2+、Na+、CO32-、NO3-
D.Na+、Al3+、Cl-、SO42-
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】如图所示是分离混合物时常用的仪器,从左至右,可以进行的混合物分离操作分别是( ) 
A.蒸馏、蒸发、萃取、过滤
B.蒸馏、过滤、萃取、蒸发
C.萃取、过滤、蒸馏、蒸发
D.过滤、蒸发、萃取、蒸馏
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一定质量的Mg-Al合金投入100mL一定物质的量浓度的某HCl溶液中,充分反应。向反应后的溶液中逐滴加入一定物质的量浓度的NaOH溶液,生成沉淀的质量与所加NaOH溶液的体积关系如下图。回答下列问题:
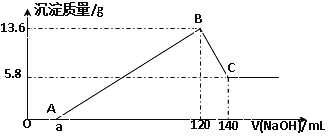
(1)写出OA段和BC段反应的离子方程式:
OA:________________________________ ; BC:_____________________________;
(2)原Mg-Al合金的质量是_____________。
(3)原HCl溶液的物质的量浓度是________________。
(4)所加NaOH溶液的物质的量浓度是____________。
(5)a的值是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示为CH4燃料电池的装置(A、B为多孔碳棒):
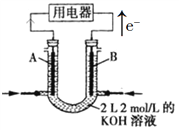
(1)_____(填A或B)处电极入口通甲烷,其电极反应式为_____________。
(2)当消耗甲烷的体积为11.2 L(标准状况下)时,消耗KOH的质量为_______g。
(3)铅蓄电池是最早使用的充电电池,由Pb、PbO2、硫酸构成。该电池工作时,正极的电极反应式为____________________。
(4)500 mL KNO3和Cu(NO3)2的混合溶液中c(![]() )=6.0 mol·L1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4 L气体(标准状况),假定电解后溶液体积仍为500 mL。原混合溶液中c(K+)为_________mol·L1。
)=6.0 mol·L1,用石墨作电极电解此溶液,当通电一段时间后,两极均收集到22.4 L气体(标准状况),假定电解后溶液体积仍为500 mL。原混合溶液中c(K+)为_________mol·L1。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CO、CO2是火力发电厂释放出的主要尾气,为减少对环境造成的影响,发电厂试图采用以下方法将其资源化利用,重新获得燃料或重要工业产品。
(1)CO 与Cl2在催化剂的作用下合成光气(COCl2)。某温度下,向2L的密闭容器中投入一定量的CO和Cl2,在催化剂的作用下发生反应:CO(g)+Cl2(g)![]() COCl2(g) ;△H=akJ/mol 反应过程中测定的部分数据如下表:
COCl2(g) ;△H=akJ/mol 反应过程中测定的部分数据如下表:
t/min | n (CO) /mol | n(Cl2)/mol |
0 | 1.20 | 0.60 |
1 | 0.90 | |
2 | 0.80 | |
4 | 0.20 |
①反应1~2min末的平均速率v(COCl2)=________mol/(L·min)。
②在2min~4min间,vCl2正_______vCO逆 (填“>”、“=”或“<”),该温度下K=________。
③已知X、L可分别代表温度或压强,下图表示L一定时,CO的转化率随X的变化关系。
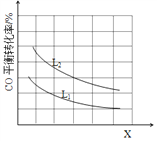
X代表的物理量是___________;a_______0 (填“>”,“=”,“<”)。
(2)在催化剂作用下NO和CO转化为无毒气体:2CO(g) +2NO(g)![]() 2CO2(g) +N2(g);△H=-748kJ·mol-1
2CO2(g) +N2(g);△H=-748kJ·mol-1
①一定条件下,单位时间内不同温度下测定的氮氧化物转化率如图1所示。温度高于710K时,随温度的升高氮氧化物转化率降低的原因可能是________________________________________________。
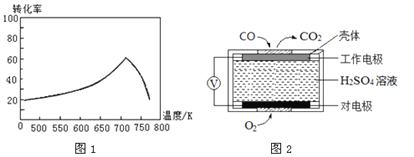
②已知: 测定空气中NO和CO含量常用的方法有两种:
方法1:电化学气敏传感器法。其中CO 传感器的工作原理如图2 所示,则工作电极的反应式为____________。
方法2:氧化还原滴定法。用H2O2溶液吸收尾气、将氮氧化物转化为强酸,用酸碱中和滴定法测定强酸依度。写出NO与H2O2溶液反应的离子方程式:____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钢铁分析中常用高氯酸(HClO4)溶解矿样,某研究性学习小组欲制取少量高氯酸。该学习小组查阅到:
a.HClO4浓度高于60%时遇含碳化合物易爆炸,浓度低于60%时比较稳定;
b.NaClO4与浓硫酸反应可制得高氯酸,若采用真空蒸馏可得纯高氯酸;
c.NaClO3在673K(400℃) 分解产生NaClO4、NaCl和一种气体。
该小组同学设计实验分三步制备高氯酸:
(一)制氯气并使制得的氯气与氢氧化纳溶液反应制氯酸纳;
(二)氯酸钠分解制高氯酸钠;
(三)高氯酸纳与浓硫酸反应制高氯酸[2NaClO4+H2SO4(浓)![]() Na2SO4+2HClO4]。
Na2SO4+2HClO4]。
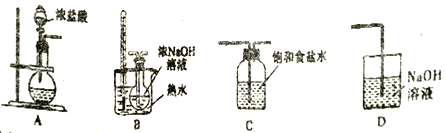
(1)制取氯酸钠的装置连接顺序为A,___________
(2)B 装置中发生反应的离子方程式为__________________________。
(3)为了制备高氯酸钠并推出氯酸钠分解制高氯酸钠的化学方程式,该小组设计了两组装置(甲,乙)如下:
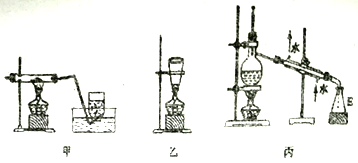
该小组经过分析决定选用甲装置制备高氯酸钠,取NaClO3样品2.13 g,加热充分反应后集气瓶中收集到224 mL (标准状况下)气体,则该反应的化学方程式为_________________________;不选用乙装置的原因可能为______________________。
(4)用丙裝置制备高氯酸,向烧瓶中加入高氯酸钠,然后加入浓硫酸后,加热可制取高氯酸。实验开始前,胶塞及导管接口需要包锡箔纸,其原因是___________,仪器E的名称为___________。该组同学发现操作中少加入一种物质,该物质的名称为___________。发现后的正确操作为_________________。
(5)工业上大量制备NaClO4常用高电流密度电解NaClO3的方法,试写出以惰性电极电解时的阳极反应式:_______________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式中,属于水解反应的是( )
A.HCOOH+H2OHCOO﹣+H3O+
B.CO32﹣+H2OHCO3﹣+OH﹣
C.CO2+H2OHCO3﹣+H+
D.HS﹣+H2OS2﹣+H3O+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将AgCl和AgBr的饱和溶液等体积混合,再加入足量的浓AgNO3溶液,下列说法正确的是( )
A.只有AgBr沉淀生成
B.生成等物质的量的AgCl和AgBr沉淀
C.沉淀的物质的量:AgCl多于AgBr
D.沉淀的物质的量:AgCl少于AgBr
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com