
A、 称量一定量的NaOH固体 |
B、 量取9.3mL稀盐酸 |
C、 转移液体 |
D、 铜锌原电池实验 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CaO+H2O═Ca(OH)2,可以放出大量的热,故可把该反应设计成原电池,把其中的化学能转化为电能 |
| B、某原电池反应为Cu+2AgNO3═Cu(NO3)2+2Ag,装置中的盐桥中可以是由KCl饱和溶液制得的琼脂 |
| C、因为铁的活动性强于铜,所以将铁、铜用导线连接后放入浓硝酸中,若能组成原电池,必是铁作负极,铜作正极 |
| D、理论上说,任何能自发进行的氧化还原反应都可被设计成原电池 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 除去混有的杂质气体 |
B、 浓硫酸稀释 |
C、 分离出AgNO3溶液中AgCl |
D、 称量30.46g的NaOH固体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、醋酸钠的水解:CH3COO-+H2O=CH3COOH+OH- |
| B、碳酸氢钠的水解:HCO3-+H2O?H3O++CO32- |
| C、硫酸氢钠溶液与氢氧化铝反应:H++OH-=H2O |
| D、碳酸氢钾与氢氧化钾溶液反应:HCO3-+OH-=H2O+CO32- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、标准状况下,11.2L SO3含有0.5NA分子 |
| B、1mol Na2O2和足量的CO2反应转移的电子数为2NA |
| C、常温常压下,32g O2和O3混合气体所含氧原子数一定是2NA |
| D、22.4L CO和CO2的混合气体中所含的碳原子数一定是NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
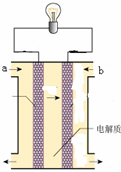 如图所示是一个燃料电池的示意图,当燃料电池如下时,其分析中正确的是( )
如图所示是一个燃料电池的示意图,当燃料电池如下时,其分析中正确的是( )| A、如果a极通入H2,b极通入O2,NaOH溶液作电解质溶液,则通H2的电极上发生的反应为:H2-2e-=2H+ |
| B、如果a极通入H2,b极通入O2,H2SO4溶液作电解质溶液,则通O2的电极上发生的反应为:O2+4e-+2H2O=4OH- |
| C、如果a极通入CH4,b极通入O2,NaOH作电解质溶液,则通CH4的电极上发生的反应为:CH4-8e-+10 OH-=CO32-+7H2O |
| D、如果a极通入H2,b极通入O2,NaOH溶液作电解质溶液,则溶液中的OH-离子向b极附近移动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、SO3溶于水能导电,但SO3是非电解质 |
| B、酸、碱、盐是电解质,都有很强的导电能力 |
| C、电解质在水中一定能导电,在水中导电的化合物一定是电解质 |
| D、纯水的导电性很差,所以水不是电解质 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| X | Y | |
| Z | W |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com