
【题目】下表是元素周期表的一部分,表中所列的字母分别代表某一元素。
B | C | D | |||||
A | E | F | |||||
(1)A的的最高价氧化物对应水化物的电子式为__________。
(2)R是由表中已标出的A~F 中某三种元素组成的化合物,是常见家用消毒剂的主要成分,其化学名称为_____________;Na2FeO4是工业常用的消毒剂,利用R 制备Na2FeO4的原理如下,请补齐缺少的物质,并配平反应方程式的系数:___ Fe(OH)3 + ___R(________) + ___ NaOH = ____ Na2FeO4 + ___ NaCl + ____H2O
(3)气态氢化物沸点:D _____ E;元素形成的简单离子的半径:A _____ D(填“>”,“<”或“=”)
(4)E 的某种氧化物通入F 单质的水溶液中,并不能增大F 单质水溶液的漂白性,请结合方程式说明______________________________________________________________。
(5)由表中未标出的某种金属元素的单质G ,可以发生如图所示的转化:
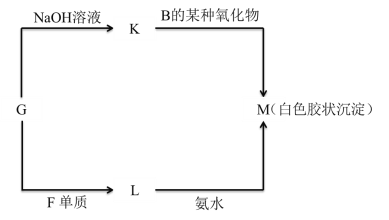
①写出 G 转化为 K 的化学方程式________________________________________。
②写出 L 转化为 M 的离子方程式________________________________________。
【答案】![]() 次氯酸钠2 3(NaClO)4 2 3 5><SO2 + Cl2 + 2H2O = H2SO4 + 2HCl 或 SO2 + Cl2 + 2H2O = 4H+ + SO42 + 2Cl2Al + 2NaOH + 2H2O = 2NaAlO2 + 3H2↑Al3+ + 3NH3H2O = Al(OH)3↓ + 3NH4+
次氯酸钠2 3(NaClO)4 2 3 5><SO2 + Cl2 + 2H2O = H2SO4 + 2HCl 或 SO2 + Cl2 + 2H2O = 4H+ + SO42 + 2Cl2Al + 2NaOH + 2H2O = 2NaAlO2 + 3H2↑Al3+ + 3NH3H2O = Al(OH)3↓ + 3NH4+
【解析】
根据元素周期表的结构分析,A为钠,B为碳,C为氮,D为氧,E为硫,F为氯。据此解答。
(1)氢氧化钠的电子式为![]() 。(2)R是常见家用消毒剂的主要成分,其化学名称为次氯酸钠;Na2FeO4是工业常用的消毒剂,利用次氯酸钠制备Na2FeO4,氯元素的化合价从+1价降低到-1价,铁元素的化合价从+3价升高到+6价,所以氯元素和铁元素的物质的量比为3:2,再根据元素质量守恒分析其他物质的化学计量数,得到方程式为:2Fe(OH)3 +3 NaClO + 4NaOH = 2Na2FeO4 +3NaCl +5H2O。(3)水分子间存在氢键,所以其沸点比硫化氢高;钠离子和氧离子电子层结构相同,根据核电荷数越大,半径越小分析,钠离子半径小于氧离子半径。(4)二氧化硫和氯气和水反应生成硫酸和盐酸,减少了氯水中的次氯酸的存在,即减少了漂白性,方程式为:SO2+Cl2+2H2O=H2SO4+2HCl或SO2+Cl2+2H2O=4H++SO42+2Cl。(5)金属元素的单质G能与氢氧化钠反应,说明为金属铝,铝和氢氧化钠反应生成偏铝酸钠,方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2,偏铝酸钠和二氧化碳反应生成氢氧化铝沉淀,铝和氯气反应生成氯化铝,氯化铝和氨水反应生成氢氧化铝沉淀和氯化铵,离子方程式为:Al3++ 3NH3H2O=Al(OH)3↓+3NH4+。
。(2)R是常见家用消毒剂的主要成分,其化学名称为次氯酸钠;Na2FeO4是工业常用的消毒剂,利用次氯酸钠制备Na2FeO4,氯元素的化合价从+1价降低到-1价,铁元素的化合价从+3价升高到+6价,所以氯元素和铁元素的物质的量比为3:2,再根据元素质量守恒分析其他物质的化学计量数,得到方程式为:2Fe(OH)3 +3 NaClO + 4NaOH = 2Na2FeO4 +3NaCl +5H2O。(3)水分子间存在氢键,所以其沸点比硫化氢高;钠离子和氧离子电子层结构相同,根据核电荷数越大,半径越小分析,钠离子半径小于氧离子半径。(4)二氧化硫和氯气和水反应生成硫酸和盐酸,减少了氯水中的次氯酸的存在,即减少了漂白性,方程式为:SO2+Cl2+2H2O=H2SO4+2HCl或SO2+Cl2+2H2O=4H++SO42+2Cl。(5)金属元素的单质G能与氢氧化钠反应,说明为金属铝,铝和氢氧化钠反应生成偏铝酸钠,方程式为:2Al+2NaOH+2H2O=2NaAlO2+3H2,偏铝酸钠和二氧化碳反应生成氢氧化铝沉淀,铝和氯气反应生成氯化铝,氯化铝和氨水反应生成氢氧化铝沉淀和氯化铵,离子方程式为:Al3++ 3NH3H2O=Al(OH)3↓+3NH4+。


科目:高中化学 来源: 题型:
【题目】500 mL KNO3和Cu(NO3)2的混合溶液中c(NO3-)=6.0 mol·L-1,用石墨做电极电解此溶液,当通电一段时间后,两极均收集到22.4 L气体(标准状况),假定电解后溶液体积仍为500 mL,下列说法正确的是( )
A. 原混合溶液中c(K+)为2 mol·L-1
B. 上述电解过程中共转移6 mol电子
C. 电解得到的Cu的物质的量为0.5 mol
D. 电解后溶液中c(H+)为2 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关1~18号元素的原子核外电子排布规律的描述正确的是( )
A.最外层电子数为1的金属元素有3种
B.最外层电子数为2的元素一定是金属元素
C.K层与L层电子数之比为1:2的元素有2种
D.最外层电子数为8的元素一定是稀有气体元素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中华人民共和国国家标准(GB2760-2011)规定葡萄酒中SO2最大使用量为0.25g·L-1。某兴趣小组用题图1装置(夹持装置略)收集某葡萄酒中SO2,并对其含量进行测定。
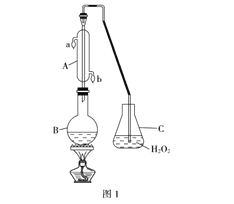
(1)B中加入300.00mL葡萄酒和适量盐酸,加热使SO2全部逸出并与C中H2O2完全反应,其化学方程式为_______________________________________________________。
(2)除去C中过量的H2O2,然后用0.0900mol·L-1NaOH标准溶液进行滴定。若滴定前俯视,滴定后仰视,对滴定结果的影响是____________(填无影响、偏高或偏低);若滴定前滴定管尖嘴有气泡,滴定后气泡消失,对滴定结果的影响是____________(填无影响、偏高或偏低);若滴定终点时溶液的pH=8.8,则选择的指示剂为___________________;滴定终点的判断为_____________________________________________。
(3)滴定至终点时,消耗NaOH溶液25.00mL,该葡萄酒中SO2含量为:__________g·L-1。
(4)该测定结果比实际值偏高,分析原因并利用现有装置提出改进措施______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列所得溶液的物质的量浓度一定为1.0mol/L 的是
A. 1.0克 NaCl固体溶于1L水中所得溶液
B. 1mol NaCl固体溶于1L水中所得溶液
C. 22.4L HCl气体溶于水配成1L溶液
D. 4.0克NaOH固体溶于水配成100mL溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学是以实验为基础的科学,以下实验是高一学生必须掌握的基本实验,请根据实验内容完成下列问题;
(1)下图是从海带中提取碘单质的过程:
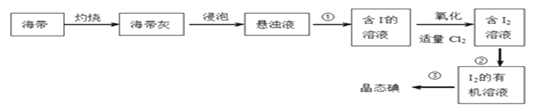
①进行实验①的操作名称是:_________________。
②在进行实验②的过程中,可以选择的有机溶剂是____________。
A.乙醇 B.四氯化碳 C.苯 D. 乙酸
③从I2的有机溶液中提取碘的装置如图所示,仪器a的名称为:_______。
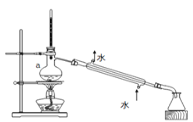
④向含I-的溶液中加入适量氯气发生反应的离子方程式为:__________________________。
(2)下图是实验室制取乙酸乙酯的实验装置,回答下列问题:
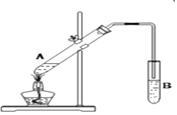
①在A试管中加入试剂的顺序是___________ (填以下字母序号)。
a.先浓硫酸再乙醇后乙酸 b.先浓硫酸再乙酸后乙醇 c.先乙醇再浓硫酸后乙酸
②在试管B中常加入_______________ 来接收乙酸乙酯。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com