
【题目】一切植物中均含有天然有机高分子化合物A,它是构成植物细胞壁的基础物质,不溶于水,也不溶于一般的有机溶剂。各物质之间的转化关系如下所示(A~F均分别代表一种物质,部分产物略去):
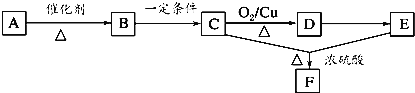
已知:B生成C的同时还有CO2生成,请回答下列问题:
(1)由A生成B的化学方程式为 ______。
(2)B、C均含有的官能团名称是 ______。
(3)A→F发生反应的反应类型有 ______(填序号)。
A.氧化反应 B.酯化反应 C.加成反应 D.水解反应
(4)写出C→D所发生反应的化学方程式:______。
(5)F有多种同分异构体,请写出与它具有相同官能团且能发生银镜反应的所有同分异构体 ______。
【答案】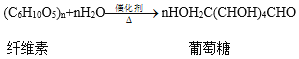 羟基 ABD 2C2H5OH+O2
羟基 ABD 2C2H5OH+O2![]() 2CH3CHO+2H2O HCOOCH2CH2CH3、HCOOCH(CH3)2
2CH3CHO+2H2O HCOOCH2CH2CH3、HCOOCH(CH3)2
【解析】
构成细胞壁的天然高分子化合物为纤维素,则A的结构简式为(C6H10O5)n,纤维素水解最终生成葡萄糖,则B结构简式为HOH2C(CHOH)4CHO,B反应生成C,C和E在浓硫酸、加热条件下发生酯化反应,则C结构简式为CH3CH2OH,D结构简式为CH3CHO、E结构简式为CH3COOH、F结构简式为CH3COOCH2CH3,据此分析解答。
根据上述推断可知A是(C6H10O5)n,B是HOH2C(CHOH)4CHO,C是CH3CH2OH,D是CH3CHO、E是CH3COOH、F是CH3COOCH2CH3。
(1)A是纤维素、B是葡萄糖,纤维素在催化剂、加热条件下水解生成葡萄糖,则由A生成B的化学方程式为: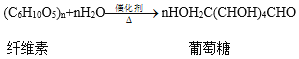 ;
;
(2) B结构简式HOH2C(CHOH)4CHO,C结构简式是CH3CH2OH,B、C均含有的官能团名称是羟基;
(3)纤维素发生水解反应生成葡萄糖,葡萄糖发酵生成乙醇,乙醇被氧化生成乙醛,乙醛被氧化生成乙酸,乙醇和乙酸发生酯化反应生成乙酸乙酯,所以发生的反应有水解反应、氧化反应、取代反应或酯化反应,故合理选项是ABD;
(4) C是乙醇、D是乙醛,乙醇在催化剂存在和加热条件下发生氧化反应生成乙醛,反应方程式为2C2H5OH+O2![]() 2CH3CHO+2H2O;
2CH3CHO+2H2O;
(5)F为乙酸乙酯,F有多种同分异构体,与它具有相同官能团且能发生银镜反应,说明其同分异构体中含有甲酯基,烷基可能是-CH2CH2CH3、-CH(CH3)2,该物质可能的同分异构体结构简式为HCOOCH2CH2CH3、HCOOCH(CH3)2。


科目:高中化学 来源: 题型:
【题目】研究证明高铁酸钠![]() 是一种“绿色环保高效”消毒剂,比目前国内外广泛使用的含氯饮用水消毒剂性能更为优良。高铁酸钠只能在碱性环境中稳定存在。下列是通过次氯酸钠氧化法制备高铁酸钠并探究其性质的实验,步骤如下:
是一种“绿色环保高效”消毒剂,比目前国内外广泛使用的含氯饮用水消毒剂性能更为优良。高铁酸钠只能在碱性环境中稳定存在。下列是通过次氯酸钠氧化法制备高铁酸钠并探究其性质的实验,步骤如下:
Ⅰ![]() 用氯气和氢氧化钠溶液反应制备NaClO溶液
用氯气和氢氧化钠溶液反应制备NaClO溶液
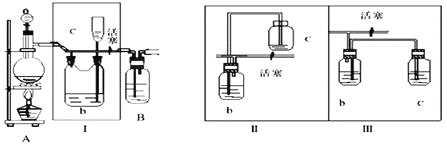
(1)![]() 是氯气发生装置,写出实验室用此装置制取氯气的离子方程式___________。
是氯气发生装置,写出实验室用此装置制取氯气的离子方程式___________。
(2)Ⅰ装置的作用是__________。
(3)用图示的Ⅱ或Ⅲ代替Ⅰ是否可行?___________。简要说明理由_________________________。
(4)将产生的氯气通入D装置中制NaClO溶液
已知:![]() 为了防止产生
为了防止产生![]() ,除搅拌和混入
,除搅拌和混入![]() 稀释外,还应采取的操作是___________________________。
稀释外,还应采取的操作是___________________________。
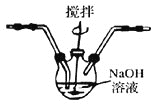
Ⅱ![]() 制备
制备![]()
(1)将![]() 溶液加入到NaOH与NaClO的混合溶液中,过滤得到粗产品,再用NaOH溶液溶解,重结晶,用有机溶剂脱碱,低温烘干得到固体样品,上述制备过程中,用NaOH溶液溶解粗产品而不用水的原因是______________________________。
溶液加入到NaOH与NaClO的混合溶液中,过滤得到粗产品,再用NaOH溶液溶解,重结晶,用有机溶剂脱碱,低温烘干得到固体样品,上述制备过程中,用NaOH溶液溶解粗产品而不用水的原因是______________________________。
(2)高铁酸钠电池是一种新型可充电电池,电解质为NaOH溶液,放电时负极材料为Zn,正极产生红褐色沉淀,写出该电池反应的化学方程式_______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知热化学方程式:
H2O(g)=H2(g)+![]() O2(g)△H=+241.8kJ·mol-1
O2(g)△H=+241.8kJ·mol-1
H2(g)+![]() O2(g)=H2O(1)△H=-285.8kJ·mol-1
O2(g)=H2O(1)△H=-285.8kJ·mol-1
当1g液态水变为水蒸气时,其热量变化是( )
A.吸热88kJ B.吸热44 kJ C.放热44kJ D.吸热2.44 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)写出下列物质在水溶液中电离的方程式:
HNO3__;
HClO__;
NaHCO3__、___。
(2)在25℃、101kPa下,1g甲醇燃烧生成CO2和液态水时放热22.68kJ。则表示甲醇燃烧热的热化学方程式为___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学对Cl2与KI溶液的反应进行了实验探究。反应装置如下:
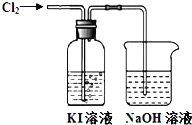
通入氯气一段时间,KI溶液变为黄色。继续通入氯气一段时间后,溶液黄色褪去,变为无色。继续通入氯气,最后溶液变为浅黄绿色。
(1)Cl2与NaOH溶液反应的化学方程式是___。
(2)KI溶液变为黄色说明氯气具有的___性,该反应的离子方程式是___。
(3)已知I2+I-![]() I3-,I2、I3-在水中均呈黄色。为确定黄色溶液的成分,进行了以下实验。
I3-,I2、I3-在水中均呈黄色。为确定黄色溶液的成分,进行了以下实验。
①实验b的目的是___。
②根据实验a中,水层中含有的粒子有___。
操作 | 实验现象 | |
a | 取2~3mL黄色溶液,加入足量CCl4,振荡静置 | CCl4层呈紫红色,水层显浅黄色 |
b | 取2~3mL饱和碘水,加入足量CCl4,振荡静置 | CCl4层呈紫红色,水层几近无色 |
③实验a中水溶液颜色变浅的原因是___。
④为保证实验的严谨性,在实验a、b的基础上,需补充一个实验,该实验为___。
(4)通入氯气,溶液由黄色变为无色,是因为氯气将I2氧化,已知1molCl2可氧化0.2molI2,该反应的化学方程式是___。
(5)根据上述实验,请预测向淀粉-KI溶液中持续通入氯气,可能观察到的现象为___。
(6)溶液最终变为浅绿色的原因是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知 2CH3OH(g)![]() C2H4(g)+2H2O(g)。 某研究小组将甲醇蒸气以一定的流速持续通过相同量的同种催化剂, 不同温度得到如下图像, 则下列结论不正确的是
C2H4(g)+2H2O(g)。 某研究小组将甲醇蒸气以一定的流速持续通过相同量的同种催化剂, 不同温度得到如下图像, 则下列结论不正确的是
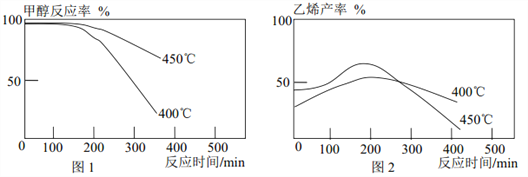
A. 一段时间后甲醇反应率下降可能是催化剂活性下降
B. 综合图 1、 图 2 可知, 甲醇还发生了其他反应
C. 若改变甲醇蒸气的流速, 不会影响甲醇反应率和乙烯产率
D. 制乙烯比较适宜的温度是 450℃左右
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】部分果蔬中含有下列成分:
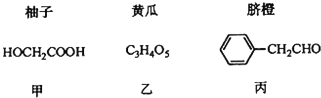
已知:①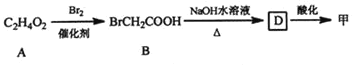
C2H4O2![]() BrCH2COOH
BrCH2COOH![]() D
D![]() 甲
甲
②1mol乙消耗NaHCO3的物质的量是甲的2倍
③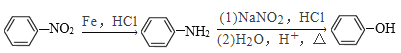
回答下列问题:
(1)甲可由已知①得到。
①甲中含有不饱和键的官能团名称为______。
②A→B为取代反应,A的结构简式为______。
③B→D的化学方程式为______。
(2)乙在一定条件下生成链状酯类有机高分子化合物的化学方程式为______。
(3)由丙经下列途径可得一种重要的医药和香料中间体J(部分反应条件略去):

①用化学方法除去E中残留的少量丙(室温时E和丙呈液态,忽略它们在水中的溶解),第1步加入试剂的名称为______ ,第2、3操作分别是过滤、分液。
②经E→G→H保护的官能团是______,可以表征有机化合物中存在何种官能团的仪器是______。
③J的同分异构体中在核磁共振氢谱上显示为两组峰,峰面积比为3:2的链状且不存在支链的异构体共有______ 种(不含立体异构),其中某异构体L中的官能团都能与H2发生加成反应,则L的结构简式为______ (只写一种)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F、G、H 是元素周期表前四周期常见元素,且原子序数依次增大,其相关信息如下表:
元素 | 相关信息 |
A | 原子核外有 6 种不同运动状态的电子 |
C | 基态原子中 s 电子总数与p 电子总数相等 |
D | 原子半径在同周期元素中最大 |
E | 基态原子最外层电子排布式为 3s23p1 |
F | 基态原子的最外层 p 轨道有两个电子的自旋方向与其他电子的自 旋方向相反 |
G | 基态原子核外有 7 个能级且能量最高的能级上有 6 个电子 |
H | 是我国使用最早的合金中的最主要金属元素 |
(1) A 元素的名称是_______________;A 元素和 F 元素形成的最简单化合物的分子构型为_______________,该分子是_______________分子。(填“极性”或“非极性”)
(2) B 元素形成的单质分子中σ键与π键数目之比为_______________。
(3) G 元素的低价阳离子的离子结构示意图是_______________。
(4) G 的高价阳离子的溶液与 H 单质反应的离子方程式为___________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关阿伏加德罗常数NA的叙述中不正确的是( )
A.1mol NaHSO4固体所含的阳离子数目为NA
B.常温常压下,92 g的NO2和N2O4混合气体含有的原子数为6NA
C.标准状况下,22.4L HF含有电子数为8NA
D.60g石英晶体中含有的Si-O键数目为4NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com