
【题目】根据下列图示所得出的结论不正确的是( )
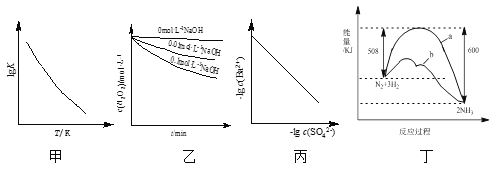
A.图甲是CO(g)+H2O(g)![]() CO2(g)+H2(g)的lgK与反应温度T的关系曲线,说明该反应的ΔH<0
CO2(g)+H2(g)的lgK与反应温度T的关系曲线,说明该反应的ΔH<0
B.图乙是70℃时不同pH条件下H2O2浓度随时间的变化曲线。说明其他条件相同时,溶液pH越小,H2O2分解速率越快
C.图丙是室温下用Na2SO4除去溶液中Ba2+达到沉淀溶解平衡时,溶液中c(Ba2+)与c(SO![]() )的关系曲线,说明溶液中c(SO
)的关系曲线,说明溶液中c(SO![]() )越大c(Ba2+)越小
)越大c(Ba2+)越小
D.图丁是合成氨反应过程中能量变化曲线,说明该反应为放热反应,且b表示在反应体系中加入了催化剂
【答案】B
【解析】
A.根据图知,升高温度,化学平衡常数减小,说明平衡逆向,升高温度平衡向吸热方向移动,则逆反应是吸热反应,正反应是放热反应,即正反应△H<0,故A正确;
B.图乙中H2O2浓度相同,但加入NaOH浓度不同,说明溶液的pH不同,NaOH浓度越大,相同时间内双氧水浓度变化量越大,由此得出:双氧水浓度相同时,pH越大双氧水分解速率越快,故B错误;
C.温度不变,溶度积常数不变,Ksp(BaSO4)=c(Ba2+)![]() c(SO42-),c(Ba2+)与c(SO42-)成反比,则c(SO42-)越大c(Ba2+)越小,故C正确;
c(SO42-),c(Ba2+)与c(SO42-)成反比,则c(SO42-)越大c(Ba2+)越小,故C正确;
D.反应物总能量大于生成物总能量为放热反应,催化剂降低反应所需的活化能,焓变不变,则图2表明合成氨反应是放热反应,b表示在反应体系中加入了催化剂,故D正确。
答案选B。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】一定温度下,在某2 L恒容密闭容器中加入纳米级氧化亚铜并通入0.1 mol 水(g),发生如下反应:2H2O(g)![]() 2H2(g)+O2(g) ΔH=+484 kJ·mol-1。不同时间产生O2的物质的量见下表:
2H2(g)+O2(g) ΔH=+484 kJ·mol-1。不同时间产生O2的物质的量见下表:
时间/min | 20 | 40 | 60 | 80 |
n(O2)/mol | 0.0010 | 0.0016 | 0.0020 | 0.0020 |
下列说法不正确的是( )
A.前20 min内的平均反应速率v(H2O)=5×10-5mol·L-1·min-1
B.达到平衡时,需要从外界吸收的能量为0.968 kJ
C.增大水的浓度,可以改变待反应的限度
D.使用纳米级的氧化亚铜,可以增大平衡时氧气的体积分数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如右图所示,把试管放入盛有25 ℃饱和澄清石灰水的烧杯中,试管中开始放入几小块镁片,再用滴管滴入10 mL盐酸于试管中,试回答下列问题:
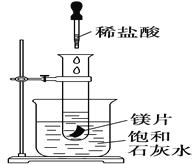
(1)实验中观察到的现象是________________________________ 。
(2)产生上述现象的原因是____________________________。
(3)写出有关反应的离子方程式:_________________________________;
反应中转移了0. 04mol电子时;标准状况下产生多少________mL的H2;消耗镁多少________g(保留两位小数);生成的MgCl2物质的量浓度为________。(溶液体积保持不变)
(4)由实验推知,镁片溶液和盐酸的总能量________(填“大于”、“小于”或“等于”) MgCl2和H2的总能量;此反应为________ (填放热反应或者吸热反应)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关硫元素及其化合物的相关化学用语表示正确的是( )
A.质子数为16,中子数为16的硫原子:![]() S
S
B.硫化钠的电子式:![]()
C.二硫化碳分子的比例模型:![]()
D.NaHSO3电离方程式:NaHSO3=Na++H++SO![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关物质的性质与用途具有对应关系的是( )
A.NaClO溶液具有碱性,可用于杀菌消毒
B.NH3具有还原性,可用于检验HCl泄漏
C.FeCl3溶液能与Cu反应,可用于蚀刻印刷电路板
D.漂白粉在空气中不稳定,可用于漂白纸浆
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下图所示的实验,回答问题:
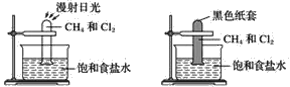
(1)装置A中的实验现象是____________________装置B中的实验现象是____
(2)根据上述实验,你能得出的结论是________________________________
(3)写出上述实验A中反应的化学方程式:
____________________________________________________;
____________________________________________________;
___________________________________________________;
______________________________________________________。
(4)上述反应的反应类型是________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在常温下的一密闭容器中事先放入1.56g过氧化钠,然后再通入乙烷与氧气的混合气体,用电火花引爆,直至反应完全为止,恢复到原温度,容器内压强近似为零。
(1)相同条件下,通入的气体氧气和乙烷的体积比是多少?_____
(2)通入氧气的质量最大应是多少?_____
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中常用下列反应制取氯气:MnO2 + 4HCl(浓)![]() MnCl2 + Cl2↑+ 2 H2O
MnCl2 + Cl2↑+ 2 H2O
(1)用双线桥或单线桥的方式表示该反应电子转移的方向和数目:________
(2)该反应中还原剂是________;
(3)标准状况下,收集到2.24 L Cl2时,被氧化的还原剂的物质的量为_____mol,转移电子的物质的量为____mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在水溶液中,重铬酸钾K2Cr2O7存在以下平衡:Cr2O72-+H2O![]() 2CrO42-+2H+,下列说法正确的是( )
2CrO42-+2H+,下列说法正确的是( )
A.向该溶液中加入过量浓NaOH溶液后,溶液呈橙红色
B.该反应是氧化还原反应
C.向该溶液中滴加适量的浓硫酸,平衡向逆反应方向移动,再次达到平衡后,氢离子浓度比原溶液大
D.该反应的平衡常数表达式是K=c2(CrO42-)c2(H+)/c(Cr2O72-)c(H2O)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com