
X、Y、Z、W四种常见元素,其中X、Y、Z为短周期元素。有关信息如下表:
| | 原子或分子相关信息 | 单质及其化合物相关信息 |
| X | ZX4分子是由粗Z提纯Z的中间产物 | X的最高价氧化物对应的水化物为无机酸中最强酸 |
| Y | Y原子的最外层电子数等于电子层数 | Y的氧化物是典型的两性氧化物,可用于制造一种极有前途的高温材料 |
| Z | Z原子的最外层电子数是次外层电子数的1/2 | Z是无机非金属材料的主角,其单质是制取大规模集成电路的主要原料 |
| W | W原子的最外层电子数小于4 | W的常见化合价有+3、+2,WX3稀溶液呈黄色 |
(1)第四周期 VIII族 4Fe(OH)2+O2+2H2O="=" 4Fe(OH)3
(2)  6H++Al2O3=2Al3++3H2O (3)光导纤维 SiO2+2C
6H++Al2O3=2Al3++3H2O (3)光导纤维 SiO2+2C Si+2CO↑ Ge+2 H2O2+2NaOH=Na2GeO3+3H2O (4)360
Si+2CO↑ Ge+2 H2O2+2NaOH=Na2GeO3+3H2O (4)360
解析试题分析:(1)根据题意可知:X是氯;Y是铝;Z是硅;W是铁。铁在所以周期表中位于第四周期第Ⅷ族。氢氧化亚铁在空气中被氧化的方程式是 4Fe(OH)2+O2+2H2O="=" 4Fe(OH)3(2)Cl-离子的结构示意图是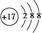 。氧化铝是两性氧化物,既能与强酸反应又能与强碱反应生成盐和水。高氯酸与氧化铝反应的离子方程式是:6H++Al2O3=2Al3++3H2O (3)SiO2广泛用作光导纤维。工业上制备单质硅的化学反应方程式是:SiO2+2C
。氧化铝是两性氧化物,既能与强酸反应又能与强碱反应生成盐和水。高氯酸与氧化铝反应的离子方程式是:6H++Al2O3=2Al3++3H2O (3)SiO2广泛用作光导纤维。工业上制备单质硅的化学反应方程式是:SiO2+2C Si+2CO↑ 锗在有H2O2存在时可与NaOH 溶液反应生成锗酸盐,其方程式为Ge+2 H2O2+2NaOH=Na2GeO3+3H2O (4)AlCl3+3NaOH=Al(OH)3↓+3NaCl。Al(OH)3++NaOH=NaAlO2+2H2O。n(AlCl3)=0.05mol,n(Al(OH)3)="m/M=1.56" g÷78g/mol=0.02mol.n(AlCl3)>n(Al(OH)3).沉淀没有达到最大值,一种情况是加入的氢氧化钠不足量,另一种情况是加入的氢氧化钠过量,溶解了一部分产生氢氧化铝沉淀。加入NaOH溶液的体积最多时是第二种情况n(NaOH)=4n(AlCl3)-n(Al(OH)3)=4×0.05mol-0.02mol=0.18mol.所以氢氧化钠的体积是V="n/C=0.18mol÷0.5" mol·L-1=0.36L=360ml.
Si+2CO↑ 锗在有H2O2存在时可与NaOH 溶液反应生成锗酸盐,其方程式为Ge+2 H2O2+2NaOH=Na2GeO3+3H2O (4)AlCl3+3NaOH=Al(OH)3↓+3NaCl。Al(OH)3++NaOH=NaAlO2+2H2O。n(AlCl3)=0.05mol,n(Al(OH)3)="m/M=1.56" g÷78g/mol=0.02mol.n(AlCl3)>n(Al(OH)3).沉淀没有达到最大值,一种情况是加入的氢氧化钠不足量,另一种情况是加入的氢氧化钠过量,溶解了一部分产生氢氧化铝沉淀。加入NaOH溶液的体积最多时是第二种情况n(NaOH)=4n(AlCl3)-n(Al(OH)3)=4×0.05mol-0.02mol=0.18mol.所以氢氧化钠的体积是V="n/C=0.18mol÷0.5" mol·L-1=0.36L=360ml.
考点:考查元素的推断及氧化铝、氢氧化铝的两性等知识。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:填空题
前四周期原子序数依次增大的元素A、B、C、D中,A和B的价电子层中未成对电子均只有1个,并且A_和B+的电子相差为8;与B位于同一周期的C和D,它们价电子层中的未成对电子数分别为4和2,且原子序数相差为2。回答下列问题:
(1)D2+的价层电子排布图为_______________。
(2)四种元素中第一电离最小的是_________________,电负性最大的是________________。(填元素符号)
(3)A、B和D三种元素组成的一个化合物的晶胞如图所示。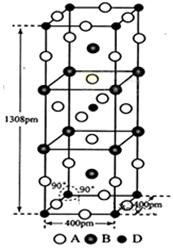
①该化合物的化学式为_____________;D的配位数为_______;
②列式计算该晶体的密度为___________g·cm-3。(列式并计算)
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
A、B、C、D、E五种短周期元素,A与D同周期,A的单质既可与盐酸反应,又可与NaOH溶液反应,B的单质在放电条件下能与氧气反应,C元素的离子不含电子,D元素原子的最外层电子数是其次外层电子数的3/4,E元素原子的最外层电子数是其次外层电子数的3倍。
(1)A的原子结构示意图为 。
(2)0.1 mol/L A的硫酸盐溶液与0.1 mol/L NaOH溶液等体积混合,反应的离子
方程式为 。
(3)以A的单质和NiO(OH)为电极,NaOH溶液为电解液组成一种新型电池,放电时NiO(OH)转化为Ni(OH)2,该电池总反应的化学方程式是 。
(4)化合物甲由元素A、B组成,具有良好电绝缘性。
化合物甲能与水缓慢反应生成含B的化合物乙,乙分子中含有10个电子。写出该
反应的化学方程式: 。
工业用A的单质和化合物乙在高于1700K反应制备甲。已知该反应可以认为是置
换反应,该反应的化学方程式是 。
(5)D和E两种元素相比较,非金属性较强的是(填元素名称) ,可以验证该结论的是(填写编号) ;
a.比较这两种元素的常见单质的沸点
b.比较这两种元素的单质与氢气化合的难易
c.比较这两种元素的气态氢化物的稳定性
(6)C、D、E间可形成丙、丁两种分子,它们均含有18个电子,则丙与丁反应生成D单质的化学方程式为 ;
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
A、B、C、D、E五种元素,它们原子的核电荷数依次递增且均小于18。A元素原子核外只有1个电子;C是地壳中含量最多的元素;B、C可形成两种化合物BC和BC2,B的最高正价与最低负价绝对值相等,BC有毒,BC2可用于灭火;D元素的最外层电子数是其电子层数的三分之一;E—具有与Ar原子相同的电子层结构。
(1)写出A、C两种元素的符号:A , C 。
(2)写出D原子和E—离子的结构示意图:D原子 ,E—离子 。
(3)由A、B、C、D四种元素组成的常见化合物的化学式为 ,
其电离方程式为 。
(4)写出A、C、D三种元素组成的常见化合物的稀溶液,常温下和E的单质反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
U、V、W、X、Y、Z是原子序数依次增大的六种常见元素。Y的单质在W2中燃烧的产物可使品红溶液褪色。Z和W元素形成的化合物Z3W4具有磁性。U的单质在W2中燃烧可生成UW和UW2两种气体。X的单质是一种金属,该金属在UW2中剧烈燃烧生成黑、白两种固体。
请回答下列问题:
(1)V的单质分子的结构式为 ,XW的电子式为 ;
(2)Z元素在周期表中的位置是 。
(3)元素U、V、W形成的10电子氢化物中,沸点较低的是 (写化学式);结合H+能力较强的是 (写化学式);用一个离子方程式加以说明 。
(4)YW2气体通入BaCl2和HNO3的混合溶液,生成白色沉淀和无色气体VW,有关反应的离子方程式为 ,由此可知VW和YW2还原性较强的是 (写化学式)。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
X、Y、Z、M、Q、G六种短周期元素,原子序数依次增大。X、Z同主族,可形成离子化合物ZX;Y、M同主族,Y的一种同位素原子常用于测定文物的年代;Q形成的单质为淡黄色固体。请回答下列问题(涉及物质均用化学式表示)。
(1)离子化合物ZX中X离子的结构示意图为 ; Y在元素周期表中的位置是_______________。
(2)上述元素的最高价氧化物对应的水化物酸性最强的是_______________,Q与G的气态氢化物还原性更强的是__________________。
(3)工业上制备M的高纯度单质,其中一个重要反应是:由MXG3与X2在高温下反应。该反应过程必须控制无水无氧,因为MXG3遇水剧烈反应生成H2、 和 ,而混入氧气,引起的后果是 。
(4)X2Q的燃烧热为a kJ·mol-1,下列X2Q燃烧反应的热化学方程式正确的是 。
| A.2X2Q(g) + O2(g) =" 2Q(s)" + 2X2O(g)△H=" -2a" kJ·mol-1 |
| B.X2Q(g) + 2O2(g) = QO3(g) + X2O(l)△H=" +a" kJ·mol-1 |
| C.2X2Q(g)+ 3O2(g) = 2QO2(g) + 2X2O(l)△H=" -2a" kJ·mol-1 |
| D.X2Q(g) + 2O2(g) = QO3(g) + X2O(l)△H=" -a" kJ·mol-1 |
 Fe + 2ZG 放电时,电池的正极反应式为: 该电池的电解质为___________________。
Fe + 2ZG 放电时,电池的正极反应式为: 该电池的电解质为___________________。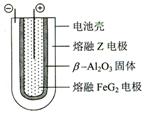
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
X、Y、Z、L、M五种元素的原子序数依次增大。X、Y、Z、L是组成蛋白质的基础元素,M是地壳中含量最高的金属元素。
回答下列问题:
⑴ L的元素符号为________;M在元素周期表中的位置为____________;
⑵ Z、X两元素按原子数目比2∶4构成分子则其结构式为____________。
⑶ 硒(se)是人体必需的微量元素,与L同一主族,Se原子比L原子多两个电子层,则其最高价氧化物对应的水化物化学式为_______。该族2 ~ 5周期元素单质分别与H2反应生成l mol气态氢化物的反应热如下:
a.+99.7 mol·L-1 b.+29.7 mol·L-1 c.-20.6 mol·L-1 d.-241.8 kJ·mol-1
其中表示生成1 mol硒化氢反应热的是__________(填字母代号)。
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
A、B、C、D、E、F为原子序数依次增大的六种元素,其中A、B、C、D、E为短周期主族元素。常温下A、B、C的常见单质均为无色、无味的气体,D、E的单质均为固体。C与E同主族,且E的原子序数为C的2倍,D的最外层电子数比最内层多1个,F是人体血红蛋白中含有的一种金属元素,请回答下列问题:
(1)D元素在周期表中的位置是: 周期 族。
(2)A与C形成的18电子分子的结构式为: 。
(3)最近意大利罗马大学的Funvio Cacace等人获得了极具理论研究意义的B4分子。B4分子结构如图所示,已知断裂l molB-B吸收167kJ热量,生成1 mo1B2放出942kJ热量。根据以上信息和数据,下列说法正确的是 。
A.B4沸点比P4(白磷)低,属于原子晶体
B.l molB4气体转变为B2吸收882kJ热量
C.B4与B2互为同素异形体
D.B4与B2分子中各原子最外电子层均达到8电子稳定结构
(4)写出过量的F与稀硝酸反应的离子方程式
(5)以D为阳极,在H2SO4溶液中电解,D表面形成氧化膜,阳极电极反应式为 。
(6)在常温,常压和光照条件下,B2在催化剂(TiO2)表面与A2C反应,生成1molBA3(g)和C2时的能量变化值为382.5kJ,此反应BA3生成量与温度的实验数据如下表。则该反应的热化学方程式为 。
| T/K | 303 | 313 | 323 |
| BA3生成量/(10—1mol) | 4.3 | 5.9 | 6.0 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
X、Y、Z、W是元素周期表前四周期中的常见元素,其相关信息如下表:
| 元素 | 相关信息 |
| X | X的某种氢化物能使湿润的红色石蕊试纸变蓝 |
| Y | 单质是良好的半导体材料,广泛应用于光电信息领域 |
| Z | Z的一种核素质量数为27,中子数为14 |
| W | 最高价氧化物对应的水化物是一种不溶于水的蓝色固体 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com