
【题目】亚硝酰氯(NOC1)是一种黄色气体,沸点为-5.5。其液体状态呈红褐色。遇水易水解,伴随有氯伴随有氯化氢生成。某化学兴趣小组按下图装置用Cl2和NO制备NOC1。回答下列相关问题:

(1)仪器a的名称是_____,装置甲中反应的离子方程式是______.
(2)装置乙的作用是____,实验开始时,先打开活塞k,当观察到装置丙中出现____(填现象)时再缓缓通入Cl2.
(3)装置丙中生成NOC1的反应方程式是___,装置丁中冰盐水的作用是______.
(4)经分析该套装置设计上有一处明显缺陷,改进方法是_____(用文字描述)。
(5)工业制得的NOC1中常含有少量N2O4杂质,为测定产品纯度进行如下实验:称取1.441g样品溶于适量的NaOH溶液中,加入几滴K2CrO4溶液作指示剂,用0.8000mol/L硝酸酸化的AgNO3溶液滴定,若消耗AgNO3溶液的体积为25.00mL,则NOC1的质量分数为___%(保留2位小数);如果AgNO3溶液出现部分变质(变质的部分不参与反应),则测得的NOC1的质量分数会____(填“偏大”或“偏小”)。
【答案】U型管 Cu+4H++2NO3-=Cu2++2NO2↑+2H2O 将NO2转化为NO,同时吸收HNO3 气体由红棕色转换为无色 2NO+Cl2=2NOCl 冷凝并收集NOCl 在装置中乙和丙之间增加一个盛有浓硫酸的洗气瓶(或在装置中乙和丙之间增加一个气体干燥装置) 90.91 偏大
【解析】
铜和浓硝酸反应生成二氧化氮气体,二氧化氮和水反应生成硝酸和一氧化氮,一氧化氮和氯气反应生成亚硝酰氯,亚硝酰氯的沸点较低,用冰水收集。
(1)仪器a为U型管,装置甲中为铜和浓硝酸反应生成硝酸铜和二氧化氮和水,离子方程式为Cu+4H++2NO3-=Cu2++2NO2↑+2H2O;
(2)装置乙中水和二氧化氮反应生成硝酸和一氧化氮,硝酸蒸气能溶于水,所以作用为:将NO2转化为NO,同时吸收HNO3 ;实验开始时,观察装置丙中气体由红棕色转换为无色,说明装置中的空气已排尽,再通入氯气。
(3)一氧化氮和氯气反应生成亚硝酰氯,方程式为:2NO+Cl2=2NOCl,冰盐水的作用是冷却亚硝酰氯,并收集。
(4)反应得到的一氧化氮含有水,氯气能和水反应,且亚硝酰氯容易水解,故应在装置中乙和丙之间增加一个盛有浓硫酸的洗气瓶(或在装置中乙和丙之间增加一个气体干燥装置)。
(5)根据NOCl - AgNO3分析,硝酸银的物质的量为0.8000×25×10-3=0.02mol,则亚硝酰氯的质量分数为![]() =90.91%。若硝酸银溶液出现部分变质,则消耗的硝酸银溶液的体积变大,则测得的亚硝酰氯的质量分数会偏大。
=90.91%。若硝酸银溶液出现部分变质,则消耗的硝酸银溶液的体积变大,则测得的亚硝酰氯的质量分数会偏大。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】已知常温下浓度均为0.1 mol·L-1的下列溶液的pH如表:
溶质 | NaF | Na2CO3 | NaClO | NaHCO3 |
pH | 8.1 | 11.6 | 9.7 | 8.4 |
下列有关说法正确的是( )
A. 在相同温度下,同浓度的三种酸溶液的导电能力顺序:H2CO3<HClO<HF
B. 等体积、等物质的量浓度的NaClO溶液与NaF溶液中离子总数大小:N前<N后
C. 若将少量CO2通入NaClO溶液至溶液中,离子方程式为:ClO-+CO2+H2O=HClO+CO32-
D. 向Na2CO3溶液中通入少量的HF气体,化学方程式为Na2CO3+2HF = CO2+H2O+2NaF
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)工业上制备氯化氢气体的化学方程式为___。
(2)实验室用氯化钠与浓硫酸反应制氯化氢气体的方程式___,利用浓硫酸___性。要制得干燥的氯化氢气体,可选用___做干燥剂。
(3)用如图装置进行实验,烧瓶内充满干燥的HCl气体,挤压预先装满水的胶头滴管后,还应该进行的操作是___,能观察到___现象。

(4)标准状况下,用容积为V升的圆底烧瓶,采用排空气法收集干燥的氯化氢,所得气体的平均式量是34.625。喷泉实验后,烧瓶中的溶液的体积为___,物质的量浓度___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知元素A的一价阴离子的电子层结构与氩原子相同,元素B的二价阳离子的电子层结构与氖原子相同。请回答:
(1)元素A离子的结构示意图为___,A的单质呈___色,检验该物质的方法是___。
(2)由A、B形成的化合物的电子式是___。
(3)与A离子具有相同电子数的一种分子是___(填名称)。
(4)A的单质与Ca(OH)2反应的化学方程式___,该反应工业上的用途是___。
(5)蓝色石蕊试纸遇到A的水溶液现象是___,请你解释这个现象___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】决定物质性质的重要因素是物质结构.请回答下列问题.
(1)已知A和B为第三周期元素,其原子的第一至第四电离能如下表所示:

则,A的化合价__B的化合价(填“>”、“<”或“=”).
(2)实验证明:KCl、MgO、CaO、TiN这4种晶体的结构与NaCl晶体结构相似(如图所示),其中3种离子晶体的晶格能数据如下表:

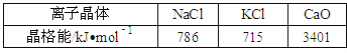
则该 4种离子晶体(不包括NaCl)熔点从高到低的顺序是:__.
(3)金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好.离子型氧化物V2O5和CrO2中,适合作录音带磁粉原料的是___________________________.
(4)某配合物的分子结构如图所示,则N原子的杂化方式为__;基态Ni原子的电子排布式__.
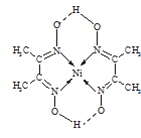
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一容积固定的密闭容器中,可逆反应H2(g)+I2(g) ![]() 2HI(g)达到平衡时的标志是( )
2HI(g)达到平衡时的标志是( )
A.混合气体密度恒定不变B.混合气体的颜色不再改变
C.H2、I2、HI的浓度相等D.I2在混合气体中体积分数不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在下列事实中,各是什么因素影响了化学反应的速率。
(1)黄铁矿煅烧时要粉碎成细小颗粒______________;
(2)夏天的食品变霉,在冬天不易发生该现象_____________;
(3)同浓度同体积的盐酸中放入同样大小的锌粒和镁块,产生气体快慢程度不同__;
(4)同样大小的石灰石分别在0.1 mol·L-1的盐酸和1 mol·L-1的盐酸中反应速度不同_____________;
(5)熔化的KClO3放出气泡很慢,撒入MnO2少量很快产生气体__________;
(6)如下图,铁在海水中的腐蚀速度是②比①快______。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)常温下,将0.2 mol·L-1的某一元酸HA溶液和0.1 mol·L-1NaOH溶液等体积混合后溶液pH大于7,若混合液体积等于两溶液体积之和,则混合液中下列关系正确的是________。
A.c(HA)<c(A-) B.c(HA)一定大于0.1 mol·L-1
C.c(Na+)=c(HA)+c(A-) D.2c(OH-)=2c(H+)+[c(HA)-c(A-)]
(2)在t℃时,某NaOH稀溶液中c(H+)=10-a mol·L-1,c(OH-)=10-b mol·L-1,已知a+b=12,则:
①该温度下水的离子积常数Kw=___________mol2·L-2。
②在该温度下,将100mL0.1 mol·L-1的稀H2SO4与100mL0.4 mol·L-1的NaOH溶液混合后,溶液的pH= _____________。
(3)常温下在20 mL 0.1 mol·L-1Na2CO3溶液中逐滴加入0.1 mol·L-1HCl溶液40 mL,溶液中含碳元素的各种微粒(CO2因逸出未画出)物质的量分数(纵轴)随溶液pH变化的部分情况如下图所示。

回答下列问题:
①在同一溶液中,H2CO3、HCO3-、CO32-________(填“能”或“不能”)大量共存。
②当pH=7时,溶液中各种离子其物质的量浓度之间的等量关系是__________________。
③已知在25 ℃时,CO32-水解反应的平衡常数Kh=c(HCO3-).c(OH-)/c(HCO3-)=2×10-4,当溶液中c(HCO3-)∶c-(CO32-)=2∶1时,溶液的pH=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是中学化学中常用于混合物的分离和提纯的装置。
A  B
B  C
C  D
D 
利用以上装置,可以按以下实验方案从海洋动物柄海鞘中提取具有抗肿瘤活性的天然产物。(已知甲苯和甲醇均为有机溶剂,有机物大多能互溶)

(1)装置A中仪器①的作用是_____,流程中使用装置A的是操作___(填“a”、“b”、“c”或“d”,下同)。
(2)流程中使用装置B的是操作____,在该操作中,震荡仪器时,为了避免因液体挥发而导致内部气压过大,还应进行的具体操作是______(填写具体的操作方法)。
(3)流程中使用装置C的操作是___,若所得沉淀不溶于水且需要洗涤,则洗涤的具体操作是_____。
(4)流程中使用装置D的操作是_____。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com