
【题目】1934年,居里夫妇![]() 粒子(4He)轰击27Al得到一种自然界中不存在的磷元素的一种核素(
粒子(4He)轰击27Al得到一种自然界中不存在的磷元素的一种核素(![]() ):
):![]() +
+![]()
![]()
![]() +
+![]() ,开创了人造核素的先河。
,开创了人造核素的先河。
(1)下列有关说法正确的有______(填序号)。
A. ![]() 的质子数是27 B.
的质子数是27 B. ![]() 是一种电中性粒子
是一种电中性粒子
C. ![]() 和
和![]() 互为同位素 D. P元素的相对原子质量为30
互为同位素 D. P元素的相对原子质量为30
(2)元素的化学性质主要取决于______(填序号)。
A. 原子最外层电子数 B. 原子核内中子数
C. 原子核内质子数 D. 原子质量数
(3)不同种元素的本质区别是______(填序号)。
A. 原子的质子数不同 B. 原子的中子教不同
C. 原子的最外层电子数不同 D. 原子的质量数不同
【答案】BC A A
【解析】
(1)根据微粒符号表示中各个角标的含义,及同位素的概念和质量数与元素相对原子质量的关系、元素相对原子质量与同位素原子质量数关系分析;
(2)根据物质在发生化学反应时通常是原子的最外层电子发生变化分析;
(3)根据元素的含义分析判断。
(1)A. ![]() 的质子数是13,质量数是27,A错误;
的质子数是13,质量数是27,A错误;
B. ![]() 表示质子数是0,中子数是1的微粒,即表示中子,中子是一种电中性粒子,B正确;
表示质子数是0,中子数是1的微粒,即表示中子,中子是一种电中性粒子,B正确;
C. ![]() 和
和![]() 的质子数都是2,中子数分别是2、1,可见两种微粒质子数相同,中子数不同,因此二者互为同位素,C正确;
的质子数都是2,中子数分别是2、1,可见两种微粒质子数相同,中子数不同,因此二者互为同位素,C正确;
D. ![]() 的质量数是30,但P元素有几种同位素原子,各种同位素原子的原子个数比未知,因此不能确定P元素的相对原子质量,D错误;
的质量数是30,但P元素有几种同位素原子,各种同位素原子的原子个数比未知,因此不能确定P元素的相对原子质量,D错误;
故合理选项是BC;
(2)物质在发生化学反应时,原子核不变,内层电子也不变,变化的通常是原子的最外层电子,所以元素的化学性质主要取决于原子核外最外层电子数,故合理选项是A;
(3)同种元素的原子,质子数相同;不同元素的原子,质子数不同,可见判断元素是否属于不同种元素,本质区别是看原子核内质子数的多少,通常把具有相同的核电荷数即质子数的同一类原子总称为元素,故合理选项是A。


科目:高中化学 来源: 题型:
【题目】[化学——选修5:有机化学基础]化合物M是一种香料,A与D是常见的有机化工原料,按下列路线合成化合物M: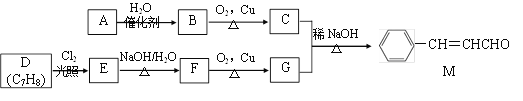
已知以下信息:
①A的相对分子质量为28
回答下列问题:
(1)A的名称是___________,D的结构简式是___________。
(2)A生成B的反应类型为________,C中官能团名称为___________。
(3)E生成F的的化学方程式为___________。
(4)下列关于G的说法正确的是___________。(填标号)
a.属于芳香烃
b.可与FeCl3溶液反应显紫色
c.可与新制的Cu(OH)2共热生成红色沉淀
d.G分子中最多有14个原子共平面
(5)化合物M的同系物N比M的相对分子质量大14,N的同分异构体中同时满足下列条件的共有________种(不考虑立体异构)。
①与化合物M含有相同的官能团;②苯环上有两个取代基
(6)参照上述合成路线,化合物X与Y以物质的量之比2:1反应可得到化合物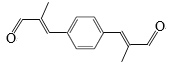 ,X的结构简式为________,Y的结构简式为________。
,X的结构简式为________,Y的结构简式为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了研究化学反应A+B=C+D的能量变化情况,某同学设计了如图所示装置。当向盛有A的试管中滴加试剂B时,看到U形管中甲处液面下降乙处液面上升。
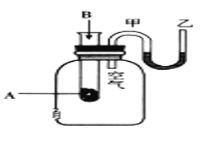
试回答下列问题:
(1)该反应为_______反应(填“放热”或“吸热”)。
(2)A和B的总能量比C和D的总能量_______(填“高”或“低”)。
(3)反应物化学键断裂吸收的能量_______(填“高”或“低”)于生成物化学键形成放出的能量。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某元素的一个原子形成的离子可表示为![]() n-,下列说法正确的是( )
n-,下列说法正确的是( )
A.![]() n-中含有的中子数为a+b
n-中含有的中子数为a+b
B.![]() n-中含有的电子数为a-n
n-中含有的电子数为a-n
C.X原子的质量数为a+b+n
D.一个X原子的质量约为![]() g
g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】观察下列A、B、C、D、E五种粒子(原子或离子)的结构示意图,回答有关问题:
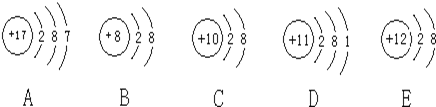
(1)属于离子结构示意图的是______、______(填编号)。
(2)性质最稳定的原子是(填写编号,在本小题中下同)______,最容易失去电子的原子是______,最容易得到电子的原子是______。
(3)A、D两种元素形成的化合物在水溶液中的电离方程式______。
(4)在核电荷数1-18的元素内,列举两个与B核外电子层排布相同的离子,写出离子的符号______、______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ、研究性学习小组进行SO2的制备及性质探究实验,装置如图(a为活塞,加热及固定装置已略去)。

(1)连接仪器、___、加药品后,打开 a,然后滴入浓硫酸,加热;
(2)铜与浓硫酸反应制备 SO2的化学方程式是___;
(3)品红溶液中的实验现象是___;
(4)从高锰酸钾溶液中观察到的现象说明 SO2具有___性。
Ⅱ、上述实验中 NaOH 溶液用于吸收剩余的 SO2 生成 Na2SO3,Na2SO3是抗氧剂。向烧碱和Na2SO3混合溶液中加入少许溴水,振荡后溶液变为无色。
(1)写出在碱性溶液中Br2氧化Na2SO3的离子方程式___
(2)反应后的溶液含有SO32-、SO42-、Br-、OH-等阴离子,请填写鉴定其中SO42-和Br-的实验报告。___
限选试剂:2mol·L-1HCl;1mol·L-1H2SO4;lmol·L-1BaCl2;lmol·L-1Ba(NO3)2;0.1mol·L-1AgNO3;CCl4;新制氯水。
编号 | 实验操作 | 预期现象和结论 |
步骤① | 取少量待测液加入试管中,加入过量的2mol·L-1盐酸,再滴加 | 有 生成,证明待测液中SO42- |
步骤② | 取出步骤①中适量上层清液于试管中,加入适量氯水,再加入 ,振荡,静置。 | 下层液体呈 ,证明待测液中含Br-。 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苹果酸的结构简式为HOOC![]() CH2—COOH,下列说法正确的是
CH2—COOH,下列说法正确的是
A. 苹果酸中能发生酯化反应的官能团有2种
B. 1mol苹果酸可与3mol NaOH发生中和反应
C. 1mol苹果酸与足量金属Na反应生成生成1mol H2
D. HOOC—CH2—CH(OH)—COOH与苹果酸互为同分异构体
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于丙烯(CH3—CH=CH2)的说法正确的是( )
A.丙烯分子中3个碳原子都是sp3杂化
B.丙烯分子有7个σ键,1个π键
C.丙烯分子存在非极性键
D.丙烯分子中3个碳原子在同一直线上
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下![]() 与
与![]() 发生反应:
发生反应:![]() ,则下列关于元素M的叙述正确的是
,则下列关于元素M的叙述正确的是
A.M位于元素周期表中第VA族
B.M的氢化物的水溶液显酸性
C.![]() 中M元素只能被还原
中M元素只能被还原
D.![]() 在常温常压下一定是气体
在常温常压下一定是气体
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com