
【题目】标准状况下一定体积的HCl气体,将其溶于500mL的稀硫酸溶液中,假设溶液的体积不变化,向混合溶液中加入0.60mol/L的NaOH溶液50mL恰好呈中性。继续向呈中性的溶液中加入过量的氯化钡溶液,所的沉淀的质量为2.33g。
(1)生成沉淀的离子反应方程式:_______________________________。
(2)原硫酸溶液的浓度为:______________________________________。
(3)标准状况下HCl气体的体积为多少毫升?(写出计算过程)__________。
【答案】Ba2++SO42-=BaSO4↓ 0.02mol/L 224mL
【解析】
(1)硫酸与NaOH发生酸碱中和反应,产生硫酸钠和水,HCl溶于水形成盐酸,盐酸与氢氧化钠发生酸碱中和反应,产生氯化钠和水,向反应后的溶液中加入BaCl2溶液,发生沉淀反应:Na2SO4+BaCl2=BaSO4↓+2NaCl,其离子方程式是:Ba2++SO42-=BaSO4↓;
(2)根据S元素守恒,可知n(H2SO4)=n(BaSO4)=![]() ,由于原硫酸溶液体积是500mL,所以硫酸溶液的浓度是c(H2SO4)=
,由于原硫酸溶液体积是500mL,所以硫酸溶液的浓度是c(H2SO4)=![]() =0.02mol/L;
=0.02mol/L;
(3)结合酸碱中和反应的实质H++OH-=H2O可知n(HCl)+2n(H2SO4)=n(NaOH),n(NaOH)=cV=0.60mol/L×0.050ml=0.03mol,则n(HCl)= n(NaOH)- 2n(H2SO4)=0.03mol-2×0.01mol=0.01mol,所以V(HCl)=nVm=0.01mol×22.4L/mol=0.224L=224mL。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案科目:高中化学 来源: 题型:
【题目】现有下列十种物质:①0.1mol/L硫酸②小苏打③纯碱④二氧化碳⑤葡萄糖⑥0.1mol/LNaOH溶液⑦SiO2 ⑧氨水⑨Al2O3⑩硫酸铁溶液
(1)上述十种物质中属于非电解质的有_____(填序号)。
(2)有两种物质在水溶液中可发生反应,离子方程式为:H++OH-=H2O,这两种物质的序号是______(填序号)。
(3)既能跟盐酸反应又能跟NaOH溶液反应的是_____(填序号)。
(4)标准状况下,_____L④中含有0.4mol氧原子。
(5)⑥与⑦溶液反应的离子方程式为__________。
(6)硅是信息技术的关键材料,写出工业上用⑦制备粗硅的化学反应方程式_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】苯丙醇异丁酸酯(![]() )是一种合成香料,其中一种合成路线如图:
)是一种合成香料,其中一种合成路线如图:

已知:R-CH=CH2![]() R-CH2CH2OH。请回答下列问题:
R-CH2CH2OH。请回答下列问题:
(1)A的化学名称是______________,B中含有的官能团名称是________________。
(2)在一定条件下,A与水反应也可以生成B或另外一种生成物,该反应的反应类型为___________,“另外一种生成物”的结构简式为_____________________________。
(3)C可被新制的Cu(OH)2悬浊液氧化,也可以被其他氧化剂所氧化。写出C与银氨溶液反应的化学方程式:_____________________________。
(4)D的核磁共振氢谱显示为6组峰,且峰面积之比为1∶1∶1∶1∶2∶2,则D的结构简式为_______________;D的同分异构体有多种,其中苯环上有两个不含环状的取代基,并能与Na反应的同分异构体有_______种(不含立体异构)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列化学反应中,属于氧化还原反应的是
A. Na2CO3+2HCl=2NaCl+H2O+CO2↑ B. 2 NaHCO3 ![]() Na2CO3 + H2O + CO2↑
Na2CO3 + H2O + CO2↑
C. Na2O+H2O=2NaOH D. Zn+H2SO4=ZnSO4 +H2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某学生欲配制3.0mol/L的H2SO4溶液100mL,实验室有标准浓度为90%、密度为1.80g/mL的硫酸溶液。请回答下列问题:
(1)实验所用90%的硫酸的物质的量浓度为________mol/L(保留1位小数)。
(2)配制该硫酸溶液应选用容量瓶的规格为_______mL。
(3)配制时,该同学的操作顺序如下,请将操作步骤A、C补充完整。
A.用量简准确量取所需的90%的硫酸溶液_______mL,沿玻璃棒倒入少量蒸馏水中,并用玻璃棒搅拌,使其混合均匀;
B.将混合均匀的硫酸溶液沿玻璃棒注入所选的容量瓶中;
C.______________________________________________;
D.振荡,继续向容量瓶中加水,直到液面接近刻度线1~2cm处;
E.改用胶头滴管加水,使溶液的凹液面恰好与刻度线相切;
F.将容量瓶盖紧,振荡,据匀。
(4)如果省略操作C,对所配溶液浓度有何影响?______(填“偏大”、“偏小”或无影响”)
(5)进行操作B前还需注意__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸晶体的组成可表示为H2C2O4·xH2O,某研究性学习小组用下图装置进行“草酸晶体受热分解的部分产物的验证”的实验。请回答下列问题。

【资料查阅】
①草酸晶体在101 ℃时开始熔化,150 ℃时开始升华,175 ℃时开始分解;
②草酸钙和草酸氢钙均为白色不溶物。
(1)按照如图所示的装置,通过实验检验草酸晶体的部分分解产物,装置B中可观察到有气泡冒出且澄清石灰水变浑浊,由此甲同学判断草酸晶体分解的产物中有CO2。但立即遭到乙同学反对,其反对的理由可能是______________________________________。
(2)丙同学认为草酸晶体分解的产物中含有CO,为进行验证,X应选用________(填化学式)浓溶液,装置D的作用是____________________。
(3)实验过程中涉及如下操作:①点燃装置A处的酒精灯;②熄灭装置A处的酒精灯;③点燃装置E处的酒精灯;④熄灭装置E处的酒精灯。这4步操作由先到后的顺序为____________(填序号)。点燃E处酒精灯前必须要进行的操作是______________。
(4)实验过程中发现装置E中黑色粉末变红色,装置F中有黑色固体生成,经检测装置F中的固体为金属单质,则装置F中发生反应的化学方程式为________________________________________________________________________。
(5)丁同学用滴定法测定草酸晶体中结晶水的含量,进行了下列操作:
步骤一:用分析天平称取3.15 g纯净的该草酸晶体,配制成250 mL溶液。
步骤二:用移液管移取25.00 mL待测草酸溶液于锥形瓶中,并加入适量硫酸酸化。
步骤三:取0.100 mol·L-1标准酸性KMnO4溶液,进行滴定,三次结果如下表所示:
第一次 | 第二次 | 第三次 | |
待测溶液体积(mL) | 25.00 | 25.00 | 25.00 |
标准溶液体积(mL) | 9.99 | 10.01 | 10.00 |
已知滴定反应的离子方程式为:MnO![]() +H2C2O4+H+―→Mn2++CO2↑+H2O(未配平)。
+H2C2O4+H+―→Mn2++CO2↑+H2O(未配平)。
①配制草酸溶液的操作步骤依次是:将晶体置于烧杯中,加水溶解,将溶液转移入________,洗涤,定容,摇匀。
②通过计算确定x=________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中正确的是
A. 标准状况下,22.4 L水中所含的分子数约为6.02×1023个
B. 1 mol Cl2中含有的原子数为NA
C. 标准状况下,a L氧气和氮气的混合物含有的分子数约为![]() ×6.02×1023个
×6.02×1023个
D. 从1 L0.5 mol·L-1NaCl溶液中取出100 mL,剩余溶液中NaCl物质的量浓度为0.45 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
(1)营养平衡、合理用药是保证人体健康和生活质量的重要途径。
①下列物质中,不能为人体提供能量的是_______(填字母)。
a.蛋白质 b.纤维素 c.油脂
②当出现外伤感染时,医生会建议使用以下常用药物中的______(填字母)。
a.复方氢氧化铝片 b.阿司匹林 c.盘尼西林
③食品添加剂亚硝酸钠的外观像食盐并有咸味,它不但是防腐剂,还具有抗氧化作用。亚硝酸钠属于____(填字母)。但亚硝酸钠会与肉类的蛋白质反应,生成一种致癌化合物——亚硝胺。所以不可长期或大量进食腌制类肉类。
a.调味剂 b.着色剂 c.发色剂
(2)积极保护生态环境可实现人与自然的和谐共处。
①向煤中加入石灰石,可有效减少_______的排放。
②向含有Hg2+的废水中加入____,可有效除去该重金属离子。
③下列物质能给水体杀菌消毒,又能使水体净化的是______(填字母)。
A.Na2FeO4(aq) B.KAl(SO4)2·12H2O C.Ca(ClO)2(aq) D.NaClO(aq)
④用二氧化碳生产化工产品,有利于二氧化碳的大量回收。某工业生产中利用CO2和C2H4及水蒸气在催化剂条件下合成乙酸(原子利用率100%),该反应的化学方程式为____________。
(3)材料是人类生存和发展的物质基础。
①汽车行驶在“超级高速公路”上行驶,自动收费系统会通过车载芯片对车辆进行自动收费。制取芯片的主要原料是_____ (填字母)。
a.硅 b.石墨 c.二氧化硅
②在下列材料中,属于复合材料的是____ (填字母)。
a.钢化玻璃 b.丁苯橡胶 c.氮化硅陶瓷 d.钢筋混凝土
③基础建设需要大量的水泥,水泥属于______(填字母),水泥的保质期通常只有三个月,不能长期保存的原因是_______________。
a.金属材料 b.无机非金属材料 c.有机高分子材料
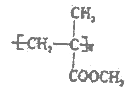
④有机玻璃是由有机物X加聚制得的热塑性塑料,为透明如玻璃状的无色固体,可用以制造航空窗玻璃、仪表盘、外科照明灯、装饰器和生活用品等,其结构简式如图所示。请写出X 的结构简式__________。
⑤太阳能电池需要用到高纯硅为原料。高温下焦炭和石英反应可以制得粗硅,该反应的方程式为__________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组的同学为了制备氯气并探究其性质,回答下列问题。
Ⅰ.写出实验室制取氯气的离子方程式:_______________________________
Ⅱ.甲同学设计如图所示装置研究氯气能否与水发生反应.气体a是含有少量空气和水蒸气的氯气.请回答下列问题:

(1)浓硫酸的作用是___________________。
(2)证明氯气和水反应的实验现象为__________。
(3)ICl的性质与Cl2类似,写出ICl与水反应的化学方程式是______________________。
(4)若将氯气通入石灰乳制取漂白粉,反应的化学方程式是______________________。漂白粉溶于水后,遇到空气中的CO2,即产生漂白、杀菌作用,反应的化学方程式是_________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com