
【题目】液氨是富氢物质,是氢能的理想载体。下列说法不正确的是( )
A. NH3分子中氮原子的杂化方式为sp3杂化
B. [Cu(NH3)4]2+中,NH3分子是配体
C. NH![]() 与PH
与PH![]() 、CH4、BH
、CH4、BH![]() 互为等电子体
互为等电子体
D. 相同压强下,NH3的沸点比PH3的沸点低
【答案】D
【解析】
A.氨气分子中氮原子价层电子对个数=3+1/2×(5-3×1)=4,所以N原子采用sp3杂化,故A正确;
B.在[Cu(NH3)4]2+离子中,Cu2+提供空轨道,N原子提供孤电子对,所以N原子是配位原子,NH3分子是配体,故B正确;
C.等电子体为原子数相等和价电子数相等的原子团,NH4+与PH4+、CH4、BH-4均含有5个原子,且价电子均为8,为等电子体,故C正确;
D.NH3和PH3结构相似且都属于分子晶体,分子晶体的熔沸点随着其相对分子质量的增大而增大,但氢键能增大物质的沸点,氨气存在分子间氢键,所以相同压强时,NH3和PH3比较,氨气沸点高,故D错误。
故选D。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】新型锌碘液流电池具有能量密度高、循环寿命长等优势,其工作原理如图所示。下列说法错误的是

A. 放电时电流从石墨电极流向锌电极
B. 充电时阳极反应式为:3I--2e-=I3-
C. 若将阳离子交换膜换成阴离子交换膜,放电时正负极也随之改变
D. 放电时左侧电解质储罐中的离子总浓度增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.利用下图装置测定中和热的实验步骤如下:
①用量筒量取50 mL 0.25 mol/L硫酸倒入小烧杯中,测出硫酸温度;
②用另一量筒量取50 mL 0.55 mol/L NaOH溶液,并用另一温度计测出其温度;③将NaOH溶液倒入小烧杯中,设法使之混合均匀,测出混合液最高温度。
回答下列问题:
(1)写出稀硫酸和稀氢氧化钠溶液反应表示中和热的热化学方程式(中和热数值为57.3 kJ/mol):_______________________________________________________________
(2)学生甲用稀硫酸与稀烧碱溶液测定中和热装置如图。

①实验时所需要的玻璃仪器除烧杯、量筒外还需要:_________。
②该装置中有一处错误是:______________________,
(3)用相同浓度和体积的氨水(NH3· H2O)代替NaOH溶液进行上述实验,测得的中和热的数值会________(填“偏大”、“偏小”或“无影响”)。
Ⅱ.(1)已知充分燃烧一定质量的丁烷(C4H10)气体时生成1mol二氧化碳气体和液态水,并放出热量bkJ,则表示丁烷燃烧热的热化学方程式为______________________
(2)已知下列热化学方程式:
C(s,石墨)+O2(g)═CO2(g)△H=-393.5kJmol-1
2H2(g)+O2(g)═2H2O(l)△H=-571.6kJmol-1
2C2H2(g)+5O2(g)═4CO2(g)+2H2O(l)△H=-2599kJmol-1
请写出C(s,石墨)和H2(g)生成1mol C2H2(g)的热化学方程式____________________
(3)已知几种共价键的键能数据如下表:
共价键 | N≡N | H—H | N—H |
键能 (kJ/mol) | 946 | 436 | 390.8 |
写出合成氨反应的热化学方程式: ____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组的同学设计实验制备CuBr(白色结晶性粉末,微溶于水,不溶于乙醇等有机溶剂),实验装置(夹持、加热仪器略)如图所示。
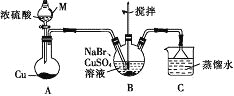
(1)仪器M的名称是________。
(2)若将M中的浓硫酸换成70%的H2SO4,则圆底烧瓶中的固体试剂为______(填化学式)。
(3)B中发生反应的化学方程式为_______,能说明B中反应已完成的依据是_____。若B中Cu2+仍未完全被还原,适宜加入的试剂是_______(填标号)。
a.液溴 b.Na2SO4 c.铁粉 d.Na2S2O3
(4)下列关于过滤的叙述不正确的是_______ (填标号)。
a.漏斗末端颈尖可以不紧靠烧杯壁
b.将滤纸润湿,使其紧贴漏斗内壁
c.滤纸边缘可以高出漏斗口
d.用玻璃棒在漏斗中轻轻搅动以加快过滤速率
(5)洗涤时,先用装置C中的吸收液清洗,其目的是_______,再依次用溶解SO2的乙醇、乙醚洗涤的目的是________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于晶体的说法一定正确的是( )
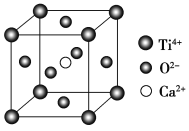
(CaTiO3的晶体结构模型(Ca2+、O2-、Ti4+分别位于立方体的体心、面心和顶点)
A. 分子晶体中都存在共价键
B. CaTiO3晶体中每个Ti4+与12个O2-相紧邻
C. SiO2晶体中每个硅原子与两个氧原子以共价键相结合
D. 金属晶体的熔点都比分子晶体的熔点高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯和钾与不同价态的铜可生成两种化合物,这两种化合物都可用于催化乙炔聚合,其阴离子均为无限长链结构(如图),已知其中一种化合物的化学式为KCuCl3,下列有关说法中错误的是( )
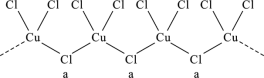
A. a位置上Cl原子的杂化轨道类型为sp3
B. 另一种的化学式为K2CuCl3
C. 铜元素在周期表中位于d区
D. 该物质中存在配位键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用图装置制取氯气,并进行相关性质的实验。
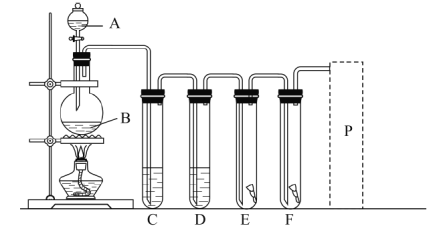
(1)A、B两仪器的名称:A________、B________。
(2)写出实验室用此装置制取氯气的化学方程式________。
(3)为了得到纯净干燥的氯气,写出装置C、D中应该加入的药品的名称:C____、D_________。
(4)E中放入红色干布条,F中放入红色湿布条。可观察到的现象是________,写出发生反应的化学方程式________。
(5)P处为尾气处理装置,画出装置图,标出所用的药品。________

(6)NaClO是“84”消毒液的有效成分。请回答下列问题。
①NaClO中Cl元素的化合价是______。
②用氢氧化钠溶液和氯气反应制备“84”消毒液,反应的离子方程式是_______。
③若将“84”消毒液与洁厕灵(主要成分是盐酸)混合使用,则会产生黄绿色的有毒气体,其反应的离子方程式是_________。
(7)FeCl3在现代工业中应用广泛,某化学研究性学习小组模拟工业生产流程制备无水FeCl3。经查阅资料得知:无水FeCl3在空气中易潮解,加热易升华,无水CaCl2是常用的干燥剂。他们设计了制备无水FeCl3的实验方案,装置示意如图(加热、加持及尾气处理装置略去)及操作步骤如下:
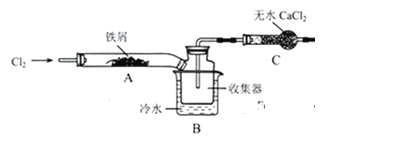
①检查装置气密性
②通入干燥的氯气,赶尽装置内的空气
③用酒精灯在铁屑下方加热至反应完成
④……
⑤体系冷却后,停止通入氯气,并用干燥的的氮气赶尽氯气,将收集器密封。
请回答下列问题:
①装置A中发生反应的化学方程式_____________。
②步骤③加热后,生成的烟状FeCl3大部分进入收集器,少量沉积在反应管A的右端。要使沉积的FeCl3进入收集器,第④步操作是________。
③操作步骤中,为防止潮解所采取的措施有(填步骤序号)________。
④装置B中的冷却水作用为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学实验是进行科学探究的重要途径,观察下图的实验装置,回答下面的问题。
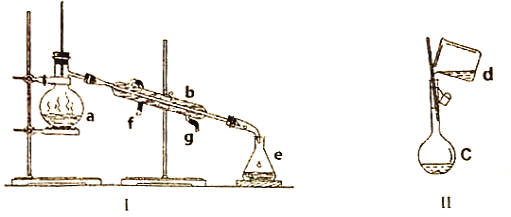
(1)写出下列仪器的名称:a:________________,b:________________,c:_________________。
(2)仪器c在使用前必须进行的操作是____________________________________________________。
(3)若用装置I制取少量蒸馏水,实验时a中除加入自来水外,还需加入_________________________,其作用是________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示中,A、B是金属单质,E、K是非金属单质,其它为化合物,F、G、H、I、J 焰色反应均为黄色,在这些物质中只有C、K是气体,其中K是黄绿色气体,反应⑧⑨是工业由H制I的重要反应。
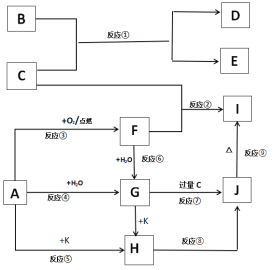
填写下列空白:
(1)写出化学式:B___,F___。
(2)写出反应①的化学反应方程式:____。
(3)写出反应⑦离子反应方程式:___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com