
����Ŀ��ij��ȤС���ͬѧ���ʵ���Ʊ�CuBr(��ɫ�ᾧ�Է�ĩ������ˮ���������Ҵ����л��ܼ�)��ʵ��װ��(�г֡�����������)��ͼ��ʾ��
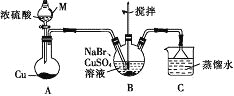
(1)����M��������________��
(2)����M�е�Ũ���ỻ��70%��H2SO4����Բ����ƿ�еĹ����Լ�Ϊ______(�ѧʽ)��
(3)B�з�����Ӧ�Ļ�ѧ����ʽΪ_______����˵��B�з�Ӧ����ɵ�������_____����B��Cu2+��δ��ȫ����ԭ�����˼�����Լ���_______(����)��
a.Һ�� b.Na2SO4 c.���� d.Na2S2O3
(4)���й��ڹ��˵���������ȷ����_______ (����)��
a.©��ĩ�˾�����Բ������ձ���
b.����ֽ��ʪ��ʹ�����©���ڱ�
c.��ֽ��Ե���Ը߳�©����
d.�ò�������©������������Լӿ��������
(5)ϴ��ʱ������װ��C�е�����Һ��ϴ����Ŀ����_______�����������ܽ�SO2���Ҵ�������ϴ�ӵ�Ŀ����________��
���𰸡���Һ©�� Na2SO3(��K2SO3��NaHSO3��KHSO3��) 2CuSO4+2NaBr+SO2+2H2O=2CuBr��+Na2SO4+2H2SO4 ��Һ��ɫ��ȥ d acd ��ֹCuBr������ ���Ҵ���ȥ��������ˮ�����ø��ӷ������ѳ�ȥ�Ҵ���ʹ����ٸ���
��������
(1)���������ṹ�ж����������ƣ�
(2)���ݸ��ֽⷴӦ�Ĺ���ѡ���Լ���
(3)��B��NaBr��SO2��CuSO4��H2O�ᷢ��������ԭ��Ӧ����CuBr���������õ����غ㡢ԭ���غ㣬��д��Ӧ�Ļ�ѧ����ʽ������Cu2+��ˮ��Һ����ɫ����ϸ÷�Ӧ���ص��жϷ�Ӧ��ȫ����������������ʣ�
(4)���ݹ��˲�����Ŀ�ġ�������ʹ�÷������
(5)CuBr���ױ�����������SO2��ˮ��Һ���л�ԭ�Է��������H2O���������Ҵ��У����Ҵ������Ѿ����ӷ������ʷ�����
(1)����װ��ͼ������M�Ľṹ��֪�������������Ƿ�Һ©����
(2)���ݸ��ֽⷴӦ�Ĺ��ɿ���70%��H2SO4��Na2SO3��K2SO3��NaHSO3��KHSO3�ȷ�Ӧ��ȡSO2���壬��Ӧ����ʽΪH2SO4+Na2SO3=Na2SO4+H2O+SO2����
(3)��B��BaBr��SO2��CuSO4��H2O�ᷢ��������ԭ��Ӧ����CuBr���������õ����غ㡢ԭ���غ㣬�ɵø÷�Ӧ�Ļ�ѧ����ʽΪ��2CuSO4+2NaBr+SO2+2H2O=2CuBr��+Na2SO4+2H2SO4��
Cu2+��ˮ��Һ����ɫ������Ӧ��ȫ������Һ�в��ٺ���Cu2+����Һ����ɫ��ȥ������CuSO4��ǿ�������Σ�����Һ��Cu2+ˮ��ʹ��Һ�����ԣ�H+��Na2S2O3��Ӧ����SO2���壬�Դ�ʹ��Ӧ�Ľ��У������B��Cu2+��δ��ȫ����ԭ�����˼�����Լ���Na2S2O3���ʺ���ѡ����d��
(4)a.©��ĩ�˾�������ձ��ڣ��Ϳ���ʹ���˵õ�����Һ���ձ��ڱڲ��Ͻ��뵽�ձ��У�a����
b.����ֽ��ʪ��ʹ�����©���ڱڣ��Ϳ���ʹ������ַ��룬b��ȷ��
c.Ϊ��ʹ�����ԵĹ�����Һ�����ʷ��룬��ֽ��ԵҪ����©���ڱ�Ե��c����
d.�ò�����������ʹ�������뵽�������У���©���в����ò����������������ʹ��ֽ���𣬵��²��ܹ��ˣ����ܷ������d����
�ʺ���ѡ����acd��
(5)SO2�Ǵ�����Ⱦ�Ϊ��ֹ����Ⱦ������������ˮ����SO2���õ�H2SO3��Һ�������ʾ��л�ԭ�ԣ���H2SO3��Һϴ�ӣ��Ϳ��Ա���CuBr�������е�����������Ȼ���������ܽ�SO2���Ҵ�������ϴ�ӵ�Ŀ�������Ҵ���ȥ��������ˮ�����ø��ӷ������ѳ�ȥ�Ҵ���ʹ����ٸ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��![]() �������л����ܹ��ϳ�
�������л����ܹ��ϳ�![]() ������ǣ� ��
������ǣ� ��
��1��3-����ϩ ��2-��-l,3-����ϩ ��1,3-���ϩ ��2��3-����-l,3������ϩ
��2��3-����-l,3�����ϩ ����Ȳ ����Ȳ ��2-��Ȳ
A. �١������ܡ��� B. �ݡ������ۡ���
C. �١������ڡ��� D. �ڡ������ܡ���
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��
(1)48g������48g����(O3)������������ԭ����_______ (������ͬ��������ͬ����������ͬ��ͬѹ�µ��������________��0.2 mol NH3������________��CH4���еĵ�������ͬ����_______g H2O���е���ԭ������ͬ�����״����____ L CO���е�ԭ������ȡ�
(2)483g Na2SO4��10H2O��������Na2SO4��10H2O�����ʵ�����_______�� Na2SO4��10H2O��Ħ��������________������Na+�����ʵ�����________����0.4 mol Al3����Al2(SO4)3��������SO42-�����ʵ�����________��
(3)ʵ���ҳ��õ�Ũ�����ܶ�Ϊ1.17 g��mL-1����������Ϊ36.5 %��
�ٴ�Ũ��������ʵ���Ũ��Ϊ__________________��
��ȡ��Ũ����50mL��������ˮϡ��Ϊ200mL��ϡ�ͺ���������ʵ���Ũ��Ϊ_____��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧ����ʽ�У�������ȷ���ﷴӦ��ɫ�仯��ԭ�����
A. ͭ���ÿ����б��������ɫ���壺2Cu��O2��CO2��H2O�TCu2(OH)2CO3
B. ij�ֻ�������������N2O4���ݳ���������ɫ���壺N2O4![]() 2NO2
2NO2
C. FeSO4��7H2O�ڿ����о��ñ�ƣ�2FeSO4��7H2O![]() Fe2O3��SO2����SO3����14H2O
Fe2O3��SO2����SO3����14H2O
D. SO2ͨ��KMnO4��Һ�У���Һ��ɫ����ȥ��5SO2��2KMnO4��2H2O�TK2SO4��2MnSO4ʮ2H2SO4
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��I.��CO2ת���ɼ״�ȼ���Ǽ��š�������һ�ֿ�ѧ������
��֪��2H2(g)+O2(g) =2H2O(g)����H=��483.6kJ��mol-1 ��
2CO2(g)+4H2O(g) ![]() 2CH3OH(g)��3O2(g)����H����1352.8kJ��mol-1��
2CH3OH(g)��3O2(g)����H����1352.8kJ��mol-1��
����CO2��H2��Ӧ�Ʊ� CH3OH(g)��ͬʱ����ˮ�������Ȼ�ѧ����ʽΪ___________________
II.���ݻ�Ϊ2L���ܱ������У��������·�Ӧ��A(g)+2B(g)![]() C(g)+D(g)���������1.0molA��2.2molB���ڲ�ͬ�¶��£�D�����ʵ���n(D)��ʱ��t�Ĺ�ϵ��ͼ��
C(g)+D(g)���������1.0molA��2.2molB���ڲ�ͬ�¶��£�D�����ʵ���n(D)��ʱ��t�Ĺ�ϵ��ͼ��

�Իش��������⣺
(1)800��ʱ,0��5min�ڣ���B��ʾ��ƽ����Ӧ����Ϊ____________��
(2)���жϸ÷�Ӧ�ﵽ��ѧƽ��״̬��������_______________��
a��������ѹǿ���� b�����������c(A)����
c��2v��(B)=v��(D) d��c(A)=c(C)
(3)���������1.0molA��2.2molB������ͼ�����ݼ���800��ʱ��ƽ�ⳣ��K=________���÷�ӦΪ_______��Ӧ(�����Ȼ����),�ж�������______________________________��
(4)800��ʱ��ijʱ�̲����ϵ�и����ʵ������£�n(A)=0.9mol��n(B)=2.0mol��n(C)=0.9mol��n(D)=0.9mol�����ʱ�÷�Ӧ________����(����������Ӧ�����������淴Ӧ��������������ƽ��״̬��)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ȤС����Ī����[��ѧʽΪ(NH4)xFe(SO4)2��6H2O��FeΪ��2�ۣ�]�ⶨKMnO4��Һ�����ʵ���Ũ�ȵĹ������£�
�ٳ�ȡ19.6gĪ�������100mL��Һ��
����ȡ10.00mLKMnO4��Һ�������м���������H2SO4�����ữ�����ữ�����Һ����εμ�Ī������Һ����Ӧ��ȫʱ����Ī������Һ�����20.00mL����������Ӧ�����ӷ���ʽ���£�4H����5Fe2����MnO4-��5Fe3����Mn2����4H2O��ش��������⣺
��1��(NH4)xFe(SO4)2��6H2O��x��___��c��Fe2������___��
��2���ڢٲ�ʵ��������IJ�����������Ͳ���ձ�����ͷ�ι����___��
�ù�����Ʒ����һ�����ʵ���Ũ�ȵ���Һ���辭���������ܽ⡢ת�ơ����ݲ���������ͼ��Ӧ�IJ����淶����___��
a������ b���ܽ�
b���ܽ� c��ת��
c��ת�� d������
d������![]()
��3������KMnO4��Һ�����ʵ���Ũ�ȣ�д��������̡�___
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Һ���Ǹ������ʣ������ܵ��������塣����˵������ȷ����(����)
A. NH3�����е�ԭ�ӵ��ӻ���ʽΪsp3�ӻ�
B. [Cu(NH3)4]2����NH3����������
C. NH![]() ��PH
��PH![]() ��CH4��BH
��CH4��BH![]() ��Ϊ�ȵ�����
��Ϊ�ȵ�����
D. ��ͬѹǿ�£�NH3�ķе��PH3�ķе��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
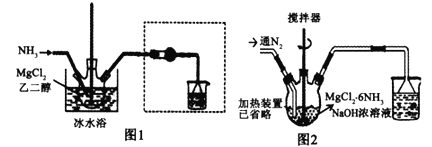
����Ŀ����֪MgCl2+6NH3![]() MgCl2��6NH3�÷�Ӧ���м��õĿ��������Ű����ԡ�ij��������ʵ����̽�������ԣ����а���(����)����ʵ��װ����ͼ1���Ű�����ʵ��װ����ͼ2��
MgCl2��6NH3�÷�Ӧ���м��õĿ��������Ű����ԡ�ij��������ʵ����̽�������ԣ����а���(����)����ʵ��װ����ͼ1���Ű�����ʵ��װ����ͼ2��
��֪��������ʵ����ʼ��±�
�������� | �������ܽ��� | �Ȼ�þ���ܽ��� | �����Ȼ�þ���ܽ��� |
ˮ | ���� | ���� | ���� |
�״����е�65��C�� | ���� | ���� | ���� |
�Ҷ������е�197��C�� | ���� | ���� | ���� |
��ش�
��1��ʵ���Ҳ��ù̹̼��ȵķ�ʽ�Ʊ�NH3���Ʊ���Ӧ�ķ���ʽΪ___________�������װ�õ�������___________���������̲��ñ�ˮԡ��ԭ�������_____(��ѡ�������ĸ)��
A����������Ϊ���ȷ�Ӧ���ٽ���Ӧ�������
B���ӿ췴Ӧ����
C����ֹ��������Һ�лӷ�����߰���������
D�����������Ȼ�þ���ܽ��
��2������MgCl2��Һ�Ʊ���ˮMgCl2����������Ϊ______________________��
��3�����зŰ�ʵ��ʱ��������ƿ����1.97 g MgCl2��6NH3���ռ��Ũ��Һ�����ȣ�������ͨ��N2��ͨ��N2Ŀ����___________��ͨ���۲��ձ�������ı仯�Ϳ��Լ��MgCl2��6NH3�ķŰ����̣���Ҫ�ж�ת�����Ƿ�ﵽ��90%�����ձ�����Һ������___________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������ϰ�������ˮƽ����ߣ���������Ѱ�����ռң��ڷ������ҵ�������ײʱ��������ȫ���һᷢ����Ӧ10NaN3+2KNO3![]() K2O+5Na2O+16N2�����йظ÷�Ӧ˵����ȷ���ǣ� ��
K2O+5Na2O+16N2�����йظ÷�Ӧ˵����ȷ���ǣ� ��
A.�������뻹ԭ�������ʵ���֮��Ϊ5��1B.N2������������Ҳ�ǻ�ԭ����
C.NaN3��������D.KNO3����������Ӧ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com