
【题目】工业上制备过碳酸钠(2Na2CO3·3H2O2)的一种流程如下:
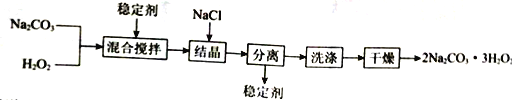
下列说法不正确的是
A. 可以用MnO2作稳定剂
B. “结晶”时,加入NaCl的主要作用是增大产品的产率
C. “分离”所用的主要玻璃仪器为烧杯、漏斗、玻璃棒
D. 2Na2CO3·3H2O2受热分解属于氧化还原反应
科目:高中化学 来源: 题型:
【题目】下列对能量转化的认识中,不正确的是
A.电解水生成氢气和氧气时,电能主要转化为化学能
B.白炽灯工作时,电能全部转化为光能
C.煤燃烧时,化学能主要转化为热能
D.风力发电时,风能主要转化为电能
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列对于“摩尔”的说法和理解正确的是( )
A. 摩尔是国际科学界建议采用的一种物理量
B. 摩尔可以把物质的宏观数量与微观粒子的数量联系起来
C. 国际上规定,0.012 kg碳原子所含有的碳原子数目为1 mol
D. 摩尔是物质的量的单位,简称摩,符号为mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫代硫酸钠(Na2S2O3),又名大苏打、海波。可用于鞣制皮革、由矿石中提取银、除去自来水中的氯气等。实验室可用以下两种力法制备少量硫代酸钠晶体(Na2S2O3 5H2O)。
方法一:将SO2通入Na2CO3和Na2S的混合溶液中充分反应而得。其流程为:
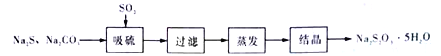
(1)SO2的制备
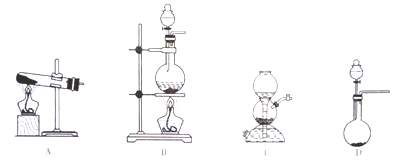
SO2的发生装置可以选择上图中的_______(填写选项的字母),反应的化学方程式为________________________________。
(2)吸硫装置如图所示。
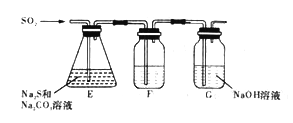
①装置F的作用是检验装置E中SO2的吸收效率,F中试剂是_____________。
②为保证Na2S和Na2CO3得到充分利用,两者的物质的量之比应为_________。
③该过程须控制SO2的通入量,SO2通入量过少或过多均不利Na2S2O3 5H2O的制备。其原因是_________________________。
方法二:将硫粉与Na2SO3溶液混合共热。先取15.1 g Na2SO3溶于80.0 mL水中,再取5.00 g硫粉,用少许乙醇润湿后(以便硫能被水浸润),加到上述溶液中。然后将上述溶液转移到仪器甲中,用小火加热至微沸.反应约为1 h后过滤,滤液在100℃经蒸发、浓缩、冷却至10℃后析出Na2S2O3·5H2O晶体。
(3)仪器甲最好是_______(填写选项的字目)。
A.圆底烧瓶 B.蒸发皿 C.试管 D.烧杯
(4)若加入的硫粉不用乙醇润湿,对反应的影响是_____(填写选项的字目)。
A.会降低反应速率 B.需要提高反应温度
C.将增大反应体系的pH值 D.会减少产量
(5)滤液中除Na2S2O3和可能未反应完全的Na2SO3外,还可能存在一种杂质。如果滤液中该杂质的含量不很低,其检测的方法是:________________________。
(6)已知:2 Na2S2O3+I2==2NaI+Na2S4O6。为测定所制得晶体的纯度,该小组以淀粉作指示剂,用0.010 mol·L-1的碘水进行多次取样滴定,测得Na2S2O3·5H2O的含量约为102%。若所用碘水及操作均无不当,产生该结果最可能的原因是______________(写出一个原因即可)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢镍电池放电时的总反应为MH+NiOOH==M+Ni(OH)2。以氢镍电池为电源,能将废水中的CN-转化为CO32-和N2,该装置如图所示。下列说法不正确的是

A. 电极a为正极
B. 负极反应式为MH+OH--e-==H2O+M
C. 每消耗1 mol CN-,理论上导线中通过3 mo1 e-
D. 阴极区溶液的PH增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乙烯和乙烷的混合气体共a mol,与b mol O2共存于一密闭容器中,点燃后充分反应,乙烯和乙烷全部消耗完,得到CO和CO2的混合气体和45 g H2O,试求:
(1)当a=1时,乙烯和乙烷的物质的量之比n(C2H4)∶n(C2H6)= 。
(2)当a=1,且反应后CO和CO2的混合气体的物质的量为反应前O2的![]() 时,b= ,得到的CO和CO2的物质的量之比n(CO)∶n(CO2)= 。
时,b= ,得到的CO和CO2的物质的量之比n(CO)∶n(CO2)= 。
(3)a的取值范围是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】W、X、Y、Z是周期表前36号元素中的四种常见元素,其原子序数依次增大。W、Y的氧化物是导致酸雨的主要物质,X的基态原子核外有7个原子轨道填充了电子,Z能形成红色(或砖红色)的Z2O和黑色的ZO两种氧化物。
(1)W位于元素周期表第________周期第________族。W的气态氢化物稳定性比H2O(g)________(填“强”或“弱”)。
(2)Y的基态原子价层电子排布式为________________,Y的第一电离能比X的________(填“大”或“小”)。
(3)Y的最高价氧化物对应水化物的浓溶液与Z的单质反应的化学方程式是
________________________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com