
����Ŀ��H2RO3��һ�ֶ�Ԫ�ᣬ��������1L1mol��L-1Na2RO3��Һ����RO2���壬��Һ��pH��RO2��������ʵ����ı仯��ͼ��ʾ������˵����ȷ����
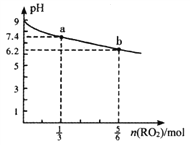
A. a����Һ��2c(Na+)=3c(RO32-)
B. ��b����Һ�м�ˮ��ʹ��Һ��pH��6.2���ߵ�7.4
C. �����£�NaHRO3��Һ��c(HRO3-)>c(RO32-)>c(H2RO3)
D. ������RO2����Һ������ʱ��c(Na+)=c(RO32-)+c(HRO3-)
���𰸡�C
��������a����Һ�к���H2RO31mol��H2RO3+H2O+RO2=2NaHRO3 ����a��ͨ��1/3 mol RO2����Һ������������2mol��RO32-Ϊ2/3 mol,��ʱa����Һ�ʼ��ԣ�˵��RO32-���ӷ�����ˮ�⣬��2c(Na+)>3c(RO32-)��A������b�㵼����Һ���Ե�������HRO3-�ĵ��룬�����Һ��ˮ�����ɵ�������Ũ����С��pH��ֻ�����ӽ�7�����ᳬ��7��B��������ͨ��5/6 molRO2ʱ����Һ������5/3mol NaHRO3 ��ʣ��Na2RO3Ϊ1/6 mol����ʱ��Һ��pH=6.2�����ԣ�˵��HRO3-�Ե���Ϊ�����ʳ����£�NaHRO3��Һ�У�c(HRO3-)>c(RO32-)>c(H2RO3)��C��ȷ��������RO2����Һ������ʱ�����ݵ���غ㣺c(H+)+c(Na+)=2c(RO32-)+c(HRO3-)+c(OH-)������c(H+)=c(OH-)������c(Na+)=2c(RO32-)+c(HRO3-)��D��������ȷѡ��C��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��H��N��Na��Al��Ti��Ԫ������Դ�����ϵ�����Ӧ�ù㷺���ش��������⣺
��һ���⻯���ƣ�NaAlH4����һ���������ʴ�����ϣ���������Ti��NaAlH4��150��ʱ���⣬��170�桢15.2MPa���������ظ����⡣NaAlH4����AlCl3��NaH���ʵ������ºϳɡ�NaAlH4�ľ����ṹ��ͼ��ʾ��Ϊ�����塣
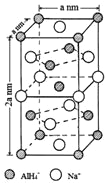
��1����̬Tiԭ�ӵļ۵����Ų�ͼΪ_________��L�ܲ��е����Ƶ���״��_______�֡�
��2��AlCl3��178��ʱ����������__________���壬����������Է�������ԼΪ267���������ӵĽṹʽΪ___________��������λ����������Al�Ĺ���ӻ���ʽΪ____________��
��3��д����AlH4���ռ乹����ͬ��һ�ַ��Ӻ�һ������_________���ѧʽ����
��4��NaAlH4�����У���AlH4�������ҵȾ��Na+��__________����NaAlH4������ܶ�Ϊ_____________g��cm��3���ú�a�Ĵ���ʽ��ʾ����
�������������ƺ��������(HN3)��һ�����������ǵ������������ȫ���ҵȡ�
��1��д����N3-���ڵȵ������һ�ַ���__________�������ʽ����
��2���������(HN3)������(N2H4)��HNO2�����Ƶã�ͬʱ����ˮ�����������������___�����ţ�
A����������HN3�Ļ�ѧ����ʽΪ��N2H4+HNO2= HN3+2 H2O
B��NaN3�ľ����ܴ���KN3�ľ�����
C���������(HN3)��ˮ���γɷ��Ӽ����
D��HN3��N2H4�����ɼ��Լ��ͷǼ��Լ����ɵķǼ��Է��ӡ�
E��HN3�������ĸ�ԭ�ӿ�����һ��ֱ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����3Cl2��6KOH![]() KClO3��5KCl��3H2O�ķ�Ӧ�У�����˵������ȷ����(����)
KClO3��5KCl��3H2O�ķ�Ӧ�У�����˵������ȷ����(����)
A. KCl�ǻ�ԭ���KClO3����������
B. KOH�ڸ÷�Ӧ�����ּ��Ժͻ�ԭ��
C. ��Ӧ��ÿ����3 mol Cl2��ת�Ƶ�����Ϊ5NA
D. ����ԭ�����������ʵ����DZ����������������ʵ�����5��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��1.92 gͭͶ��һ������Ũ�����У�ͭ��ȫ�ܽ⣬����������ɫԽ��Խdz�����ռ���672 mL����(��״��)����ʢ�д����������������ˮ�У�ͨ������ǡ��ʹ������ȫ�ܽ���ˮ�У�����Ҫ��״���µ��������Ϊ(����)
A. 336 mL B. 504 mL
C. 224 mL D. 168 mL
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����������Ҫ����ԭ�ϣ��ڹ�����ռ��Ҫ��λ����ҵ�ϳɰ��ķ�ӦΪ: N2(g)+H2(g)=2NH3(g) ��H<0
��1����ͼ��ʾ�ϳ�NH3��Ӧ��ij��ʱ��t0��t6�з�Ӧ�����뷴Ӧ���̵�����ͼ��t1��t3��t4 ʱ�̷ֱ�ı�ijһ����������������е��ﻯѧƽ���ʱ����У�NH3�����������С��һ��ʱ����___________(��д�������)

A.t1��t1 B.t2��t3 C.t3��t4 D.t5��t6
t4ʱ�ı��������________________��
���������о�:��773Kʱ���ֱ�2molN2��6molH2����һ���̶��ݻ�Ϊ1L���ܱ������У����ŷ�Ӧ�Ľ��У�����������n(H2)��n(NH3)�뷴Ӧʱ��t�Ĺ�ϵ���±���
t/min | 0 | 5 | 10 | 15 | 20 | 25 | 30 |
n(H2)/mol | 6.00 | 4.50 | 3.60 | 3.30 | 3.03 | 3.00 | 3.00 |
n(NH3)/mol | 0 | 1.00 | 1.60 | 1.80 | 1.98 | 2.00 | 2.00 |
��2�����¶��£��˷�Ӧ��ƽ�ⳣ��K=____________��
��3�����¶��£�����ͬ�ݻ�����һ������Ͷ���N2��H2��NH3��Ũ�ȷֱ�Ϊ3mo/L��3mol/L��3mo/L�����ʱV��_____V�� (��">"��<������=��)��
��4�����ϱ��е�ʵ�����ݼ���õ���Ũ��һʱ�����Ĺ�ϵ������ͼ�е����߱�ʾ����ʾc(N2)-t��������______���ڴ��¶��£�����ʼ����4molN2��12 molH2����Ӧ�մﵽƽ��ʱ����ʾc(H2)-t����������Ӧ�ĵ�Ϊ_________��
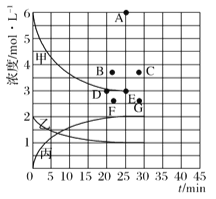
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ת����ϵ�ж�����˵����ȷ����
![]()
A. ��Ӧ���У�(C6H10O5)n�ɱ�ʾ���ۻ���ά��
B. ��Ӧ���У�1mol�����ǿɷֽ����3mol�Ҵ�
C. ���ڿ��������պ��ͭ˿���Ȳ����Ҵ��пɵõ�����
D. ��Ӧ�۵õ������������к����Ҵ������ᣬ���ñ�������������Һ��ȥ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ij�л���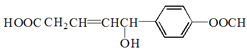 ������������ȷ����
������������ȷ����
A. 1mol���л�����������6mol H2������Ӧ
B. 1mol���л�����������3molNa������Ӧ
C. 1mol���л�����������3mol NaOH������Ӧ
D. 1mol���л�����������2mol NaHCO3������Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��ѧС���������������������װ�ã��û������Ʊ�����ϩ��
��֪�� 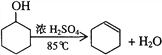
�ܶȣ�g/cm3�� | �۵㣨�棩 | �е㣨�棩 | �ܽ��� | |
������ | 0.96 | 25 | 161 | ������ˮ |
����ϩ | 0.81 | ��103 | 83 | ������ˮ |
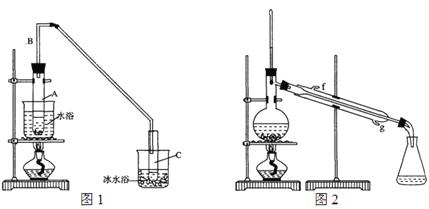
��1���Ʊ���Ʒ��������ͼ1��ʾװ�ã��û������Ʊ�����ϩ��
��12.5 mL�����������Թ�A�У��ټ���1 mLŨ���ᣬҡ�ȷ������Ƭ��������������Ӧ��ȫ�����Թ�C�ڵõ�����ϩ��Ʒ��
��A�����Ƭ��������_____________������B��������_______________��
���Թ�C���ڱ�ˮԡ�е�Ŀ����________________________��
��2���Ʊ���Ʒ��
������ϩ��Ʒ�к��л������������л��������ʵȡ����뱥��ʳ��ˮ�������á��ֲ㣬����ϩ��______�㣨��ϡ����¡�������Һ����________ϴ�ӣ�����ĸ����
A. KMnO4��Һ B. ϡH2SO4 C. Na2CO3��Һ
���ٽ�����ϩ��ͼ2װ��������ȴˮ��____�ڣ�����ĸ�����롣����ʱ������ʯ�ң�Ŀ����______________________________________��
���ռ���Ʒʱ�����Ƶ��¶�Ӧ��______���ң�ʵ���ƵõĻ���ϩ��Ʒ�����������۲��������ܵ�ԭ����______������ĸ����
a. ����ʱ��70����ʼ�ռ���Ʒ
b. ������ʵ����������
c. �Ʊ���Ʒʱ���������Ʒһ������
��3���������ֻ���ϩ��Ʒ�ʹ�Ʒ�ķ�������������________������ĸ����
a. �����Ը��������Һ
b. �ý�����
c. �ⶨ�е�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����Ҫ��ش����⡣
(1)�ʻ����ˮ�ⷴӦ����ⷴӦ�����ֳ��õ�����:
ˮ�ⷴӦ: COS(g)+ H2O(g)![]() H2S(g)+CO2(g) ��H=-34kJ/mol
H2S(g)+CO2(g) ��H=-34kJ/mol
��ⷴӦ��COS(g)+H2(g)![]() H2S(g)+CO(g) ��H=+7kJ/mol
H2S(g)+CO(g) ��H=+7kJ/mol
��֪: 2H2(g)+O2(g)=2H2O(g) ��H=-484 kJ/mol
д����ʾCOȼ���ȵ��Ȼ�ѧ����ʽ:_______________��
(2)̼��H2CO3��K1=4.3��10-7��K2=5.6��10-11������H2C2O4��K1=5.9��10-2��K2=6.4��10-5�� 0.1mol/LNa2CO3��Һ��pH_____0.1mol/L Na2C2O4��Һ��pH��(ѡ����ڡ�����С�ڡ����ڡ�)�������ȷ�Ũ�ȵIJ�����Һ��̼����Һ�������ϣ���Һ�и�������Ũ�ȴ�С��˳����ȷ����___________��(ѡ����)
A.c(H+)>c(HC2O4-)> (HCO3-)>c (CO32-)
B.c(HCO3-)>c(HC2O4-)>c(C2O42-)>c(CO32-)
C.c(H+)>c(HC2O4-)>c(C2O42-)>c(CO32-)
D.c(H2CO3) >c(HCO3-)>c(HC2O4-)>c(CO32-)
(3)��֪�������ܵ���ʵ��ܶȻ�������Ksp(CaF2)=1.5��10-10����25��ʱ2.0��10-3mol/L�����ˮ��Һ�У�������ҺpH(�����峤�仯)���õ�c(HF)��c(F-) ����ҺpH �ı仯��ϵ����ͼ��ʾ:
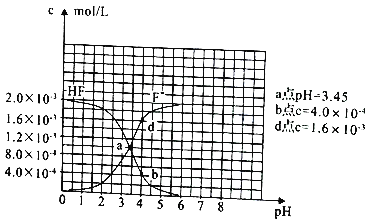
�������Ϣ�ش���������:
��25��ʱ��HF����ƽ�ⳣ������ֵKa��_______��
��4.0��10-3mol/LHF��Һ��4.0��10-4mol/LCaCl2��Һ�������ϣ����ڻ��ҺpHΪ4.0(���Ե��ڻ��Һ����ı仯)��ͨ����ʽ����˵���Ƿ��г���������____________��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com