
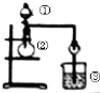
| 选项 | ① | ② | ③ | 实验结论 |
| A | 浓盐酸 | MnO2 | NaBr溶液 | 氧化性Cl2>Br2 |
| B | 浓氨水 | 碱石灰 | AgNO3溶液 | AgOH具有两性 |
| C | 浓硫酸 | Na2SO3 | FeCl3溶液 | SO2具有还原性 |
| D | 稀盐酸 | Na2CO3 | Na2SiO3 | 非金属性:Cl>Si |


科目:高中化学 来源: 题型:
| 装置 | 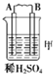 | 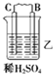 | 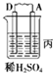 |
| 现象 | 二价金属A不断溶解 | C极质量增加 | A上有气体产生 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 氯化铝融盐电解法是以氯化铝为原料,以碱金属或碱土金属氯化物(含少量MgCl2、KCl、CaCl2)为电解质进行电解制取铝的方法.
氯化铝融盐电解法是以氯化铝为原料,以碱金属或碱土金属氯化物(含少量MgCl2、KCl、CaCl2)为电解质进行电解制取铝的方法.
| △ |
| △ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 物 质 | 除杂试剂 | 分离方法 | |
| A | Cu(Fe) | 稀硫酸 | 过滤 |
| B | Cl2(HCl) | NaOH溶液 | 洗气 |
| C | I2(CCl4) | -- | 过滤 |
| D | Br2(H2O) | 酒精 | 萃取 |
| A、A | B、B | C、C | D、D |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
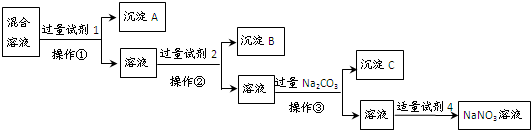
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、光束通过此分散系时会形成一条光亮的“通路” |
| B、此分散系中“纳米材料”的粒子在做不停的、无序的运动 |
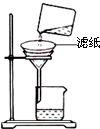
| C、用滤纸过滤的方法可以从此分散系中分离得到该“纳米材料” |
| D、在外加电场作用下,“纳米材料”的粒子可能向某一极做定向运动 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、摩尔是国际单位制确定的一个物理量 |
| B、摩尔是表示物质的量的单位 |
| C、1 mol氧气中含有6.02×1023个氧原子 |
| D、水的摩尔质量是18g |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com