
【题目】“凯式定氮法”测定奶粉中蛋白质的含量是由丹麦人约翰·凯达尔发明的,其原理是用强酸处理蛋白质样品,让样品当中的氮释放出来,通过测得氮的含量,再乘以系数6.38,即为蛋白质含量。凯式定氮法步骤如下:
①样品处理:准确称取一定质量的奶粉试样置于烧瓶中,加入稀硫酸及相应催化剂,一定条件下充分反应,所得产物用水溶解并冷却后全部转移到容量瓶中定容。
②碱化蒸馏:量取一定体积容量瓶中的溶液转移至图示中的反应管中,再加入足量NaOH溶液,塞好进样口橡皮塞。通入高温水蒸气,用吸收剂吸收产生的氨气。

③滴定:向吸收氨气后的溶液中滴加指示剂,用标准盐酸溶液滴定至终点。
根据以上知识回答下列问题:
(1)样品处理的目的是_______________________________________________________。
(2)碱化蒸馏时反应的离子方程式为_____________________,冷凝管中冷却水的进水口为__________(填“A”或“B”);如何通过简单的实验确定生成的氨气全部被水蒸气蒸出并进入锥形瓶__________________。
(3)凯式定氮法测定奶粉中蛋白质的含量灵敏度高,操作简单,缺点是____________________________。
(4)当奶粉含下列杂质或出现下列错误的实验操作时,会使所测蛋白质含量值“增大”的是__________(填字母)。
A.含三聚氰胺( )
)
B.样品入口未用蒸馏水冲洗
C.第(1)步定容时俯视刻度线
D.滴定开始时仰视读数,滴定终点时俯视读数
【答案】将奶粉中氮元素全部转化为NH![]() NH
NH![]() +OH-
+OH-![]() NH3↑+H2OB取最后一滴冷凝管中流出的液体,用红色石蕊试纸(或pH试纸)检验不变蓝(或呈中性)无法确定氮元素是否一定来自于蛋白质AC
NH3↑+H2OB取最后一滴冷凝管中流出的液体,用红色石蕊试纸(或pH试纸)检验不变蓝(或呈中性)无法确定氮元素是否一定来自于蛋白质AC
【解析】
凯氏定氮法测定奶粉中蛋白质含量原理为:通过样品处理把氮元素转化为NH4+,加入氢氧化钠转化为氨气,用吸收剂吸收,用盐酸滴定,通过消耗盐酸的量来计算氮元素的含量和蛋白质的含量.
(1)蛋白质中的氮元素不容易测定,从测量步骤可知样品处理目的是把蛋白质中氮元素转化为NH4+;(2)铵根离子与氢氧根离子反应生成氨气,则碱化蒸馏时反应的离子方程式为:NH![]() +OH-
+OH-![]() NH3↑+H2O;冷凝水与蒸汽的流向相反时冷却效果好,所以冷凝水从B口进入,从A口流出;根据氨气的性质分析;氨气的水溶液显碱性,取最后一滴冷凝流出液,用红色石蕊试纸(或pH试纸)检验不变蓝(显中性),则证明氨全部被水蒸出并进入锥形瓶;
NH3↑+H2O;冷凝水与蒸汽的流向相反时冷却效果好,所以冷凝水从B口进入,从A口流出;根据氨气的性质分析;氨气的水溶液显碱性,取最后一滴冷凝流出液,用红色石蕊试纸(或pH试纸)检验不变蓝(显中性),则证明氨全部被水蒸出并进入锥形瓶;
(3)测定原理为:把蛋白质样品用中的氮元素释放出来,通过测定氮元素的质量从而换算出蛋白质的含量,此方法的局限性很明显,它把样品中释放出来的N元素全部归为蛋白质中的N元素,若样品中含有其他含氮化合物,则无法准确测定蛋白质的含量;
(4)A.三聚氰胺( )含氮量高,会使计算结果中蛋白质含量值“增加”,故A符合; B.样品入口未用蒸馏水冲洗,损失了氮元素,会使计算结果中蛋白质含量值偏低,故B不符合; C.第①步定容时俯视刻度线,读数偏小,则溶液体积偏小,会使计算结果中蛋白质含量值“增加”,故C符合;D.滴定开始时仰视读数,滴定终点时俯视读数,盐酸读数偏小,会使计算结果中蛋白质含量值偏低,故D不符合;故答案为:AC。
)含氮量高,会使计算结果中蛋白质含量值“增加”,故A符合; B.样品入口未用蒸馏水冲洗,损失了氮元素,会使计算结果中蛋白质含量值偏低,故B不符合; C.第①步定容时俯视刻度线,读数偏小,则溶液体积偏小,会使计算结果中蛋白质含量值“增加”,故C符合;D.滴定开始时仰视读数,滴定终点时俯视读数,盐酸读数偏小,会使计算结果中蛋白质含量值偏低,故D不符合;故答案为:AC。


 智能训练练测考系列答案
智能训练练测考系列答案科目:高中化学 来源: 题型:
【题目】Ⅰ. CH3OH是一种无色有刺激性气味的液体,在生产生活中有重要用途,同时也是一种重要的化工原料。
(1)已知CH3OH(g)+1/2O2(g) ![]() CO2(g)+2H2(g)的能量变化如图所示,下列说法正确的是______(填字母)。
CO2(g)+2H2(g)的能量变化如图所示,下列说法正确的是______(填字母)。
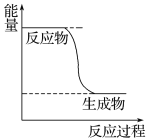
a.CH3OH转变成H2的过程是一个吸收能量的过程
b.H2的生成速率与CH3OH的消耗速率之比为1∶2
c.化学变化不仅有新物质生成,同时也一定有能量变化
d.1 mol H—O键断裂的同时2 mol C===O键断裂,则反应达最大限度
(2)某温度下,将5molCH3OH和2molO2充入2L的密闭容器中,经过4min反应达到平衡,测得c(O2)=0.2mol·L-1,4min内平均反应速率v(H2)=________________,则CH3OH的转化率为___________。
Ⅱ.在恒温条件下将一定量X和Y的混合气体通入一容积为2 L的密闭容器中,X和Y两物质的浓度随时间变化情况如下图。
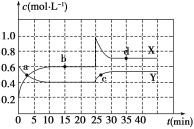
(1)该反应的化学方程式为(反应物或生成物用符号X、Y表示)______________________________。
(2)a、b、c、d四个点中,表示化学反应处于平衡状态的点是___________。
Ⅲ.当电极a为Al,电极b为Mg,电解质溶液为氢氧化钠溶液时,该电池的正极为________,负极的电极反应式为_______________________________。当反应中收集到标准状况下224 mL气体时,消耗的a电极质量为________g。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】俄罗斯科学家用铪和钨两种核素精确确定了地球和月球的年龄,得出月球至少比地球早700万年形成,它们是根据18272Hf(铪-182)和18274W(钨-182)两种核素的含量比例得出的。下列有关铪-182和钨-182的关系说法正确的是( )
A. 中子数相等 B. 互为同位素
C. 原子质量几乎相同 D. 在周期表中处于相邻位置
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA代表阿伏加德罗常数的值。下列说法正确的是
A. 常温常压下,124 g P4中所含P—P键数目为4NA
B. 100 mL 1mol·L1FeCl3溶液中所含Fe3+的数目为0.1NA
C. 标准状况下,11.2 L甲烷和乙烯混合物中含氢原子数目为2NA
D. 密闭容器中,2 mol SO2和1 mol O2催化反应后分子总数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A.π键是由两个p电子“头碰头”重叠形成的
B.σ键是镜面对称,而π键是轴对称
C.乙烷分子中的键全为σ键,而乙烯分子中含σ键和π键
D.H2分子中含σ键,而Cl2分子中还含π键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在t ℃时,AgBr在水中的沉淀溶解平衡曲线如图所示。已知t ℃时AgCl的Ksp=4×10-10,下列说法正确的是( )
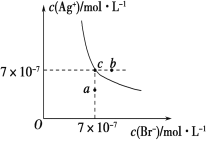
A. 加入NaBr固体,AgBr的溶解度减小,Ksp也减小
B. 在AgBr饱和溶液中加入固体NaBr,可使溶液中c点变到b点
C. 图中a点对应的是有AgBr沉淀生成
D. 在t ℃时,AgCl(s)+Br-(aq) AgBr(s)+Cl-(aq)的平衡常数K≈816
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】a、b、c、X是中学化学中常见的四种物质,且a、b、c中含有同一种元素,其转化关系如下图所示。下列说法不正确的是

A. 若a、b、c均为厨房中常用的物质,则构成c中的阳离子半径小于其阴离子半径
B. 若a为一种气态氢化物,X为O2,则a分子中可能含有10个或者18个电子
C. 若b为一种两性氢氧化物,则X可能是强酸,也可能是强碱
D. 若a为固态非金属单质,X为O2,则O元素与a元素的原子序数之差可能为8
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示装置中观察到电流计指针偏转,M棒变粗,N棒变细,由此判断下表中所列M、N、P物质,其中可以成立的是( )

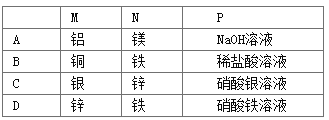
A. AB. BC. CD. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com