
【题目】用0.1000 mol/L的盐酸滴定20.00 mL NaOH溶液,测定其浓度,下列说法正确的是
A.需用NaOH溶液润洗锥形瓶
B.用量筒量取20.00 mL NaOH溶液
C.使用酚酞做指示剂,滴定终点的现象为溶液浅红色褪去,半分钟不变色
D.滴定前,没有除去酸式滴定管中的气泡,滴定后气泡消失,所测浓度会偏小
 教材全解字词句篇系列答案
教材全解字词句篇系列答案科目:高中化学 来源: 题型:
【题目】已知常温下:Ksp(AgCl)=1.8×10-10,Ksp(Ag2CrO4)=1.9×10-12,下列叙述正确的是( )
A.AgCl在饱和NaCl溶液中的Ksp比在纯水中的Ksp小
B.已知Ksp(AgBr)<Ksp(AgCl) ,故AgBr不可能转化为AgCl
C.将0.001 mol·L-1的AgNO3溶液滴入0.001 mol·L-1的KCl和0.001 mol·L-1的K2CrO4溶液中先产生Ag2CrO4沉淀
D.向AgCl的悬浊液中滴加浓氨水,沉淀溶解,说明AgCl的溶解平衡向右移动
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】X、Y、Z是三种气态物质,在一定温度下其变化符合下图。下列说法一定正确的是( )
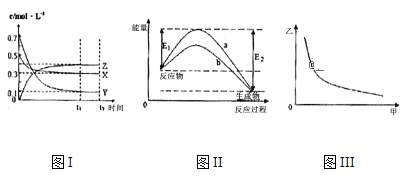
A.该反应的热化学方程式为X(g) +3Y(g) 2Z(g) △H= -(E2-E1)kJ
B.若图III中甲表示压强,乙表示Z的含量,则其变化符合图III中曲线
C.该温度下,反应的平衡常数数值约为533,若升高温度,该反应的平衡常数减小,Y的转化率降低
D.图II中曲线b是加入催化剂时的能量变化曲线,曲线a是没有加入催化剂时的能量变化曲线
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用原电池原理,在室温下从含低浓度铜的酸性废水中回收铜的实验装置如图所示,下列说法错误的是
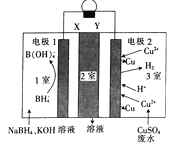
A. X、Y依次为阳离子、阴离子选择性交换膜
B. 负极的电极反应式:BH4-+8OH-一8e-═B(OH)4-+4H2O
C. 2室流出的溶液中溶质为Na2SO4和K2SO4
D. 电路中每转移1mol电子,电极2上有32gCu析出
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ca3N2是重要的化学试剂,易潮解、被氧化,实验室用N2和金属钙在加热条件下制备Ca3N2的装置如图所示(已知:钙能在CO2中燃烧)。请回答下列问题:
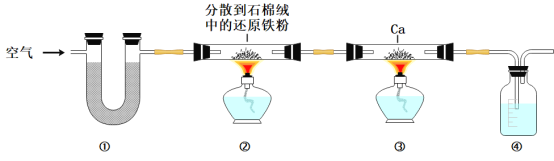
(1)Ca3N2中所含化学键的类型为____________。
A.离子键 B.共价键 C.氢键
(2)装置①中的U型管中的物质为___________,其作用为________________。
(3)装置②的作用为___________________________。
(4)组装好仪器,装入药品,通入空气后,应先点燃____________处酒精灯,再点燃另一个酒精灯。
(5)写出Ca3N2潮解时的化学方程式__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是化学家为纪念元素周期表诞辰150周年而绘制的一种新型元素周期表。在该表中能直观地看出各种元素在地球上的丰度(丰度即该元素占地球所有原子总数的百分比。用该元素所在格子的面积表示丰度的相对大小)。

(1)在图中找到地球上含量最多的元素。其原子结构示意图为___,海水中含量最多的金属离子的结构示意图为___。
(2)宇宙中含量最多的元素为氢元素。氢元素有多种同位素,其中原子核内含有2个中子的核素可表示为___。水分子的电子式为___。
(3)H、C、O和N等丰度较大的元素是构成地球生命物质的主要“材料”。
①H、C、O和N的原子半径从大到小的顺序为___。
②下列与生命活动有关的物质中一定含有H、C、O和N四种元素的是___。
a.蛋白质 b.糖类 c.油脂
(4)Al是地壳中含量最多的金属元素。Al2O3和Al(OH)3均为两性化合物。Al(OH)3和盐酸反应的离子方程式为___,Al(OH)3和NaOH溶液反应的化学方程式为___。试运用元素周期律分析Al2O3和Al(OH)3均为两性化合物的原因是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.(1)室温下,使用pH计测定0.1mol/L NH4Cl溶液的pH=5.12.由此可以得到的结论是_____________(填字母).
a、溶液中c(H+)>c(OH) b、NH4+水解是微弱的
c、NH3H2O是弱碱 d、由H2O电离出的c(H+)<107mol/L
e、物质的量浓度相等的氨水和盐酸等体积混合,溶液pH=7
(2)室温下,用0.1mol/LNaOH溶液分别滴定20.00mL0.1mol/L的盐酸和醋酸,滴定曲线如图所示,下列说法正确的是

①表示滴定盐酸的曲线是____________(填序号).
②滴定醋酸溶液的过程中:
i、V(NaOH)=10.00mL时,溶液中离子浓度由大到小的顺序为________________________.
ii、当c(Na+)=c(CH3COO)+c(CH3COOH)时,溶液pH________7(填“>”、“=”或“<”).
Ⅱ.复分解反应是中学化学中常见的一种反应类型。
(1)已知在常温下测得浓度均为0.1molL1的下列6种溶液的pH值:
溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | C6H5ONa |
pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 11.3 |
复分解存在这样一个规律:一种较强酸与另一种较弱酸的盐可以自发地反应,生成较弱酸和较强酸的盐,如:2CH3COOH+Na2CO3=2CH3COONa+CO2↑+H2O 若换个角度看,它同时揭示出另一条规律,即碱性较强的物质发生类似反应可以生成碱性较弱的物质。依照该规律,请判断下列反应不能成立的是______(填编号).
A.CO2+H2O+2NaClO═Na2CO3+2HClO
B.CO2+H2O+NaClO═NaHCO3+HClO
C.CO2+H2O+C6H5ONa→NaHCO3+C6H5OH
D.CO2+H2O+2C6H5ONa→Na2CO3+2C6H5OH
E.Na2CO3+C6H5OH→NaHCO3+C6H5ONa
F.CH3COOH+NaCN═CH3COONa+HCN
(2)根据前述信息判断,常温下,浓度均为0.05molL1的下列5种物质的溶液中,pH最小的是______(填编号),其pH值为______(填数值);pH最大的是______(填编号).
①HCN ②CH3COOH ③HClO4 ④HClO ⑤H2SO4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上制取硫酸铜采用途径I而不采用途径Ⅱ,这样做的优点是

①节省能源 ②不产生污染大气的SO2 ③提高了H2SO4的利用率 ④提高了Cu的利用率
A.仅①②B.仅②③④C.仅①②③D.全部
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分枝酸可用于生化研究。其结构简式如图。下列关于分枝酸的叙述正确的是

A. 分子中存在两种含氧官能团
B. 1mol该有机物可以分别与3molBr2和5molH2发生加成反应
C. 该有机物可以使溴水和酸性高锰酸钾溶液均褪色
D. 该有机物可以发生氧化反应、加成反应、取代反应和水解反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com