
【题目】环境监测显示,某地市的主要气体污染物为SO2、NOx、CO等,其主要来源为燃煤、机动车尾气。进行如下研究:
(1)为减少燃煤对SO2的排放,可将煤转化为清洁燃料水煤气(CO和H2)。
已知:![]() ΔH=-241.8kJ·mol-1
ΔH=-241.8kJ·mol-1
![]() ΔH=-110.5kJmol-1
ΔH=-110.5kJmol-1
写出焦炭与1mol水蒸气反应生成水煤气的热化学方程式:________。
(2)①在101 kPa时,H2(g)在 1.00 mol O2(g)中完全燃烧生成2.00 mol H2O(l)放出571.6 kJ的热量,表示H2燃烧热的热化学方程式为________________________________。
②1.00 L 1.00 mol·L1 H2SO4溶液与2.00 L 1.00 mol·L1 NaOH溶液完全反应,放出114.6 kJ热量,表示其中和热的热化学方程式为____________________________。
(3)利用如图所示装置(电极均为惰性电极)可吸收SO2,并利用阴极排出的溶液吸收NO2。
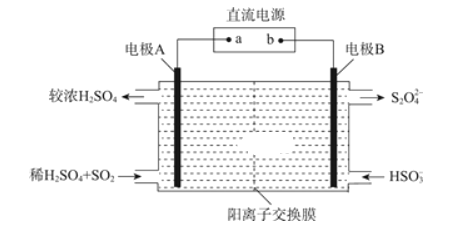
电极A的电极反应式为________;
【答案】C(s)+H2O(g)=CO(g)+H2(g) ΔH=+131.3kJ·mol-1 ![]()
![]()
![]()
【解析】
(1)根据盖斯定律进行计算,用第一个热化学方程式减去第二个热化学方程式可得焦炭与水蒸气反应的热化学方程式;
(2)①燃烧热指的是1mol物质完全燃烧生成稳定的物质时放出的热量,据此写出热化学方程式;
②中和热为稀酸和稀碱反应生成1mol H2O(l)放出的热量,据此写出热化学方程式;
(3)由图可知,电极A为阳极,SO2失电子发生氧化反应生成![]() ,据此写出电极反应方程式。
,据此写出电极反应方程式。
(1)已知:①![]() ΔH=-241.8kJ·mol-1
ΔH=-241.8kJ·mol-1
②![]() ΔH=-110.5kJmol-1,
ΔH=-110.5kJmol-1,
水煤气的主要成分为CO、H2O,根据盖斯定律,②-①可得焦炭与1mol水蒸气反应生成水煤气的热化学方程式:C(s)+H2O(g)=CO(g)+H2(g) ΔH=+131.3kJ·mol-1;
故答案为:C(s)+H2O(g)=CO(g)+H2(g) ΔH=+131.3kJ·mol-1;
(2)①由题可知,![]() , H2的燃烧热热化学方程式即1molH2完全燃烧生成1mol液态水的热化学方程式,根据盖斯定律将该热化学反应方程式×
, H2的燃烧热热化学方程式即1molH2完全燃烧生成1mol液态水的热化学方程式,根据盖斯定律将该热化学反应方程式×![]() 可得H2的燃烧热的热化学方程式:
可得H2的燃烧热的热化学方程式:![]() ;
;
故答案为:![]() ;
;
②由题可知,![]() ,该反应的中和热为表示生成1mol水的热化学方程式,将上述热化学方程式×
,该反应的中和热为表示生成1mol水的热化学方程式,将上述热化学方程式×![]() 可得该反应的中和热为:
可得该反应的中和热为:![]() ;
;
故答案为:![]() ;
;
(3)由图可知,电极A为阳极,SO2失电子发生氧化反应生成![]() ,故电极反应方程式为:
,故电极反应方程式为:![]() ;
;
故答案为:![]() 。
。


科目:高中化学 来源: 题型:
【题目】已知反应:2NO(g)+Br2(g)![]() 2NOBr(g) △H=-a kJ·mol-1 (a>0),其反应机理如下
2NOBr(g) △H=-a kJ·mol-1 (a>0),其反应机理如下
①NO(g)+Br2(g)![]() NOBr2(g) 快 ②NO(g)+NOBr2(g)
NOBr2(g) 快 ②NO(g)+NOBr2(g)![]() 2NOBr(g) 慢
2NOBr(g) 慢
下列有关该反应的说法正确的是( )
A. 该反应的速率主要取决于①的快慢
B. NOBr2是该反应的催化剂
C. 正反应的活化能比逆反应的活化能小a kJ·mol-1
D. 增大Br2(g)浓度能增大活化分子百分数, 加快反应速率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图两个装置中,液体体积均为200ml,开始时电解质溶液的浓度均为 0.1mol/L,工作一段时间后,测得导线上都通过了0.02mol电子,若不考虑溶液体积的变化,下列叙述正确的是( )

A. 产生气体体积①=②
B. 电极上析出固体质量①<②
C. 溶液的pH变化:①减小②增大
D. 电极反应式:①中阳极Cu2++2e-=Cu,②中负极Zn-2e-=Zn2+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是制取和收集某气体的实验装置,该装置可用于
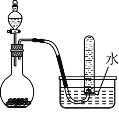
A.用浓盐酸和二氧化锰反应制取Cl2
B.用浓氨水和生石灰反应制取NH3
C.用浓硝酸与铜反应制取NO2
D.用过氧化钠固体和水反应制取O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁电池是一种新型可充电电池,与普通高能电池相比,该电池长时间保持稳定的放电电压。高铁电池的总反应为:3Zn +2K2FeO4+8H2O![]() 3Zn(OH)2+2Fe(OH)3+ 4KOH,下列叙述不正确的是( )
3Zn(OH)2+2Fe(OH)3+ 4KOH,下列叙述不正确的是( )
A.放电时负极反应为:Zn – 2e-+ 2OH- = Zn(OH)2
B.充电时阴极反应为:Fe(OH)3- 3e-+ 5OH- = FeO42-+ 4H2O
C.放电时每转移3mol电子,正极有1mol K2FeO4被还原
D.放电时正极附近溶液的碱性增强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向13.6g Cu和Cu2O的混合物中加入某浓度的稀硝酸0.25 L,固体物质完全反应,生成NO和Cu(NO3)2。在所得溶液中加入0.5 mol/L的NaOH溶液1 L,反应后溶液恰好呈中性,金属离子已完全沉淀,沉淀质量为19.6 g,下列说法不正确的是
A.Cu与Cu2O的物质的量之比为2∶1
B.硝酸的物质的量浓度为2 mol/L
C.Cu、Cu2O与硝酸反应后剩余HNO3的物质的量为0.5 mol
D.产生的NO在标准状况下的体积为2.24 L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下面是合成某药物的中间体分子(由9个碳原子和若干氢、氧原子构成)的结构示意图:
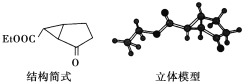
试回答下列问题:
(1)通过对比上面的结构简式与立体模型,请指出结构简式中的“Et”表示的基团是(写结构简式)_____;该药物中间体的分子式为________。
(2)该分子中含有_________个不饱和碳原子。
(3)该药物中间体中含氧官能团的名称为___________。
(4)该药物中间体分子中与碳原子结合的氢原子被溴原子取代,所得的一溴代物有______种。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.恒温恒压容器中,反应A(s)+2B(g) ![]() 2C(g)达平衡后,再通入气体C,再达平衡时气体B的浓度保持不变
2C(g)达平衡后,再通入气体C,再达平衡时气体B的浓度保持不变
B.恒温恒容容器中,通入一定量的N2O4,反应 N2O4 (g) ![]() 2NO2 (g)达平衡后,再通入N2O4,平衡正向移动,再达平衡时N2O4的转化率增大
2NO2 (g)达平衡后,再通入N2O4,平衡正向移动,再达平衡时N2O4的转化率增大
C.恒温下,向密闭容器中加入NH2COONH4固体,发生反应NH2COONH4(s) ![]() 2NH3(g)+CO2(g) ,混合气体的平均相对分子质量不再随时间变化时反应达平衡状态
2NH3(g)+CO2(g) ,混合气体的平均相对分子质量不再随时间变化时反应达平衡状态
D.恒温恒容容器中,N2(g)+3H2(g) ![]() 2NH3(g)达平衡后,改变条件使平衡正向移动,再达平衡时NH3的体积分数一定增大
2NH3(g)达平衡后,改变条件使平衡正向移动,再达平衡时NH3的体积分数一定增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下某H2CO3溶液的pH约为5.5,c (CO32-)约为5×10-11 mol/L,该溶液中浓度最低的离子是
A.HCO3-B.CO32-C.H+D.OH-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com