
【题目】在密闭容器中进行的反应C(s)+H2O(g)![]() CO(g)+H2(g),能使反应速率加快的措施有( )
CO(g)+H2(g),能使反应速率加快的措施有( )
①增加炭的量②升高温度③将炭粉碎④恒容通入水蒸气⑤通过减小容器体积增大压强⑥恒容通入N2
A.②③④⑤B.②③④⑤⑥C.①②③④⑤D.①②③④
科目:高中化学 来源: 题型:
【题目】我国科研人员提出了由CO2和CH4转化为高附加值产品CH3COOH的催化反应历程。该历程示意图如下。

下列说法不正确的是
A. 生成CH3COOH总反应的原子利用率为100%
B. CH4→CH3COOH过程中,有C―H键发生断裂
C. ①→②放出能量并形成了C―C键
D. 该催化剂可有效提高反应物的平衡转化率
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】无色的混合气体甲,可能含NO、CO2、NO2、NH3、N2中的几种,将100mL甲气体依次通过下图实验的处理,结果得到酸性溶液,几乎无气体剩余,则甲气体的组成为
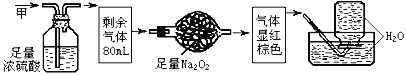
A.NH3、NO2、N2B.NH3、NO、CO2
C.NH3、NO2、CO2D.NO、CO2、N2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高铁酸钾(K2FeO4)是一新型高效无毒的多功能水处理剂。资料:K2FeO4为紫色固体,微溶于KOH溶液,具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
(1)制备K2FeO4
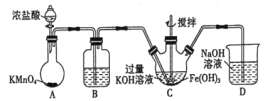
①写出A中发生反应的化学方程式______。
②除杂装置B中的试剂为____。
③C为制备K2FeO4装置,KOH溶液过量的原因是____。
④D为尾气处理装置,发生反应的离子方程式为____。
(2)探究K2FeO4的性质取C中紫色溶液,加入稀硫酸,产生黄绿色气体,得溶液a,经检验气体中含有Cl2。为证明K2FeO4能否氧化Cl而产生Cl2设计以下方案:
方案Ⅰ | 取少量溶液a,滴加KSCN溶液至过量,溶液呈红色 |
方案Ⅱ | 用KOH溶液充分洗涤C中所得固体,再用KOH溶液将K2FeO4溶出,得到紫色溶液b。取少量b,滴加盐酸,有Cl2产生 |
①由方案Ⅰ中溶液变红可知a中含有____。该离子的产生__(填“能”或“不能”)判断一定是由K2FeO4被Cl还原而形成的。
②方案Ⅱ用KOH溶液洗涤的目的是____,方案Ⅱ得出氧化性:Cl2 ___FeO42(填“![]() ”或“
”或“![]() ”)。
”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关描述正确的是( )
A. 分子组成符合![]() 的烃,分子中一定有4个原子共直线
的烃,分子中一定有4个原子共直线
B. C2H2和C6H6无论以何种比例混合,只要总质量一定,完全燃烧,消耗氧气的量保持不变
C. ![]() 、
、![]() 、
、![]() 在常温下均为气体
在常温下均为气体
D. 乙炔能使溴水和酸性高锰酸钾溶液褪色,所发生反应的反应类型相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 在鸡蛋清溶液中分别加入饱和![]() 溶液,都会因盐析产生沉淀
溶液,都会因盐析产生沉淀
B. 油脂为高分子化合物,其饱和程度越大,熔点越低
C. ![]() 的水解产物是
的水解产物是![]() 和
和![]()
D. 麦芽糖及其水解产物均能与新制氢氧化铜悬浊液反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图装置,放电时可将 Li、CO2 转化为 Li2CO3 和 C,充电时选用合适催化剂仅使Li2CO3 转化为Li、CO2 和O2。下列有关表述正确的是( )
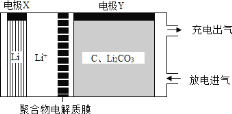
A.放电时,Li+向电极X 方向移动
B.放电时,每转移 4mol 电子,生成 1mol C
C.充电时,电极Y 应与外接直流电源的负极相连
D.充电时阳极的电极反应式为 C+2Li2CO3+4e- = 3CO2+4Li+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮的化合物在生产生活中广泛存在。请回答:
(1)催化转化器可使汽车尾气中的主要污染物(CO、NOx、碳氢化合物)进行相互反应, 生成无毒物质,减少汽车尾气污染。
已知:
N2(g)+O2(g)=2NO(g) △H1=+180.5kJ·mol-1
2C(s)+O2(g)=2CO(g) △H2= -221.0 kJ·mol-1
C(s)+O2(g)=CO2(g) △H3= -393.5 kJ·mol-1
计算尾气转化反应 2NO(g) +2CO(g)=N2(g)+2CO2(g)的△H=_____。
(2)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。反应的热化学方程式为:4NH3(g)+6NO(g) ![]() 5N2(g)+6H2O(g) △H= -11.63 kJ·mol-1。反应在2L 密闭容器中进行,在其它条件相同时,使用不同的催化剂 A、B、C,产生 N2 的物质的量随时间变化如图 1 所示。
5N2(g)+6H2O(g) △H= -11.63 kJ·mol-1。反应在2L 密闭容器中进行,在其它条件相同时,使用不同的催化剂 A、B、C,产生 N2 的物质的量随时间变化如图 1 所示。

图1 图2
①下列有关说法正确的是__________________________________。
A. 反应在任何温度下均可自发进行
B. 50 s 在催化剂A 作用下,平均反应速率v(N2)=2.5×10-2mol·L-1·s-1
C. 用催化剂C 达到平衡时,N2 产率最小
D. 分离出反应体系中的H2O(g)有利于氮氧化物的脱除
E. 相同条件下,若使用催化剂 B,使逆反应速率加快 100 倍,使用催化剂 C,使正反应速率加快 65 倍,则应该选用催化剂 B
②在催化剂A 的作用下,经过相同时间,测得脱氮率随反应温度的变化情况如图 2 所示,据图可知,在相同的时间内,300℃之前,温度升高脱氮率逐渐增大,300℃之后温度升高脱氮率逐渐减小(假设催化剂活性不受影响),写出脱氮率随温度变化的原因__________________________。
③其他条件相同时,请在图 2 中补充在催化剂B 作用下脱氮率随温度变化的曲线。__________________________________________________________
(3)以连二硫酸根(S2O42-)为媒介,使用间接电化学法也可处理燃煤烟气中的 NO,装置如图所示
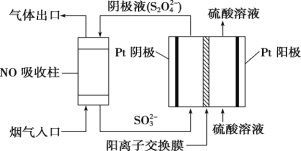
① 阴极区的电极反应式为___________________________________________ 。
② 通电时,当电路中转移 0.2mol e-,可吸收的 NO 在标准状况下的体积为 896mL。则 NO转化后的产物为_____________________________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 烷烃的通式为CnH2n+2,随n值增大,碳元素的质量百分含量逐渐减小
B. 乙烯与溴加成反应的产物为溴乙烷
C. 1 mol苯恰好与3 mol氢气完全加成,说明苯分子中有三个碳碳双键
D. n=7,主链上有5个碳原子的烷烃共有5种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com