
【题目】反应N2O4(g)2NO2(g) ΔH=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强变化曲线如图所示。下列说法正确的是( )
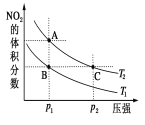
A.A、C两点的反应速率:A>C
B.A、C两点气体的颜色:A、C两点一样颜色
C.由状态A到状态B,可以用降温的方法
D.A、C两点气体的平均相对分子质量:A>C
【答案】C
【解析】
N2O4(g)2NO2(g) ΔH=+57 kJ·mol-1,升高温度,平衡正向移动,降低温度,平衡逆向移动;增大压强,平衡逆向移动,减小压强,平衡正向移动。
A.A、C两点对应的温度相同,C点压强大于A点,则C点反应速率大于A点,A错误;
B.A到C,压强增大,体积减小,NO2(g)的浓度增大,然后平衡逆向移动,最终二氧化氮的浓度比原浓度大,故气体颜色较深,即C点气体颜色比A点深,B错误;
C.A到B,NO2的体积分数减小,说明相同压强下,T2到T1,平衡逆向移动,结合分析可知,T2到T1为降温,即由状态A到状态B,可以用降温的方法,C正确;
D.A点到C点,压强增大,平衡逆向移动,该反应的逆反应为气体相对分子质量增大的反应,即A点气体的平均相对分子质量小于C点气体的平均相对分子质量,D错误。
答案选C。


科目:高中化学 来源: 题型:
【题目】H2O2分解速率受多种因素影响。实验测得 70 ℃时不同条件下H2O2浓度随时间的变化如图所示。下列说法正确的是
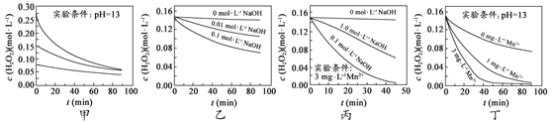
A.图甲表明,其他条件相同时,H2O2浓度越小,其分解速率越快
B.图乙表明,其他条件相同时,溶液pH越小,H2O2分解速率越快
C.图丙表明,少量Mn 2+存在时,溶液碱性越强,H2O2分解速率越快
D.图丙和图丁表明,碱性溶液中,Mn2+对H2O2分解速率的影响大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】醋酸亚铬[(CH3COO)2Cr·H2O]为砖红色晶体,难溶于冷水,易溶于酸,在气体分析中用作氧气吸收剂。一般制备方法是先在封闭体系中利用金属锌作还原剂,将三价铬还原为二价铬;二价铬再与醋酸钠溶液作用即可制得醋酸亚铬。实验装置如图所示,回答下列问题:

(1)实验中所用蒸馏水均需经煮沸后迅速冷却,目的是_________,仪器a的名称是_______。
(2)将过量锌粒和氯化铬固体置于c中,加入少量蒸馏水,按图连接好装置,打开K1、K2,关闭K3。
①c中溶液由绿色逐渐变为亮蓝色,该反应的离子方程式为_________。
②同时c中有气体产生,该气体的作用是_____________。
(3)打开K3,关闭K1和K2。c中亮蓝色溶液流入d,其原因是________;d中析出砖红色沉淀,为使沉淀充分析出并分离,需采用的操作是___________、_________、洗涤、干燥。
(4)指出装置d可能存在的缺点______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,C和H2O(g)在密闭容器里发生下列反应:
①C(s)+H2O(g)![]() CO(g)+H2(g), ②CO(g)+H2O(g)
CO(g)+H2(g), ②CO(g)+H2O(g)![]() CO2(g)+H2(g)
CO2(g)+H2(g)
当反应达到平衡时,c(H2)=1.9 mol·L-1,c(CO)=0.1 mol·L-1。则下列叙述正确的有
A. CO在平衡时转化率为10%
B. 平衡浓度c(CO2)=c(H2)
C. 平衡时气体平均相对分子质量约为23.3
D. 其他条件不变时,缩小体积,H2O(g)的转化率随之降低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组粒子在溶液中可以大量共存,且加入或通入试剂M后,发生反应的离子方程式也正确的是
选项 | 微粒组 | 试剂M | 发生反应的离子方程式 |
A | K+、Na+、 | 少量HCl | 2H++ |
B |
| 过量H2S | Fe2++H2S |
C | HClO、Na+、Fe3+、 | 过量CaCl2 | Ca2++ |
D |
| 少量CO2 | CO2+2 |
A.AB.BC.CD.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某高中科研小组模拟工业尿素法生产肼(N2H4),具体方法:先将尿素、次氯酸钠和氢氧化钠溶液混合,然后在催化剂存在的条件下反应制得肼,利用氮气吹出混合物中的肼,并用硫酸吸收制备硫酸肼。具体实验原理图如下:
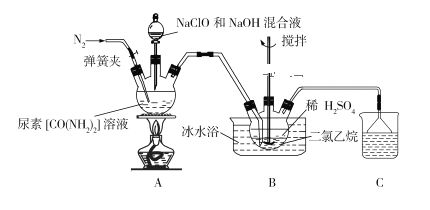
已知:①肼极易溶于水,长期暴露在空气中或短时间受高温作用会爆炸分解。
②硫酸肼(N2H4·H2SO4)是类似于NH4HSO4的盐类,白色固体,微溶于冷水,易溶于热水,不溶于乙醇和二氯乙烷等有机溶剂。
③密度:ρ硫酸肼>ρ二氯乙烷>ρ稀硫酸
(1)盛装尿素溶液的装置名称为_____________________;硫酸肼的水溶液中含有多种阳离子,其中阳离子N2H5+的电子式为________________________。
(2)反应前应先通入一段时间氮气,其目的为________________________________。
(3)装置A中发生反应制备肼的离子方程式为_______________________________。
(4)装置B中二氯乙烷的作用为__________________________________________;使用冰水浴的作用__________________________________________________。
(5)装置B反应完全后需经过过滤、洗涤、干燥等操作得到硫酸肼,洗涤过程中最好选择下列那种洗涤剂________________(填字母)。
A.冷水 B.热水 C.无水乙醇 D.饱和食盐水
(6)若实验中所用的NaClO和NaOH混合液中两溶质的浓度均为0.1mol·L1,则此溶液中离子浓度的大小顺序为______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是
A. 24 g 镁与27 g铝中,含有相同的质子数
B. 同等质量的氧气和臭氧中,电子数相同
C. 1 mol重水与1 mol水中,中子数比为2∶1
D. 1 mol乙烷和1 mol乙烯中,化学键数相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】磷酸(H3PO4)是一种中强酸,常温下,H3PO4水溶液中含磷微粒的分布分数(平衡时某微粒的浓度占各含磷微粒总浓度的分数)与pH的关系如图,下列说法正确的是( )
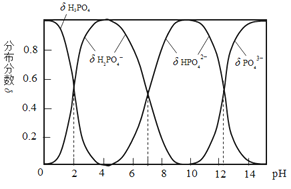
A.H3PO4的电离方程式为:H3PO4![]() 3H++ PO43
3H++ PO43
B.pH=2时,溶液中大量存在的微粒有:H3PO4、H2PO4、HPO42、PO43
C.滴加NaOH溶液至pH=7,溶液中c(Na+)= c(H2PO4)+2c(HPO42)+3c(PO43)
D.滴加少量Na2CO3溶液,3Na2CO3+2H3PO4 =2Na3PO4+3H2O+3CO2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了确认乙酸、碳酸和硅酸的酸性强弱,有人设计用如图所示装置,一次实验达到目的(不能再选用其他酸性溶液)。

(1)锥形瓶内装有某种可溶性正盐固体(含有3种酸的酸根的其中一种),此固体为________,分液漏斗中所盛试剂是___。
(2)装置B中所盛试剂的名称是________,试剂的作用是__________。
(3)装置C中出现的现象是__________________。
(4)由实验可知三种酸的酸性大小顺序为________(用化学式表示)。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com