
【题目】如图所示三个烧瓶中分别装入含酚酞的0.01molL﹣1 CH3COONa溶液,并分别放置在盛有水的烧杯中,然后向烧杯①中加入生石灰,向烧杯③中加入NH4NO3晶体,烧杯②中不加任何物质. 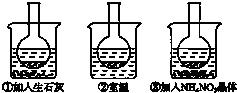
(1)含酚酞的0.01molL﹣1 CH3COONa溶液显浅红色的原因为
(2)实验过程中发现烧瓶①中溶液红色变深,烧瓶③中溶液红色变浅,则下列叙述正确的是 .
A.水解反应为放热反应
B.水解反应为吸热反应
C.NH4NO3溶于水时放出热量
D.NH4NO3溶于水时吸收热量
(3)向0.01molL﹣1 CH3COONa溶液中分别加入少量浓盐酸、NaOH固体、Na2CO3固体、FeSO4固体,使CH3COO﹣水解平衡移动的方向分别为、、、(填“左”“右”或“不移动”).
【答案】
(1)CH3COO﹣+H2OCH3COOH+OH﹣ , 使溶液呈碱性
(2)BD
(3)右;左;左;右
【解析】解:(1)CH3COONa为强碱弱酸盐,醋酸根离子水解而使溶液呈碱性,水解方程式为CH3COO﹣+H2OCH3COOH+OH﹣ , 故答案为:CH3COO﹣+H2OCH3COOH+OH﹣ , 使溶液显碱性;(2)CaO+H2O=Ca(OH)2 , 该反应是放热反应,所以会导致溶液温度升高,硝酸铵溶解过程吸收热量,会导致溶液温度降低,升高温度促进CH3COONa水解,降低温度抑制CH3COONa水解,所以CH3COONa水解反应为吸热反应,故答案为:BD;(3)CH3COO﹣+H2OCH3COOH+OH﹣ , 加入少量浓盐酸、FeSO4固体时,氢离子和亚铁离子都和氢氧根离子反应,所以促进水解,平衡向右移动,加入少量NaOH固体、Na2CO3固体,氢氧根离子浓度增大,抑制醋酸钠水解,平衡向逆反应方向移动,故答案为:右;左;左;右. (1)CH3COONa为强碱弱酸盐,醋酸根离子水解而使溶液呈碱性;(2)CaO和水反应是放热反应,所以会导致溶液温度升高,硝酸铵溶解过程吸收热量,会导致溶液温度降低,升高温度促进CH3COONa水解,降低温度抑制CH3COONa水解;(3)CH3COO﹣+H2OCH3COOH+OH﹣ , 加入和氢氧根离子反应的物质促进水解、加入含有氢氧根离子的物质抑制水解,据此分析解答.


科目:高中化学 来源: 题型:
【题目】氢气是人类未来最理想的燃料,以水为原料大量制取氢气的最理想的途径是( )
A. 利用太阳能直接使水分解产生氢气
B. 以焦炭和水制取水煤气(含CO和H2)后分离出氢气
C. 用铁和盐酸反应放出氢气
D. 由热电站提供电力电解水产生氢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2与Cl2的氧化性相近,在自来水消毒和果蔬保鲜等方面应用广泛.某兴趣小组通过题图1装置(夹持装置略)对其制备、吸收、释放和应用进行了研究.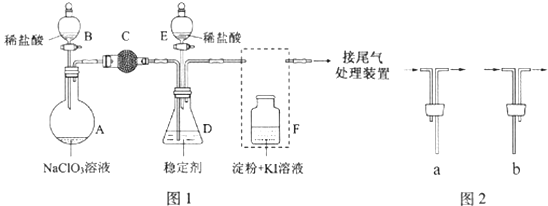
(1)仪器D的名称是 . 安装F中导管时,应选用图2中的 .
(2)打开B的活塞,A中发生反应:2NaClO3+4HCl═2ClO2↑+Cl2↑+2NaCl+2H2O.
为使ClO2在D中被稳定剂充分吸收,滴加稀盐酸的速度宜(填“快”或“慢”).
(3)关闭B的活塞,ClO2在D中被稳定剂完全吸收生成NaClO2 , 此时F中溶液的颜色不变,则装置C的作用是 .
(4)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2 , 该反应的离子方程式为 , 在ClO2释放实验中,打开E的活塞,D中发生反应,则装置F的作用是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电离平衡常数是衡量弱电解质电离程度强弱的量.已知如表数据.
化学式 | 电离平衡常数(25℃) |
HCN | K=4.9×10﹣10 |
CH3COOH | K=1.8×10﹣5 |
H2CO3 | K1=4.3×10﹣7、K2=5.6×10﹣11 |
(1)25℃时,有等浓度的NaCN溶液、Na2CO3溶液、CH3COONa溶液,三种溶液的pH由大到小的顺序为 .
(2)25℃时,pH=3的CH3COOH溶液和pH=11的NaOH溶液混合,若所得溶液显酸性,则c(Na+)c(CH3COO﹣)(填“>”、“<”或“=”).
(3)NaCN溶液中通入少量CO2 , 所发生反应的化学方程式为
(4)25℃时,pH=8的CH3COONa溶液中,c(Na+)﹣c(CH3COO﹣)= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据原子结构及元素周期律的知识,下列推断正确的是( )
A. 同主族元素含氧酸的酸性随核电荷数的增加而减弱
B. 核外电子排布相同的微粒化学性质也相同
C. 碱金属密度随核电荷数的增加逐渐增大
D. 3517Cl与3717Cl得电子能力相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将1.12g铁粉加入25mL 2mol/L的FeCl3溶液中,充分反应后,其结果是( )
A.铁粉有剩余,溶液呈浅绿色,Cl﹣基本保持不变
B.往溶液中滴入无色KSCN溶液,不显红色
C.Fe2+和Fe3+物质的量之比为6:1
D.氧化产物和还原产物的物质的量之比为2:5
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.1 mol任何气体所占体积都为22.4 L
B.1 mol H2O在标准状况下体积为22.4 L
C.1 mol气体体积为22.4 L,则一定是标准状况
D.气体摩尔体积不一定是22.4 L/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国清代《本草纲目拾遗》中记叙无机药物335种,其中“强水”条目下写道:“性最烈,能蚀五金……其水甚强,五金八石皆能穿第,惟玻璃可盛。”这里的“强水”是指
A. 氨水 B. 卤水 C. 醋 D. 硝酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com