
【题目】电离平衡常数是衡量弱电解质电离程度强弱的量.已知如表数据.
化学式 | 电离平衡常数(25℃) |
HCN | K=4.9×10﹣10 |
CH3COOH | K=1.8×10﹣5 |
H2CO3 | K1=4.3×10﹣7、K2=5.6×10﹣11 |
(1)25℃时,有等浓度的NaCN溶液、Na2CO3溶液、CH3COONa溶液,三种溶液的pH由大到小的顺序为 .
(2)25℃时,pH=3的CH3COOH溶液和pH=11的NaOH溶液混合,若所得溶液显酸性,则c(Na+)c(CH3COO﹣)(填“>”、“<”或“=”).
(3)NaCN溶液中通入少量CO2 , 所发生反应的化学方程式为
(4)25℃时,pH=8的CH3COONa溶液中,c(Na+)﹣c(CH3COO﹣)= .
【答案】
(1)Na2CO3溶液>NaCN溶液>CH3COONa溶液
(2)>
(3)NaCN+H2O+CO2=HCN+NaHCO3
(4)9.9×10﹣7mol/L
【解析】解:(1)依据图表数据分析,醋酸电离常数大于氰酸大于碳酸氢根离子,所以等浓度的NaCN溶液、Na2CO3溶液、CH3COONa溶液水解程度等浓度的Na2CO3溶液>NaCN溶液>CH3COONa溶液,溶液pH为Na2CO3溶液的>NaCN溶液的>CH3COONa溶液的; 故答案为:Na2CO3溶液>NaCN溶液>CH3COONa溶液;(2)等浓度的CH3COOH溶液和NaOH溶液等体积混合,所得溶液显碱性,c(H+)<c(OH﹣)依据溶液中电荷守恒c(H+)+c(Na+)=c(OH﹣)+c(CH3COO﹣),c(Na+)>c(CH3COO﹣);
故答案为:>;(3)向NaCN溶液中通入少量CO2 , H2CO3酸性大于HCN大于HCO3﹣ , 所以反应生成氰酸和碳酸氢钠,不能生成二氧化碳,反应的化学方程式为:NaCN+H2O+CO2=HCN+NaHCO3;
故答案为:NaCN+H2O+CO2=HCN+NaHCO3;(4)25℃时,pH=8的CH3COONa溶液中,c(H+)=10﹣8mol/L,c(OH﹣)= ![]() =10﹣6mol/L,溶液中存在电荷守恒:c(Na+)+c(H+)=c(CH3COO﹣)+c(OH﹣)
=10﹣6mol/L,溶液中存在电荷守恒:c(Na+)+c(H+)=c(CH3COO﹣)+c(OH﹣)
c(Na+)﹣c(CH3COO﹣)=c(OH﹣)﹣c(H+)=10﹣6mol/L﹣10﹣8mol/L=9.9×10﹣7 mol/L,
故答案为:9.9×10﹣7 mol/L.
(1)酸的电离常数意义分析判断,越易电离得算对应盐水解程度越小(2)溶液中电荷守恒计算分析;(3)电离常数大小分析反应生成产物,电离平衡常数比较可知酸性:H2CO3>HCN>HCO3﹣ , 所以反应生成氰酸和碳酸氢钠,;(4)电解质溶液中电荷守恒计算,PH=8溶液显碱性;


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】水的三态的熵值的大小关系正确的是( )
A.S(s)>S(l)>S(g)
B.S(l)>S(s)>S(g)
C.S(g)>S(l)>S(s)
D.S(g)>S(s)>S(l)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】完成下列各题:
(1)铜与浓硝酸可发生反应:Cu+4HNO3(浓)═Cu(NO3)2 +2NO2↑+2H2O,其中铜被(填“氧化”或“还原”),浓硝酸作(填“氧化”或“还原”)剂.在该反应中,若消耗了1mol Cu,则生成mol NO2
(2)3.01×1023个氯气分子的物质的量是;1.5 mol Na2SO410H2O中所含的Na+的物质的量是 , 所含的SO42﹣的物质的量是 , 所含H2O的数目是NA
(3)4种物质:①NH3、②SO2、③NaCl溶液、④H2SO4溶液.其中,能使品红溶液褪色的是(填序号,下同),焰色反应呈黄色的是,遇氯化氢有白烟产生的是 , 与氯化钡溶液反应产生白色沉淀的是
(4)某些铁、铝制品的表面常生成一层氧化物,其主要成分分别是氧化铁、氧化铝.请回答: a.两种氧化物均能与盐酸反应,生成的两种盐的化学式分别为、 . 向这两种盐的溶液中分别滴加足量氢氧化钠溶液,可观察到:其中一种溶液中的现象是先产生白色沉淀,然后白色沉淀逐渐消失;另一种溶液中的现象是(填序号).
①产生白色沉淀
②产生红褐色沉淀
③产生白色沉淀,迅速变成灰绿色,最后变成红褐色
b.铝与氧化铁的反应可用于焊接钢轨,其反应的化学方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下,现有①6.72 L CH4 ②3.01×1023个HCl分子 ③13.6 g H2S ④0.2 mol NH3,对这四种气体的关系有以下四种表述,其中不正确的是
A.体积:②>③>①>④ B.物质的量:②>③>④>①
C.质量:②>③>①>④ D.氢原子个数:①>③>④>②
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下有0.1molL﹣1四种溶液NaOH、NH3H2O、HCl、CH3COOH
(1)已知CH3COOH溶液的pH=3,其电离度为 , 由水电离的c(H+)=molL﹣1 .
(2)相同pH的CH3COOH溶液和HCl溶液加水稀释,其pH变化情况如图,其中表示HCl溶液的是曲线 , a、b两点中,导电能力更强的是 . 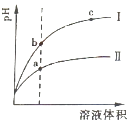
(3)NH3H2O溶液和HCl溶液混合,已知体积V(NH3H2O)>V(HCl),当溶液中c(NH3H2O)=c(NH4+)时,溶液的pH= . [已知:Kb(NH3H2O)=1.77×10﹣5 , lg 1.77=0.25].
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示三个烧瓶中分别装入含酚酞的0.01molL﹣1 CH3COONa溶液,并分别放置在盛有水的烧杯中,然后向烧杯①中加入生石灰,向烧杯③中加入NH4NO3晶体,烧杯②中不加任何物质. 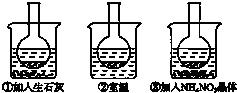
(1)含酚酞的0.01molL﹣1 CH3COONa溶液显浅红色的原因为
(2)实验过程中发现烧瓶①中溶液红色变深,烧瓶③中溶液红色变浅,则下列叙述正确的是 .
A.水解反应为放热反应
B.水解反应为吸热反应
C.NH4NO3溶于水时放出热量
D.NH4NO3溶于水时吸收热量
(3)向0.01molL﹣1 CH3COONa溶液中分别加入少量浓盐酸、NaOH固体、Na2CO3固体、FeSO4固体,使CH3COO﹣水解平衡移动的方向分别为、、、(填“左”“右”或“不移动”).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将物质X逐渐加入(或滴入)Y溶液中,其生成沉淀的量与加入X的物质的量关系如下图所示,符合图示情况的是( )
A | B | C | D | |
X | CO2 | HCl | NaOH | AlCl3 |
Y | Ca(OH)2 | NaAlO2 | AlCl3 | NaOH |
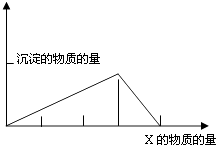
A.A
B.B
C.C
D.D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由废铜制硝酸铜.用胶头滴管吸取浓HNO3缓慢加到锥形瓶内的废铜屑中(废铜屑过量),充分反应后过滤,得到硝酸铜溶液.
(1)写出浓硝酸与铜反应的离子方程式: .
(2)如图装置中NaOH溶液的作用是 . 反应结束后,广口瓶内的溶液中,除了含有NaOH外,还有(填化学式).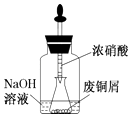
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com