
【题目】标准状况下,现有①6.72 L CH4 ②3.01×1023个HCl分子 ③13.6 g H2S ④0.2 mol NH3,对这四种气体的关系有以下四种表述,其中不正确的是
A.体积:②>③>①>④ B.物质的量:②>③>④>①
C.质量:②>③>①>④ D.氢原子个数:①>③>④>②
 初中暑期衔接系列答案
初中暑期衔接系列答案科目:高中化学 来源: 题型:
【题目】钢铁工业对促进经济和社会发展起了重要作用。
(1)炼铁高炉分为五部分,铁矿石与高温煤气主要在部分发生反应,在部分开始生成生铁和炉渣。
(2)炼钢时,除磷的化学方程式为;加入硅、锰和铝的目的是。
(3)不锈钢含有的Cr元素是在炼钢过程的氧吹(填“前”或“后”)加入,原因是。
(4)炼铁和炼钢生产中,尾气中均含有的主要污染物是。从环保和经济角度考虑,上述尾气经处理可用作。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有A、B、C三种不溶于水的固体。A是某元素的一种单质,它在氧气中完全燃烧得到一种无色气体,此气体能使澄清的石灰水变浑浊,另外测得这种气体密度为同温、同压下的氧气密度的1.375倍。B固体能溶于热苛性钠溶液,再往所得的溶液中加入过量盐酸时,析出白色胶状沉淀。此沉淀干燥后,成为不溶于水的白色粉末,这是一种比碳酸酸性还弱的酸。将B与石灰石、纯碱按比例混合加热后能得到C,C在高温时软化,无固定熔点。
根据以上事实,判断A为元素的单质,B的化学式为 , C物质为。
写出生成C的有关反应的化学方程式。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】从海水中提取金属镁的生产步骤有:①浓缩结晶 ②加熟石灰③加盐酸 ④过滤 ⑤熔融电解,正确的生产顺序是( )
A.①②③④⑤
B.⑤④③①②
C.②④③①⑤
D.③④②①⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】ClO2与Cl2的氧化性相近,在自来水消毒和果蔬保鲜等方面应用广泛.某兴趣小组通过题图1装置(夹持装置略)对其制备、吸收、释放和应用进行了研究.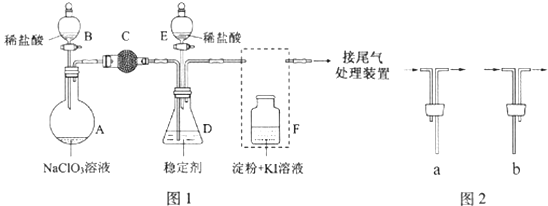
(1)仪器D的名称是 . 安装F中导管时,应选用图2中的 .
(2)打开B的活塞,A中发生反应:2NaClO3+4HCl═2ClO2↑+Cl2↑+2NaCl+2H2O.
为使ClO2在D中被稳定剂充分吸收,滴加稀盐酸的速度宜(填“快”或“慢”).
(3)关闭B的活塞,ClO2在D中被稳定剂完全吸收生成NaClO2 , 此时F中溶液的颜色不变,则装置C的作用是 .
(4)已知在酸性条件下NaClO2可发生反应生成NaCl并释放出ClO2 , 该反应的离子方程式为 , 在ClO2释放实验中,打开E的活塞,D中发生反应,则装置F的作用是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】处理生活污水中的NH4+ , 过程如下: 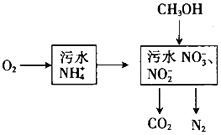
(1)空气将NH4+转变为NO3﹣或NO2﹣ , 溶液pH(填“增大”、“减小”或“不变”).
(2)根据较新的研究表明,将只含NO2﹣的污水与含NH4+的污水按比例混合,直接转化为无毒气体,该气体为 . 此方法的优点是
(3)完全处理含1mol NH4+污水,则n(O2)与n(CH3OH)关系式为[以n(O2)与n(CH3OH)表示].
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电离平衡常数是衡量弱电解质电离程度强弱的量.已知如表数据.
化学式 | 电离平衡常数(25℃) |
HCN | K=4.9×10﹣10 |
CH3COOH | K=1.8×10﹣5 |
H2CO3 | K1=4.3×10﹣7、K2=5.6×10﹣11 |
(1)25℃时,有等浓度的NaCN溶液、Na2CO3溶液、CH3COONa溶液,三种溶液的pH由大到小的顺序为 .
(2)25℃时,pH=3的CH3COOH溶液和pH=11的NaOH溶液混合,若所得溶液显酸性,则c(Na+)c(CH3COO﹣)(填“>”、“<”或“=”).
(3)NaCN溶液中通入少量CO2 , 所发生反应的化学方程式为
(4)25℃时,pH=8的CH3COONa溶液中,c(Na+)﹣c(CH3COO﹣)= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据原子结构及元素周期律的知识,下列推断正确的是( )
A. 同主族元素含氧酸的酸性随核电荷数的增加而减弱
B. 核外电子排布相同的微粒化学性质也相同
C. 碱金属密度随核电荷数的增加逐渐增大
D. 3517Cl与3717Cl得电子能力相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氧化还原反应与四种基本反应类型的关系如图所示,则下列反应属于丙区域的是( ) 
A.Cl2+2KBr═Br2+2KCl
B.2NaHCO3 ![]() Na2CO3+H2O+CO2↑
Na2CO3+H2O+CO2↑
C.3Mg+N2 ![]() Mg3N2
Mg3N2
D.2Na2O2+2CO2═2Na2CO3+O2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com