
【题目】一定温度下,在三个体积均为2.0L的恒容密闭容器中发生如下反应:PCl5(g)═PCl3(g)+Cl2(g)
编号 | 温度(℃) | 起始物质的量 | 平衡物质的量 | 达到平衡所需时间 | |
PCl5(g) | PCl3(g) | Cl2(g) | |||
Ⅰ | 320 | 0.40 | 0.10 | 0.10 | t1 |
Ⅱ | 320 | 0.80 | t2 | ||
Ⅲ | 410 | 0.40 | 0.15 | 0.15 | t3 |
下列说法正确的是( )
A.平衡常数K:容器Ⅱ>容器Ⅲ
B.反应到达平衡时,PCl5的转化率:容器Ⅱ>容器Ⅰ
C.反应到达平衡时,容器I中的平均速率为v(PCl5)=0.1/t1 mol/(Ls)
D.起始时向容器Ⅲ中充入PCl5 0.30 mol、PCl30.45 mol和Cl20.10 mol,则反应将向逆反应方向进行
【答案】D
【解析】A.I、Ⅱ温度相同,则二者平衡常数相等,Ⅲ比I相比温度升高,平衡时Ⅲ中PCl3比I中的大,说明升高温度平衡正向移动,平衡常数增大,故平衡常数K:容器Ⅱ<容器Ⅲ,A不符合题意;
B.恒温恒容下,Ⅱ等效在I中平衡基础上压强增大一倍,平衡逆向移动,转化率减小,PCl5的转化率:容器Ⅱ<容器Ⅰ,B不符合题意;
C.速率之比等于化学计量数之比,则v(PCl5)=v(PCl3)= ![]() =
= ![]() =
= ![]() mol/(Ls),C不符合题意;
mol/(Ls),C不符合题意;
D.410℃平衡时PCl5为0.4mol﹣0.15mol=0.25mol,该温度下平衡常数K= ![]() =
=  =0.045,浓度商Qc=
=0.045,浓度商Qc= ![]() =0.075>K=0.045,反应向逆反应进行,D符合题意;
=0.075>K=0.045,反应向逆反应进行,D符合题意;
故答案为:D
A.平衡常数与温度有关,需考虑温度对平衡移动的影响,确定平衡常数的大小;
B.Ⅰ、Ⅱ为恒温恒容装置,容器Ⅱ等效于在容器Ⅰ的平衡基础上增大一倍压强,结合压强对平衡移动的影响分析;
C.根据速率之比等于化学计量系数之比进行计算即可;
D.根据题干信息确定容器Ⅲ反应的平衡常数,与选项中的浓度商比较,确定反应进行的方向。


 寒假学与练系列答案
寒假学与练系列答案科目:高中化学 来源: 题型:
【题目】某固体混合物可能由NaCl、NaI、NH4Cl、Na2CO3、Na2SO3、Na2SO4中的一种或几种组成,准确称取4.7g该固体混合物进行如下实验(所加试剂均足量,气体体积已折算成标准状况下) :
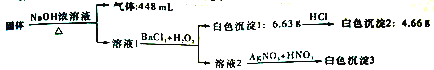
根据实验结果,下列有关说法不正确的是
A. 原固体混合物中是否含有NaCl无法确定
B. 若溶液1中只加BaCl2,则生成白色沉淀的质量必小于6.63 g
C. 原固体混合物中必含有NH4Cl、Na2CO3、Na2SO3
D. 测定出“白色沉淀3”的质量可以确定原固体混合物的组成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】黄铜矿(CuFeS2)是制取铜及其化合物的主要原料之一,还可制备硫及铁的化合物.冶炼铜的反应为8CuFeS2+21O2![]() 8Cu+4FeO+2Fe2O3+16SO2.
8Cu+4FeO+2Fe2O3+16SO2.
(1)若CuFeS2中Fe的化合价为+2,反应中被还原的元素是__(填元素符号).
(2)用稀H2SO4浸泡上述反应制取铜后剩余的固体残渣,取少量所得溶液,检验溶液中存在Fe3+的方法是__(注明试剂、现象).
(3)上述冶炼过程产生大量SO2.下列处理方案中合理的是__(填代号)
a.高空排放 b.用于制备硫酸 c.用纯碱溶液吸收制Na2SO3 d.用浓硫酸吸收
(4)验证黄铜矿冶炼铜的反应后气体中含有SO2的方法是__.
(5)实验室制备,收集干燥的SO2,所需仪器如下.
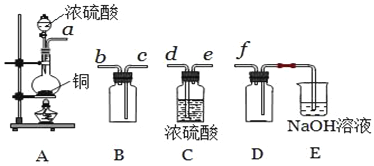
①其中装置A产生SO2,反应的化学方程式为__.
②请按气流方向连接各仪器接口,顺序为a→__→ → → f,装置E中NaOH溶液的作用是__.E中反应的离子方程式__.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在2 L密闭容器中进行反应:mX(g)+nY(g)![]() pZ(g)+qQ(g),式中m、n、p、q为化学计量数。在0~3 min内,各物质物质的量的变化如下表所示:
pZ(g)+qQ(g),式中m、n、p、q为化学计量数。在0~3 min内,各物质物质的量的变化如下表所示:

已知2 min内v(Q)=0.075 mol·L-1·min-1,v(Z)∶v(Y)=1∶2。
(1)试确定:起始时n(Y)=________,n(Q)=________。
(2)方程式中m=________,n=________,p=________,q=________。
(3)用Z表示2 min内的反应速率________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】温度为T时,向V L的密闭容器中充入一定量的A和B,发生反应:A(g)+B(g)C(s)+xD(g)△H>0,容器中A、B、D的物质的量浓度随时间的变化如图所示,下列说法不正确的是( )
A.反应在前10min的平均反应速率v(B)=0.15mol/(Lmin)
B.该反应的平衡常数表达式K= ![]()
C.若平衡时保持温度不变,压缩容器体积平衡向逆反应方向移动
D.反应至15min时,改变的反应条件是降低温度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定条件下可实现下图所示物质之间的转化:
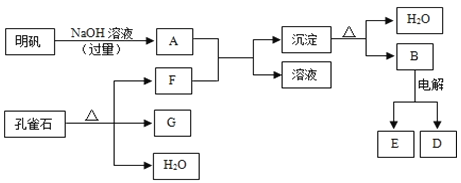
注意:①明矾(KAl(SO4)2·12H2O),可以电离出K+,Al3+,SO42-
②G是黑色固体,D是金属单质,E是常见的双原子气体分子
请填写下列空白:
(1)孔雀石的主要成分是CuCO3·Cu(OH)2(碱式碳酸铜),受热易分解,图中的F是______(填化学式)。
(2)写出明矾溶液与过量NaOH溶液反应的离子方程式:________________。
(3)写出B电解生成E和D的反应方程式:________________。
(4)图中所得G和D都为固体,混合后在高温下可发生反应,写出该反应的化学方程式______,该反应消耗了2 molG,则转移的电子数是____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知可逆反应X(g)+Y(g)Z(g)(未配平).温度为T0时,在容积固定的容器中发生反应各物质的浓度随时间变化的关系如图a所示.其他条件相同,温度分别为T1、T2时发生反应,Z的浓度随时间变化的关系如图b所示.下列叙述正确的是( )
A.发生反应时,各物质的反应速率大小关系为:v(X)=v(Y)=2v(Z)
B.图a中反应达到平衡时,Y的转化率为37.5%
C.T0℃时,该反应的平衡常数为33.3
D.该反应正反应的反应热△H<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某实验室采用新型合成技术,以Cu(CH3COO)·2H2O和K2C2O4·H2O为原料在玛瑙研钵中研磨反应,经过后处理得到蓝色晶体。已知该蓝色晶体的化学式为Ka[Cub(C2O4)c]·nH2O,在合成过程中各种元素的化合价均不发生变化。为了测定其组成进行以下两组实验,请回答相关问题:
Ⅰ.草酸根与铜含量的测定
①将蓝色晶体于研钵中研碎,取该固体粉末,加入1mol/L的H2SO4溶解,配制成250mL溶液。
②配制100mL0.1000mol/LKMnO4溶液备用。
③取所配溶液25.00mL于锥形瓶中,采用0.1000mol/LKMnO4溶液滴定至草酸根恰好全部氧化成二氧化碳,共消耗KMnO4溶液20.00mL。
④另取所配溶液25.00mL于锥形瓶中,加入过量KI溶液,充分反应后用0.2000mol/LNa2S2O3溶液滴定,消耗12.50mL.(发生反应:2Cu2++4I-=2CuI↓+I2,2Na2S2O3+I2=Na2S4O6 + 2NaI)
(1)后处理提纯该蓝色晶体时,除掉的杂质的主要成分 (除原料外)是_______(填化学式)
(2)配制0.1000mol/LKMnO4溶液,需要的玻璃仪器有________、_______,胶头滴管,玻璃棒,烧杯。
(3)用Na2S2O3滴定时,应选用_______滴定管(填“酸式”或“碱式”)
(4)KMnO4溶液滴定草酸根过程中发生反应的离子方程式为_______,滴定终点的现象为_____。
Ⅱ.热重分析法测定结晶的含量
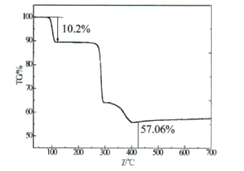
氮气气氛中以升温速率10℃/min测定该化合物的热失重曲线,如图所示晶体在107℃失重10.2%,失去全部结晶水。
(5)通过热失重分析,蓝色晶体的化学式中n=________,经过实验测定后,蓝色晶体的化学式为________.
(6)加热400℃之后,剩余物质的质量不再发生变化。为探究剩余固体的成分,冷却后取少量固体于试管中,加水溶解有红色不溶物,过滤后向滤液中加入稀盐酸产生无色无味气体。则剩余固体的成分为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应是吸热反应的是( )
A.C+CO2 ![]() 2CO
2CO
B.Fe+H2SO4═FeSO4+H2↑
C.2Al+Fe2O3 ![]() 2Fe+Al2O3
2Fe+Al2O3
D.2Na2O2+2H2O═4NaOH+O2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com