
【题目】根据元素周期律,卤族元素的下列性质从上到下依次递减的有( )
A.非金属性
B.原子半径
C.单质的氧化性
D.氢化物的稳定性
科目:高中化学 来源: 题型:
【题目】下列各物质的转化关系如下图所示.B、D是气体,其中B是空气的主要成分之一;C是淡黄色固体,常用于供氧剂;E是红棕色固体;F是最常见的无色液体.

回答下列问题:
(1)C的化学式是_______________.
(2)气体D通入紫色石蕊溶液的现象是_____________________.
(3)写出反应①的离子方程式______________________________________.
(4)写出反应②的化学方程式_____________________________________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化工原料红矾钠(重铬酸钠:Na2Cr2O72H2O)主要是以铬铁矿(主要成分为FeOCr2O3 , 还含有Al2O3、SiO2等杂质)为主要原料生产,其主要工艺流程如下: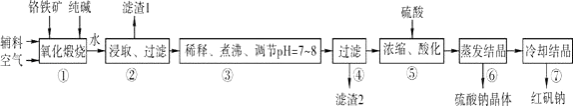
步骤①中主要反应的化学方程式如下:
4FeOCr2O3+8Na2CO3+7O2═8Na2CrO4+2Fe2O3+8CO2
(1)①中反应是在回转窑中进行的,反应时需不断搅拌,其作用是 .
(2)杂质Al2O3在①中转化的化学反应方程式为 .
(3)用化学平衡移动原理说明③中煮沸的作用是(用离子方程式结合文字说明),若调节pH过低产生的影响是 .
(4)⑤中酸化是使CrO42﹣转化为Cr2O72﹣写出该反应的离子方程式: . 
(5)工业上还可用电解法制备重铬酸钠,其装置示意图如上.阴极的电极反应式为;
阳极的电极反应式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列离子方程式书写正确的( )
A.钠与水的反应:2Na+2H2O═2Na++2OH﹣+H2↑
B.硅酸钠溶液中通入过量CO2:SiO ![]() +2CO2+2H2O═H2SiO3↓+2HCO3﹣
+2CO2+2H2O═H2SiO3↓+2HCO3﹣
C.氯气与水反应:Cl2+H2O═2H++Cl﹣+ClO﹣
D.明矾溶液中加入过量的Ba(OH)2溶液:Al3++4OH﹣═AlO2﹣+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乳酸亚铁{[CH3CH(OH)COO]2Fe·3H2O,Mr=288}是一种常用的补铁剂,可通过乳酸与碳酸亚铁反应制得:CH3CH(OH)COOH+FeCO3+2H2O―→[CH3CH(OH)COO]2Fe·3H2O+CO2↑。
已知FeCO3易被氧化:4FeCO3+6H2O+O2===4Fe(OH)3+4CO2。
某兴趣小组用FeCl2(用铁粉和稀盐酸制得)和NH4HCO3制备FeCO3的装置示意图如下:

回答下列问题:
(1)NH4HCO3盛放在装置______________中(填字母),该装置中涉及的主要反应的离子方程式为____________________________________________________________________。
(2)将生成的FeCl2溶液和NH4HCO3溶液混合时的操作是__________________________。
(3)将制得的FeCO3加入到足量乳酸溶液中,再加入少量铁粉,75 ℃下搅拌反应。铁粉的作用是__________________________________ 。反应结束后,无需过滤,除去过量铁粉的方法是________________________________。
(4)该兴趣小组用KMnO4法测定样品中亚铁含量进而计算产品中乳酸亚铁的质量分数,发现产品的质量分数总是大于100%,其原因可能是_____________________________________。经查阅文献后,该兴趣小组改用铈(Ce)量法测定产品中Fe2+的含量。取2.880 g产品配成100 mL溶液,每次取20.00 mL进行必要处理,用0.100 0 mol·L-1Ce(SO4)2标准溶液滴定至终点,平均消耗Ce(SO4)2 19.70 mL。滴定反应如下:Ce4++Fe2+===Ce3++Fe3+,则产品中乳酸亚铁的质量分数为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据下表部分短周期元素信息,判断以下叙述正确的是( )

A. 氢化物的沸点为H2T<H2R B. 单质与稀盐酸反应的剧烈程度L<Q
C. M与T形成的化合物具有两性 D. L2+与R2﹣的核外电子数相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国宋代的药物著作《开宝本草》中记载了有关中药材----铁华粉的制法为:取钢煅作叶,令表光净、以盐水洒之并置于浓醋瓮中,阴处埋之百日,则铁上生衣,铁华成矣。由此判断铁华粉是指( )
A.铁粉B.醋酸亚铁C.食盐D.氢氧化铁
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com