
【题目】氮氧化物是大气主要污染物,主要来自于工业废气及汽车尾气的排放,工业废气中NO是主要成分之一。
(1)乙烯作为还原剂的脱硝(NO),其反应机理示意图如图所示.写出解吸过程的化学方程式____________________。

(2)FeSO4-Na2SO3复合吸收剂吸收烟气中的NO,该方法利用Fe2+易与NO发生络合反应的特性,原理如下NO+FeSO4![]() Fe(NO)SO4
Fe(NO)SO4
①如图是一段时间内不同吸收剂对NO脱除率对比,加入Na2SO3溶液后,吸收效率增强,除了Na2SO3也能吸收部分NO外,还能防氧化从而增大Fe2+的含量,写出此原理的离子方程式_______________________________________。

②模拟实验表明,温度过高或过低都会降低NO的脱除率,其原因是_______________________________________。
(3)采用无隔膜法电解食盐水脱氮可将氮氧化物转化成NO3-,原理如图

①无隔膜条件下电解食盐水后溶液呈弱碱性,原因是____________________________.
②写出NO发生反应的离子方程式____________________________。
③根据下图所示,脱NO过程中控制溶液pH在______________范围内更合理。

【答案】2C2H4+6NO2![]() 4CO2+3N2+4H2O 2Fe3++SO32-+H2O=2Fe3++SO42-+2H+ 温度过低,反应速率缓慢;温度过高,NO的溶解度降低,都会造成脱除率下降 ClO-+H2O
4CO2+3N2+4H2O 2Fe3++SO32-+H2O=2Fe3++SO42-+2H+ 温度过低,反应速率缓慢;温度过高,NO的溶解度降低,都会造成脱除率下降 ClO-+H2O![]() HClO+OH- 2NO+3ClO-+2OH-
HClO+OH- 2NO+3ClO-+2OH-![]() 2NO3-+3Cl-+2H2O 5—6
2NO3-+3Cl-+2H2O 5—6
【解析】
(1)反应机理示意图如图所示,解吸过程反应物为C2H4,NO2生成物为CO2、N2、H2O ,写出对应化学方程式;
(2)①Na2SO3具有还原性,Fe3+具有氧化性,两者发生氧化还原反应,能防Fe2+氧化从而增大Fe2+的含量;
②温度过低,反应速率缓慢,温度过高,NO的溶解度降低;
(3)①电解食盐水,阳极失去电子,反生为2Cl--2e-=Cl2↑,阴极得到电子,反生的反应为2H2O+2e-=2OH-+H2↑,总反应方程式为Cl-+ H2O= ClO-+H2↑,ClO-会水解;
②ClO-作氧化剂,NO为还原剂,在碱性条件下的反应为2NO+3ClO-+2OH-![]() 2NO3-+3Cl-+2H2O;
2NO3-+3Cl-+2H2O;
③根据图分析,当pH介于5-6时,Cl元素以HClO存在,此时氧化性最强。
(1)反应机理示意图如图所示,解吸过程反应物为C2H4,NO2生成物为CO2、N2、H2O ,化学方程式为2C2H4+6NO2![]() 4CO2+3N2+4H2O,故答案为:2C2H4+6NO2
4CO2+3N2+4H2O,故答案为:2C2H4+6NO2![]() 4CO2+3N2+4H2O;
4CO2+3N2+4H2O;
(2) ①Na2SO3具有还原性,Fe3+具有氧化性,两者发生氧化还原反应,能防Fe2+氧化从而增大Fe2+的含量,离子方程式为2Fe3++SO32-+H2O=2Fe3++SO42-+2H+,故答案为:2Fe3++SO32-+H2O=2Fe3++SO42-+2H+;
②温度过低,反应速率缓慢,温度过高,NO的溶解度降低,故答案为:温度过低,反应速率缓慢;温度过高,NO的溶解度降低,都会造成脱除率下降;
(3)①电解食盐水,阳极失去电子,反生为2Cl--2e-=Cl2↑,阴极得到电子,反生的反应为2H2O+2e-=2OH-+H2↑,总反应方程式为Cl-+ H2O= ClO-+H2↑,ClO-会发生水解,方程式为ClO-+H2O![]() HClO+OH-,故答案为:ClO-+H2O
HClO+OH-,故答案为:ClO-+H2O![]() HClO+OH-;
HClO+OH-;
②ClO-作氧化剂,NO为还原剂,在碱性条件下的反应为2NO+3ClO-+2OH-![]() 2NO3-+3Cl-+2H2O,故答案为:2NO+3ClO-+2OH-
2NO3-+3Cl-+2H2O,故答案为:2NO+3ClO-+2OH-![]() 2NO3-+3Cl-+2H2O;
2NO3-+3Cl-+2H2O;
③根据图分析,当pH介于5-6时,Cl元素以HClO存在,此时氧化性最强,故答案为5-6。


科目:高中化学 来源: 题型:
【题目】在室温下,下列五种溶液:
①0.1 mol·L-1 NH4Cl ②0.1 mol·L-1 CH3COONH4 ③0.1 mol·L-1 NH4HSO4 ④0.1 mol·L-1 NH3·H2O和0.1 mol·L-1 NH4Cl混合液 ⑤0.1 mol·L-1 NH3·H2O
请根据要求填写下列空白:
(1)溶液①呈___(填“酸”“碱”或“中”)性,其原因是____________(用离子方程式表示)。
(2)比较溶液②③中c (NH4+)②____________③(填“>”、“<”或“=”)
(3)在溶液④中,___的浓度为0.1 mol·L-1(填选项);NH3·H2O和_____离子的浓度之和为0.2 mol·L-1。(填选项)
A .c (NH4+) B. c (Cl-)
(4)室温下,测得溶液②的pH=7,则说明CH3COO-的水解程度___NH4+的水解程度,(填“>”“<”或“=”),c(CH3COO-)_____ c(NH4+) (填“>”“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
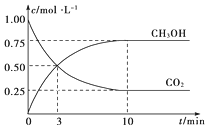
【题目】已知:CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1。一定条件下,向体积为1 L的密闭容器中充入1 mol CO2和3 mol H2,测得CO2和CH3OH(g)的浓度随时间的变化曲线如图所示。下列叙述中正确的是( )
CH3OH(g)+H2O(g) ΔH=-49.0 kJ·mol-1。一定条件下,向体积为1 L的密闭容器中充入1 mol CO2和3 mol H2,测得CO2和CH3OH(g)的浓度随时间的变化曲线如图所示。下列叙述中正确的是( )
A.欲增大平衡状态时![]() 的比值,可采用升高温度的方法
的比值,可采用升高温度的方法
B.3 min时,CO2的消耗速率等于CH3OH的生成速率,且二者浓度相同
C.欲提高H2的平衡转化率只能加压减小反应容器的体积
D.从反应开始到平衡,H2的平均反应速率v(H2)=0.075 mol·L-1·min-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿魏酸是传统中药当归、川穹的有效成分之一,工业上合成阿魏酸的原理如下,下列说法不正确的是
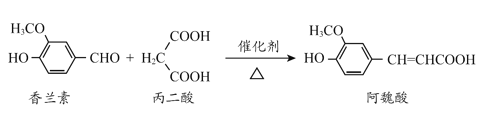 +H2O+CO2
+H2O+CO2
A.阿魏酸分子式为C10H10O4
B.阿魏酸存在顺反异构
C.方程式中三种有机物均可与NaOH、Na2CO3反应
D.可用酸性KMnO4溶液检测上述反应是否有阿魏酸生成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是( )
A. 所有的原子都含有质子、中子和电子三种基本构成微粒
B. 宇宙大爆炸产生了氢、氦、锂元素
C. ![]() 左图的原子模型是玻尔提出的
左图的原子模型是玻尔提出的
D.  模型中的小黑点表示电子在原子核外出现的概率密度的形象描述
模型中的小黑点表示电子在原子核外出现的概率密度的形象描述
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】莽草酸可用于合成药物达菲,其结构简式如图,下列关于莽草酸的说法正确的是

A.分子式为C7H6O5
B.分子中含有2种官能团
C.可发生加成和取代反应
D.在水溶液羧基和羟基均能电离出H+
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列解释事实的离子方程式正确的是
A. 明矾做净水剂:Al3++ 3H2O = Al (OH)3↓+ 3H+
B. 小苏打治疗胃酸过多:CO32-+ 2H+= CO2↑+ H2O
C. 漂白液加白醋,提高漂白效率:CH3COOH + ClO-=HClO + CH3COO-
D. 酸化的淀粉碘化钾溶液在空气中放置一段时间变蓝:4I-+ O2+2H2O= 2I2+ 4OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
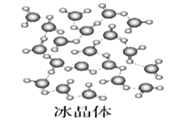
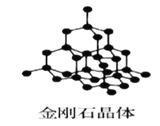
【题目】Ⅰ下图为几种晶体或晶胞的示意图:
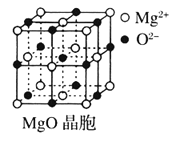
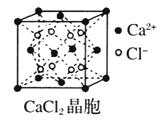

请回答下列问题:
(1)上述晶体中,粒子之间仅以共价键结合形成的晶体是____________。
(2)冰、金刚石、![]() 、
、![]() 、干冰5种晶体的熔点由高到低的顺序为_________________。
、干冰5种晶体的熔点由高到低的顺序为_________________。
(3)![]() 晶胞与
晶胞与![]() 晶胞相同,
晶胞相同,![]() 晶体的晶格能______(填“大于”或“小于”)
晶体的晶格能______(填“大于”或“小于”)![]() 晶体,原因是_________________。
晶体,原因是_________________。
(4)![]() 晶体中
晶体中![]() 的配位数为____________。
的配位数为____________。
(5)冰的熔点远高于干冰,除![]() 是极性分子、
是极性分子、![]() 是非极性分子外,还有一个重要的原因是__________________。
是非极性分子外,还有一个重要的原因是__________________。
Ⅱ(1)原子坐标参数可表示晶胞内部各原子的相对位置,金属钾是体心立方晶系,其构型如图。其中原子坐标参数![]() 、
、![]() ,则
,则![]() 原子的坐标参数为________________。
原子的坐标参数为________________。
(2)钾晶体的晶胞参数为![]() 。假定金属钾原子为等径的刚性小球且处于体对角线上的三个球相切,则钾原子的半径为_____
。假定金属钾原子为等径的刚性小球且处于体对角线上的三个球相切,则钾原子的半径为_____![]() ,晶体钾的密度计算式是_____
,晶体钾的密度计算式是_____![]() 。
。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向1L0.1 molL—l 一元酸HR溶液中逐渐通入氨气[已知常温下NH3 H2O电离平衡常数K = l .76x 10-5], 使溶液温度和体积保持不变, 混合溶液的pH与离子浓度变化的关系如图所示。下列叙述正确的是
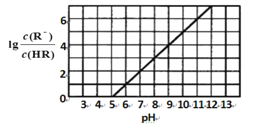
A.0. l molL—1HR 溶液的pH为5
B.HR为弱酸,常温时随着氨气的通入,c(R—)/[c(OH—).c(HR)] 逐渐增大
C.当通入0.1 mol NH3时,c(NH4+ > c(R—)
D.当c(R— )=c(HR)时 溶液必为中性
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com