
【题目】设NA为阿伏加德罗常数的值,下列说法正确的是( )
A.含0.2 mol H2SO4的浓硫酸和足量的铜反应,转移电子数为0.2NA
B.25 ℃时,1 L pH=13的Ba(OH)2溶液中由水电离产生的OH-的数目为0.1NA
C.15 g HCHO中含有1.5NA对共用电子对
D.常温常压下,22.4 L甲烷气体中含有的氢原子数目小于4NA
【答案】D
【解析】
A. 铜在一定条件下与浓硫酸反应Cu+2H2SO4(浓)![]() CuSO4+SO2↑+2H2O,与稀硫酸不反应,含0.2 molH2SO4的浓硫酸和足量的铜反应,并不能完全反应,所以转移电子数一定小于0.2NA,A项错误;
CuSO4+SO2↑+2H2O,与稀硫酸不反应,含0.2 molH2SO4的浓硫酸和足量的铜反应,并不能完全反应,所以转移电子数一定小于0.2NA,A项错误;
B. 25 ℃时,1 L pH=13的Ba(OH)2溶液中由水电离产生的OH-的浓度为10-13mol/L,则1L该溶液中由水电离产生的OH-的数目为1×10-13NA,B项错误;
C. 一个HCHO分子中含有2个碳氢单键和一个碳氧双键,即4对共用电子对,15 g HCHO物质的量为0.5mol,因此15 gHCHO含有0.5mol×4=2mol共用电子对,即2NA对共用电子对,C项错误;
D. 常温常压下,气体摩尔体积大于22.4L/mol,则22.4 L甲烷气体的物质的量小于1 mol,因此含有的氢原子数目小于4NA,D项正确;
答案选D。


 计算高手系列答案
计算高手系列答案科目:高中化学 来源: 题型:
【题目】一定条件下某容器中各微粒在反应前后的变化如图所示,其中●和代表不同元素的原子。关于此反应说法错误的是
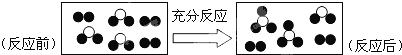
A.一定属于化合反应
B.一定属于可逆反应
C.一定属于吸热反应
D.一定属于氧化还原反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室用标准盐酸溶液测定某NaOH溶液的浓度,用甲基橙作指示剂,下列操作中可能使测定结果偏低的是( )
A.酸式滴定管在装酸液前未用标准盐酸溶液润洗2~3次
B.开始实验时酸式滴定管尖嘴部分有气泡,在滴定过程中气泡消失
C.锥形瓶内溶液颜色变化由黄色变橙色,立即记下滴定管液面所在刻度
D.盛NaOH溶液的锥形瓶滴定前用NaOH溶液润洗2~3次
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有如下物质:
①明矾 ②一水合氨 ③碳酸氢钠 ④硫酸铁 ⑤硝酸钡 ⑥硝酸
请完成下列问题:
(1)属于弱电解质的是___________________;(选填编号)
(2)由于促进水的电离平衡而使溶液显酸性的是__________________;(选填编号)
(3)它们水溶液PH >7的有_________________;(选填编号)
(4)写出下列物质之间发生反应的离子方程式:
①+⑤__________________ ②+④___________________ ③+⑥__________________
(5)明矾溶于水后能净水,是由于Al3+水解后能形成Al(OH)3胶体,该胶体具有吸附性,请写出Al3+水解的方程式:____________________;
硫酸铁溶液水解可以得到一系列具有净水作用的碱式硫酸铁(xFe2O3ySO3zH2O),为测定某碱式硫酸铁的组成,取5.130g样品溶于足量盐酸中,然后加入过量的BaCl2溶液,经过滤、洗涤、干燥得白色固体5.825g,向上述滤液中加入过量的NaOH溶液,经过滤、洗涤、灼烧得到固体1.600g,该样品的化学式中x、y、z的值分别为_______________(填整数)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度下,在2L的密闭容器中,加入1molX(g)和2molY(g)发生反应:X(g)+m Y(g)![]() 3Z(g),平衡时,X、Y、Z的体积分数分别为30%、60%、10%。在此平衡体系中加入1molZ(g),再次达到平衡后,X、Y、Z的体积分数不变。下列叙述不正确的是
3Z(g),平衡时,X、Y、Z的体积分数分别为30%、60%、10%。在此平衡体系中加入1molZ(g),再次达到平衡后,X、Y、Z的体积分数不变。下列叙述不正确的是
A. m=2
B. 两次平衡的平衡常数相同
C. X与Y的平衡转化率之比为1:1
D. 第二次平衡时,Z的浓度为0.4 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在普通铝中加入少量Cu和Mg后,形成一种称为拉维斯相的MgCu2微小晶粒,其分散在Al中可使得铝材的硬度增加、延展性减小,形成所谓“坚铝”,是制造飞机的主要村料。回答下列问题:
(1)下列状态的镁中,电离最外层一个电子所需能量最大的是______________。
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
(2)乙二胺(H2NCH2CH2NH2)是一种有机化合物,分子中氮、碳的杂化类型分别是_________、_________。乙二胺能与Mg2+、Cu2+等金属离子形成稳定环状离子,其中与乙二胺形成的化合物稳定性相对较高的是____________(填“Mg2+”或“Cu2+”)。
(3)一些氧化物的熔点如表所示:
氧化物 | Li2O | MgO | P4O6 | SO2 |
熔点/°C | 1570 | 2800 | 23.8 | 75.5 |
解释MgO熔点比P4O6熔点高得多的原因______________
(4)金刚石的晶胞如图,若以硅原子代替金刚石晶体中的碳原子,便得到晶体硅;若将金刚石晶体中一半的碳原子换成硅原子,且碳、硅原子交替,即得到碳化硅晶体(金刚砂)
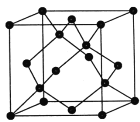
①碳化硅晶体(金刚砂)的化学式______________
②金刚石、晶体硅、碳化硅的熔点由高到低的顺序为__________________
③立方氮化硼晶体的结构与金刚石相似,硬度与金刚石相当,晶胞边长为361.5 pm。立方氮化硼的密度是_____________g/cm3(列出式子并化简,阿伏加德罗常数为NA)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一包由Cu、![]() 和CuO组成的混合物均分成两份:一份混合物在加热条件下与
和CuO组成的混合物均分成两份:一份混合物在加热条件下与![]() 充分反应,将固体全部转化成铜粉时固体质量减少了
充分反应,将固体全部转化成铜粉时固体质量减少了![]() ;向另一份混合物中加入
;向另一份混合物中加入![]() 溶液恰好完全反应生成
溶液恰好完全反应生成![]() 和
和![]() 假设不产生其他还原产物
假设不产生其他还原产物![]() ,这些NO和
,这些NO和![]() 标准状况
标准状况![]() 混合并通入足量水中,气体全部被吸收生成
混合并通入足量水中,气体全部被吸收生成![]() 。则该硝酸的物质的量浓度为
。则该硝酸的物质的量浓度为![]()
![]()
A.![]() B.
B.![]() C.
C.![]() D.
D.![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢氧燃料电池是一种常见化学电源,其原理反应:2H2+O2=2H2O,其工作示意图如图。下列说法不正确的是( )
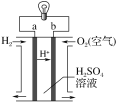
A.a极是负极,发生反应为H2-2e-=2H+
B.b电极上发生还原反应,电极反应式为O2+4H++4e-=2H2O
C.电解质溶液中H+向正极移动
D.放电前后电解质溶液的pH不会发生改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2018年国际计量大会将摩尔的定义修改为:1摩尔包含6.02214076×1023个基本单元,这一常数被称为阿伏加德罗常数(NA),通常用6.02×1023mol-1表示,新定义于2019年5月20日正式生效。下列说法不正确的是( )
A.标准状况下,22.4L的NH3约含有17×6.02×1023个质子
B.白磷分子(P4)呈正四面体结构,62g白磷中约含有3×6.02×1023个P-P键
C.标准状况下,18gH2O中约含有2×6.02×1023个氢原子
D.由新定义可知,阿伏加德罗常数表达为NA=6.02214076×1023 mol-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com