
【题目】将固体X投入过量的Y中,能生成白色沉淀并放出一种无色气体,该气体能燃烧,不易溶于水,则X和Y分别可能是( )
A.钠和氯化铝溶液B.铝和烧碱溶液C.过氧化钠和氯化亚铁D.锌和稀硫酸
科目:高中化学 来源: 题型:
【题目】实验室欲用NaOH固体配制0.1molL﹣1的NaOH溶液500mL:
(1)本实验必须用到的仪器有天平、药匙、玻璃棒、烧杯、胶头滴管、还有____.
(2)要完成本实验该同学应称出______g NaOH.
(3)在配制过程中,其他操作都是正确的,下列操作对浓度无影响的是__(填代号).
①没有洗涤烧杯和玻璃棒 ②转移溶液时不慎有少量洒到容量瓶外面 ③容量瓶不干燥,含有少量蒸馏水 ④ 定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向a mol NaOH的水溶液中通入b mol CO2,下列说法不正确的是
A. 当a>2b时,NaOH剩余(a-2b)mol
B. 当a<b时,发生的离子反应为:OH-+CO2=HCO3-
C. 当3a=4b时,发生的离子反应为:4OH-+3CO2=CO32-+2HCO3-+H2O
D. 当a/2<b<a时,溶液中生成HCO3-(a-b) mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】测定1 mol氧气在标准状况下所占体积的实验操作的步骤如下:
①按下图装配实验装置。
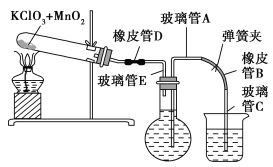
②洗净试管然后充分干燥。
③向500 mL烧瓶里装满水,向500 mL烧杯里加入少量水,把连接烧瓶和烧杯的玻璃管A、橡皮管B和玻璃管C中也装满水,在中间不要留下气泡,然后用弹簧夹把橡皮管B夹紧。
④称得试管的质量为14.45 g,往试管里加入KClO3和MnO2的混合物,再称其质量为15.95 g。
⑤打开弹簧夹,把烧杯举起使烧瓶和烧杯中的水面一致,再关闭弹簧夹,然后把烧杯中的水倒掉。
⑥打开弹簧夹,加热试管的混合物到不再产生气体,即水不再流向烧杯时为止。
⑦反应完毕后把装置冷却到室温。
⑧调节烧杯的高度使烧瓶和烧杯中的水面一致,然后再关闭弹簧夹。
⑨用500 mL量筒测量烧杯里水的体积为285.0 mL,把它换算为标准状况下氧气的体积为279.7 mL。
⑩再称量冷却后试管的质量为15.55 g。
(1)在操作⑦中,装置冷却时,玻璃管C的出口一直要在烧杯的水中,不能离开水面,其理由是 。
(2)简述操作⑧的必要性,即为什么要调节烧杯的高度,使烧瓶和烧杯中的水面一致? 。
(3)标准状况下,1 mol氧气所占的体积(保留小数后两位)为 L;混合物中MnO2的质量分数为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于能层与能级的说法中正确的是:
A、原子核外电子的每一个能层最多可容纳的电子数为2n2
B、任一能层的能级总是从s能级开始,而且能级数不一定等于该能层序数
C、同是s能级,在不同的能层中所能容纳的最多电子数是不相同的
D、1个原子轨道里最多只能容纳2个电子,但自旋方向相同。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】葡萄酒中抗氧化剂的残留量是以游离SO2的含量计算,我国国家标准(GB2760-2014)规定葡萄酒中SO2的残留量≤0.25g/L。某兴趣小组设计实验方案对葡萄酒中SO2进行测定。设计方案如下:
(1)用图甲装置(加持装置略)蒸馏并收集馏分SO2,实验时B中加入100.00mL葡萄酒样品和适量盐酸,加热使SO2全部逸出,在C中收集馏分。
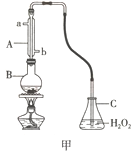
①若C中盛装H2O2溶液,则SO2与其完全反应的化学方程式为_________________________。除去C中过量的H2O2,然后用0.04000mol/LNaOH标准溶液进行滴定,滴定前排气泡时,应选择图乙中的_________(填序号)
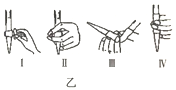
②滴定至终点消耗NaOH溶液25.00mL,据此计算葡萄酒中SO2含量为____________g/L。
(2)由于蒸馏时盐酸易挥发,该测定结果比实际值偏高,因此改进实验方案时可将盐酸改为稀硫酸,或者采取以下措施:
①将图甲装置C中盛装的液体改为H2O,且馏分无挥发,改用0.01000 mol/L 标准I2溶液滴定,反应的化学方程式为SO2+I2+2H2O=H2SO4+2HI,可选择________作指示剂,滴定终点的现象是_____________。
②盐酸虽然对此实验无干扰,但由于在上述实验过程中,存在空气的氧化作用,会使测定结果___________(填“偏高”“偏低”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在标准状况下,在三个干燥的烧瓶内分别装有纯净的NH3,含一半空气的HCl气体, NO2 和O2的混合气体[V(NO2)∶V(O2) = 4∶1 ],然后分别作喷泉实验,三个烧瓶内所得溶液的物质的量浓度之比为
A. 2∶1∶2 B. 5∶5∶4 C. 1∶1∶1 D. 无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应mA(s)+nB(g)![]() pC(g) △H<0,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系如图所示,下列叙述中一定正确的是
pC(g) △H<0,在一定温度下,平衡时B的体积分数(B%)与压强变化的关系如图所示,下列叙述中一定正确的是

①m+n>p ②x点表示的正反应速率大于逆反应速率
③n>p ④x点比y点时的反应速率慢
⑤若升高温度,该反应的平衡常数增大
A. ①②⑤ B. 只有②④ C. 只有①③ D. ①③⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com