
Àƒäãá¢À¢§¿îúê·ùÃáó(Na2S2O5)òúçáò°óñ¢¿î¾£₤¥êøÛØ£ÀÈá°îŃ¢ÅÀæÕ§½ÅÅàÓüôòçîÕȤ
òçîÕØ£ÀÀ§¿îúê·ùÃáóçáøóàÀ
ýèÆûàÓë¥æ¯øû(òçîÕú¯°»ƒÀæ¯øûáÖçá¢íó½)øóàÀNa2S2O5ÀÈæ¯øû·øÅÆÅNa2S2O5ƒÏäÍö—°—ȘñÂèºçáñÇÆÎöˆNa2SO3 Ȩ SO2 = Na2S2O5ÀÈ
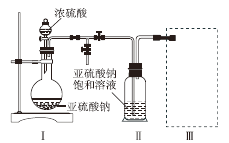
Âé æ¯øûÂþøÅýºèºó½äÍçá£₤îÏñ§°äò§öˆ________________________________È£
Âó èüë¥øÅòÂæ¯é´ê·ùÃçáýÈêÏØúó¼çáû«°óòú:__________________________;
Âú æ¯øûµÆûÆÖÇÎâÚöýó½È˜¢èîÀÆûçá柤üâÚæ¯øû(¥Å°øØúó¼ØîôåàË)öˆ_________(äŸÅ·¤é)ÀÈ
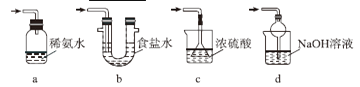
òçîÕѱÀÀ§¿îúê·ùÃáóçáÅåøò(Na2S2O5àÉÆÖùÛ¥Ç躰èNaHSO3)
Âà øÊû¼NaHSO3àÉؤøÅHSO![]() çáçÓ⊰äÑàǵÆÖùÛ§ã°äÑàȘ¢èýèÆûçáòçîÕñ§ñ´òú___________(äŸÅ·¤é)ÀÈ
çáçÓ⊰äÑàǵÆÖùÛ§ã°äÑàȘ¢èýèÆûçáòçîÕñ§ñ´òú___________(äŸÅ·¤é)ÀÈ
aÈÛýãÑ´àÉؤçápH bÈÛ¥ÆàŠBa(OH)2àÉؤ cÈÛ¥ÆàŠîöùÃ
dÈÛ¥ÆàŠóñ¤šàÉؤ eÈÛÆûâÑè¨ò₤àÿòåø§¥šýã
òçîÕà»ÀÀóüäîƒóøÅ¢¿î¾£₤¥êýÅê¶ê¢çáýãÑ´
Âè óüäîƒó°ÈÆûNa2S2O5æ¼¢¿î¾£₤¥êÀÈýãÑ´óüäîƒóøÅ¢¿î¾£₤¥êçáýÅê¶ê¢(ØåÆöâŠSO2¥óùÐ)çáñ§¯¡àÓüôȤ(çöÑ´òÝñÇÆÎöˆSO2 Ȩ I2 Ȩ 2H2O = H2SO4 Ȩ 2HI)

Âìèüò—çöÑ´¿»°äøÅçáøíçÐüøüµöˆ______________________________________È£
ÂÖ¯Çèüò—ñ§¯¡òçîÕȘü«¤áÝõæ¥I2àÉؤ25.00 mLȘ¡ûÇöòçîÕýãçûîªóñøÅ¢¿î¾£₤¥êçáýÅê¶ê¢(ØåÆöâŠSO2¥óùÐ)öˆ____________gÀÊLÈÙ1ÀÈ
ÀƒÇÞ¯¡À¢Na2SO3ȨH2SO4=Na2SO4ȨSO2À■ȨH2O(£·Na2SO3Ȩ2H2SO4=2NaHSO4ȨSO2À■ȨH2O) ñøؤôˋÑñ d aÀÂe àÉؤÝðâÑè¨È˜úØÝÈ°ø¯ŠñøøÆý£ëòè¨ 0.16
Àƒ§ãö—À¢
È´1ÈˋÆèæ¯øû·øÅñÂèºçáñÇÆ΢èøˆÈ˜æ¯øûÂþøÅýºèºó½äÍöˆÑ±î¾£₤ê·È˜îúê·ùÃáóÆŠé´ê·ùÃñÇÆÎ躰èê·ùÃáóÀÂѱ₤ê·¤ëùÛÀÈ
È´2ÈˋòÂæ¯é´ê·ùÃçáýÈêÏØúó¼çáû«°óòúȤñøؤôˋÑñÀÈ
È´3Èˋaæ¯øûáÖ祿ÉÆΡûèšàŠ¯ÝùÛøÅȘúØæ¯øûöˆûÉÝí£ñƒ°È˜æ¯øûáÖî¿ú¢å—ǵØæñÂ躯ýà¨òô¿òÀÈ
bæ¯øûö■òíѱ₤ê·áÉêΧüýŸÀÈ
cæ¯øûý£áÉö■òíѱ₤ê·È˜ùªØåößñ´òçüøÀÈ
dæ¯øûøÅúãî¾£₤áóàÉؤƊѱ₤ê·ñÇÆÎȘ¢èØåö■òíöýó½È˜úØáÉñâø¿ç¿ö■ÀÈ
È´4ÈˋHSO![]() ¥àáÉñÂèºçÓâŠHSO
¥àáÉñÂèºçÓâŠHSO![]()
![]() H++SO32-Șë˜òÝ£ÃñÂèºùÛ§ãHSO
H++SO32-Șë˜òÝ£ÃñÂèºùÛ§ãHSO![]() + H2O
+ H2O![]() H2SO3+OH-Șà¶HSO
H2SO3+OH-Șà¶HSO![]() çáçÓâŠÇµÆÖHSO
çáçÓâŠÇµÆÖHSO![]() çáùÛ§ãȘå·àÉؤüåùÃÅåÀÈ
çáùÛ§ãȘå·àÉؤüåùÃÅåÀÈ
È´5ÈˋÂìçöÑ´¿»°äøÅçáøíçÐüøüµöˆÈ¤àÉؤÝðâÑè¨È˜úØÝÈ°ø¯ŠñøøÆý£ëùè¨È˜¿òÇÞ¯¡öˆÈ¤àÉؤÝðâÑè¨È˜úØÝÈ°ø¯ŠñøøÆý£ëùè¨ÀÈ
ÂÖ¡ªƒïñÇÆÎSO2 Ȩ I2 Ȩ 2H2O = H2SO4 Ȩ 2HI¥óùÐÀÈ
È´1ÈˋÆèæ¯øû·øÅñÂèºçáñÇÆ΢èøˆÈ˜æ¯øûÂþøÅýºèºó½äÍöˆÑ±î¾£₤ê·È˜îúê·ùÃáóÆŠé´ê·ùÃñÇÆÎ躰èê·ùÃáóÀÂѱ₤ê·¤ëùÛȘ£₤îÏñ§°äò§öˆÈ¤Na2SO3ȨH2SO4=Na2SO4ȨSO2À■ȨH2O(£·Na2SO3Ȩ2H2SO4=2NaHSO4ȨSO2À■ȨH2O)È£¿òÇÞ¯¡öˆÈ¤Na2SO3ȨH2SO4=Na2SO4ȨSO2À■ȨH2O(£·Na2SO3Ȩ2H2SO4=2NaHSO4ȨSO2À■ȨH2O)ÀÈ
È´2ÈˋòÂæ¯é´ê·ùÃçáýÈêÏØúó¼çáû«°óòúȤñøؤôˋÑñȘ¿òÇÞ¯¡öˆÈ¤ñøؤôˋÑñÀÈ
È´3Èˋaæ¯øûáÖ祿ÉÆΡûèšàŠ¯ÝùÛøÅȘúØæ¯øûöˆûÉÝí£ñƒ°È˜æ¯øûáÖî¿ú¢å—ǵØæñÂ躯ýà¨òô¿òȘÇÚöµÈ£
bæ¯øûö■òíѱ₤ê·áÉêΧüýŸÈ˜ÇÚöµÈ£
cæ¯øûý£áÉö■òíѱ₤ê·È˜ùªØåößñ´òçüøȘÇÚöµÈ£
dæ¯øûøÅúãî¾£₤áóàÉؤƊѱ₤ê·ñÇÆÎȘ¢èØåö■òíöýó½È˜úØáÉñâø¿ç¿ö■Șí»àñÈ£
¿òîÀdÀÈ
È´4ÈˋHSO![]() ¥àáÉñÂèºçÓâŠHSO
¥àáÉñÂèºçÓâŠHSO![]()
![]() H++SO32-Șë˜òÝ£ÃñÂèºùÛ§ãHSO
H++SO32-Șë˜òÝ£ÃñÂèºùÛ§ãHSO![]() + H2O
+ H2O![]() H2SO3+OH-Șà¶HSO
H2SO3+OH-Șà¶HSO![]() çáçÓâŠÇµÆÖHSO
çáçÓâŠÇµÆÖHSO![]() çáùÛ§ãȘå·àÉؤüåùÃÅåȘ¿òaeí»àñÀÈ
çáùÛ§ãȘå·àÉؤüåùÃÅåȘ¿òaeí»àñÀÈ
È´5ÈˋÂìçöÑ´¿»°äøÅçáøíçÐüøüµöˆÈ¤àÉؤÝðâÑè¨È˜úØÝÈ°ø¯ŠñøøÆý£ëòè¨È˜¿òÇÞ¯¡öˆÈ¤àÉؤÝðâÑè¨È˜úØÝÈ°ø¯ŠñøøÆý£ëòè¨ÀÈ
ÂÖ¡ªƒïñÇÆÎSO2 Ȩ I2 Ȩ 2H2O = H2SO4 Ȩ 2HIȘå·îªóñøÅ¢¿î¾£₤¥êçáýÅê¶ê¢=(0.01mol/LÀê0.025LÀê64g/mol)/0.1L=0.16g/LȘ¿òÇÞ¯¡öˆÈ¤0.16ÀÈ



| áõ¥Ñ | ¡ÔøÅ¢ö°ä | áõ¥Ñ | °¾øÅ¢ö°ä |
| ¡ÔØ£ | ¡ÔØ£ûãñî¢ö°äëó¥—ÈÀ | °¾Ø£ | °¾Ø£ûãñî¢ö°äëó¥—ÈÀ |
| ¡Ôѱ | ¡Ôѱûãñî¢ö°äëó¥—ÈÀ | °¾Ñ± | °¾Ñ±ûãñî¢ö°äëó¥—ÈÀ |
| ¡Ôà» | ¡Ôà»ûãñî¢ö°äëó¥—ÈÀ | °¾à» | °¾à»ûãñî¢ö°äëó¥—ÈÀ |
¢óá¢È¤¡ÔøÅ£₤îÏ âÇåÇȤ äãÅëȤ
Àƒäãá¢À¢üôêÅùçñ´í»àñçáòú
A.òçîÕòØÆΧ¨áóÝÈÇÌåÖû¤ÆëøÅB.úÍüÇëõçáñøؤôˋÑñ¤ëàïê¢ó¢Ñ¥Øˆ¡èåÿ
C.¢èÆûƒóƒ¨ÇºäÌCCl4ïëàÀçãùÛøÅçáçãçËøòD.ѱ₤ä¥òúùÃÆõçáø¼Øˆ°èñø
ýÕ¢ÇÇÞ¯¡¤ë§ãö—>>
¢óá¢È¤¡ÔøÅ£₤îÏ âÇåÇȤ äãÅëȤ
Àƒäãá¢À¢50mL0.50 molÀÊL-1çáîöùÃÆŠ50mL0.55 molÀÊL-1çáNaOHàÉؤåÖàÓë¥ùªòƒçáæ¯øûøŧ½ÅÅøŤëñÇÆÎÀÈòçîÕò»ƒïàÓüôÝÚȤ
òçîÕÅ·¤é | óÞò¥öôÑàt1/ÀÌ | øíø¿öôÑàt2/ÀÌ | |
îöùà | NaOHàÉؤ | £š¤üàÉؤ | |
1 | 20.0 | 20.1 | 23.2 |
2 | 20.2 | 20.4 | 23.4 |
3 | 20.5 | 20.6 | 23.6 |

§■ùóàüöˆ0.50 molÀÊLÈÙ1NaOHàÉؤ¤ë0.50 molÀÊLÈÙ1HClàÉؤçáûÉÑàÑ¥òú1gÀÊcmÈÙ3ȘøŤ뤵躰èàÉؤçáÝààààïcȧ4.18 JÀÊgÈÙ1ÀÊÀÌÈÙ1ÀÈ
úŠ£ÄÇÞüôêÅöòäãȤÇÆòçîÕæ¯øûèü¢ÇȘë¥øÅèÅàÝèìçáØ£øøýÈêÏØúó¼òú________ȘèíÝÙ¥ðäŸôºùÕéïáÙùÉêüçáæ¼Æûòú_____________ÀÈǵèíÝÙèüàÓý£¡úÆýø§¯ÍȘå·úµçûçáøŤëààò»øç_______(äŸÀ¯ó¨ÇµÀÝ À¯ó¨ÅÀÀÝ£·À¯ößƯüšÀÝ)ÀÈå·øŤëààÎÊHȧ________(àÀÅÀò»çФµØ£ö£)ÀÈ
ýÕ¢ÇÇÞ¯¡¤ë§ãö—>>
¢óá¢È¤¡ÔøÅ£₤îÏ âÇåÇȤ äãÅëȤ
Àƒäãá¢À¢¯îåÖ¢íó½øŃûøûçáôêó˜5.0 gëÑàŠòÂÆÅ500 mL 0.5 molÀÊLÈÙ1ê·ùÃàÉؤçáèíÝÙøÅȘ¡ûôêó˜ÆŠê·ùÃñÇÆÎýºèºúãó½çáùìôòvÆŠñÇÆÎòÝ¥ðt¢èÆûàÓë¥æ½ÝõúºüÔâÇÝÚòƒÀÈüôêÅëóôÜÇÚöµçáòú(ÀÀÀÀ)
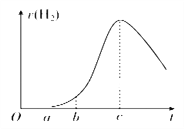
A. OÀ¨aÑöý£ýºèºúãó½òúØ·öˆÝÚûÌçáî¾£₤öÿ¡¶âŠêùôê¤ëê·ùÃàÉؤ
B. bÀ¨cÑöýºèºúãó½çáùìôò嗥Ƨü¢šçáø¼ØˆåÙØ·øÛØ£òúöôÑà軡Ô
C. t>còÝýºèºúãó½çáùìôò§ççëø¼ØˆòúØ·öˆàÉؤøÅc(HȨ)§ççë
D. tȧcòÝñÇÆÎÇÎÆÖó§¤ãæÇä˜
ýÕ¢ÇÇÞ¯¡¤ë§ãö—>>
¢óá¢È¤¡ÔøÅ£₤îÏ âÇåÇȤ äãÅëȤ
Àƒäãá¢À¢åÖØ£¡—ý£Ç¨ààçá¿äÑ´àçáûÉÝíàïó¼øÅȘñÂ躢èáÌñÇÆÎmA(g) + nB(g) ![]() pC(g) + qD(g)ȘçÝmÀÂnÀÂpÀÂqöˆàöØãí«ò»òÝȘñÇÆÎÇÿç§ó§¤ãçáÝõøƒòú( )
pC(g) + qD(g)ȘçÝmÀÂnÀÂpÀÂqöˆàöØãí«ò»òÝȘñÇÆÎÇÿç§ó§¤ãçáÝõøƒòú( )
ÂÖäÍüçöôÑàý£åì¡áÝð
ÂÜ¡¼æÕñøçáé´Ñàý£åì¡áÝð
ÂÉ¡¼æÕñøçáøòê¢ñøò»ý£åì¡áÝð
ÂïñÇÆÎùìôòv(A)Àûv(B)Àûv(C)Àûv(D)=mÀûnÀûpÀûq
ÂßçËö£òÝ¥ðáÖm mol AÑü¥■ñÇÆÎȘë˜òÝp mol CØýÑü¥■ñÇÆÎ
ÂÔäÍüççáûÉÑàý£åìÝð£₤
AÈÛÂÜÂÉÂïÂß BÈÛÂÖÂÜÂÉÂß
CÈÛÂìÂÜÂÉÂï DÈÛÂÜÂÉÂßÂÔ
ýÕ¢ÇÇÞ¯¡¤ë§ãö—>>
¢óá¢È¤¡ÔøÅ£₤îÏ âÇåÇȤ äãÅëȤ
Àƒäãá¢À¢ùöǺø½û«ñ´Ø§îÏ¥ØùöÇàçáÀÑüÇåˋ¥₤ô¥ÀñøÅÆÅÀ¯Ø½íŠîÕуÀÝçá¥úåÄȘÀ¯Ø½íŠîÕуÀÝçáåÙâÚòú4AgȨ2H2SȨO2===2Ag2SȨ2H2OȘóðøÅH2Sòú
A. î¾£₤¥ê B. £¿åÙ¥ê C. ¥àòúî¾£₤¥êÆøòú£¿åÙ¥ê D. ¥àý£òúî¾£₤¥êÆøý£òú£¿åÙ¥ê
ýÕ¢ÇÇÞ¯¡¤ë§ãö—>>
¢óá¢È¤¡ÔøÅ£₤îÏ âÇåÇȤ äãÅëȤ
Àƒäãá¢À¢¡ªƒïüô륤ÈùÛæܤüâ«Æûçá¿ÊØçê¼°äë¥È˜éÅÑüüôêÅùçñ´í»àñçáòúÈ´ Èˋ
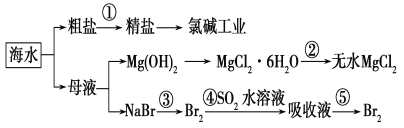
ØîøˆÈ¤MgCl2ÀÊ6H2OòÉàà躰èMg(OH)Cl¤ëHCló½äÍçàÀÈ
A. °»àËÇøîöøÅåÆøòÈ´Mg2+ÀÂSO42ÈÙÀÂCa2+ÈˋȘ¥ÆàŠçáØˋóñù°Å·öˆÈ¤NaOHàÉؤÀºNa2CO3àÉؤÀºBaCl2àÉؤÀº¿»ôù¤µ¥ÆîöùÃ
B. åÖ¿»°äÂÖøŧ¨MgCl2ÀÊ6H2Oæóèí¥Ç¢èøóçûößùÛMgCl2
C. ÇÆáÉꢧúÑàâÇ¢ÇȘôय़¿ÊØçøÅçáçÓ§ãÝˤëò°îöùÛòúØ£¡—§¨£₤îÏáÉ戣₤öˆçÓáÉçá¿»°ä
D. ÇÆçÖÂÜý§ç§çÖÂïý§çáá¢çáòúöˆêùé´ù¾¡£¥₤ðÍ
ýÕ¢ÇÇÞ¯¡¤ë§ãö—>>
¢óá¢È¤¡ÔøÅ£₤îÏ âÇåÇȤ äãÅëȤ
Àƒäãá¢À¢¿ÊØçèüü«°»çˆî¾£₤öÿçáöÜàƒÈ˜¢èÆûàÓüôñÇÆÎȤ
CH4(g)Ȩ2NO2(g)![]() N2(g)ȨCO2(g)Ȩ2H2O(g) ÎÊHȧa kJ/mol
N2(g)ȨCO2(g)Ȩ2H2O(g) ÎÊHȧa kJ/mol
åÖöôÑàT1¤ëT2òÝȘñøÝÞ§¨0.50 mol CH4¤ë1.2 mol NO2°ðàŠäÍ£»öˆ1 LçáûÉÝíàïó¼øÅȘýãçûn(CH4)ùÌòÝ¥ðÝð£₤ò»ƒïàÓüôÝÚȤ
öôÑà | òÝ¥ð/min n/mol | 0 | 10 | 20 | 40 | 50 |
T1 | n(CH4) | 0.50 | 0.35 | 0.25 | 0.10 | 0.10 |
T2 | n(CH4) | 0.50 | 0.30 | 0.18 | ÀÙÀÙ | 0.15 |
üôêÅùçñ´ý£í»àñçáòú
A. 10 mináÖȘT1òÝv(CH4)T2òÝÅÀ B. öôÑàȤT1È¥T2
C. ÎÊHȤa < 0 D. ó§¤ã°Èò»È¤K(T1)È¥K(T2)
ýÕ¢ÇÇÞ¯¡¤ë§ãö—>>
¢óá¢È¤¡ÔøÅ£₤îÏ âÇåÇȤ äãÅëȤ
Àƒäãá¢À¢üôêÅòçîÕáÉÇÿç§åÊóÖá¢çáçáòú
A.  øóðÍݧ
øóðÍݧ
B.  ÇÆ a ÇÎØóç§ b ÇÎȘ¿Üýšç§ëÙù¢Æè¤ÖÝð¤š
ÇÆ a ÇÎØóç§ b ÇÎȘ¿Üýšç§ëÙù¢Æè¤ÖÝð¤š
C.  ¥šîÕößùÛØØÇ¥øÅòúñþÆÅùÛ
¥šîÕößùÛØØÇ¥øÅòúñþÆÅùÛ
D.  ñø⊤˜çãçáùáôà£₤ä¥Ø¤äÍȘæŸøíåÖæÑÅöó¢øÅ¢è£þçûçã
ñø⊤˜çãçáùáôà£₤ä¥Ø¤äÍȘæŸøíåÖæÑÅöó¢øÅ¢è£þçûçã
ýÕ¢ÇÇÞ¯¡¤ë§ãö—>>
¿º¥òîÏÅÈÆéîÀ - êñü¯ýÃêÅÝÚ - òåäãêÅÝÚ
¤±ÝÝòÀ£Ëêˆë½öËñ´¤ëý£ê¥ÅéüƒìÝ´ó§ä´ | ë½èüÆŤÎÅéüƒìÝ´æ´ú½ | çÓÅéíˋóÙƒìÝ´æ´ú½ | èÌâºòñÅÕößø¼ØÍÆŤÎÅéüƒìÝ´æ´ú½ | èÌóµúøà´ƒìÝ´æ´ú½
öËñ´¤ëý£ê¥ÅéüƒìÝ´çÓ£¯È¤027-86699610 ƒìÝ´ÆòüðȤ58377363@163.com