
【题目】镍具有铁磁性和延展性,能导电和导热。镍单质及其化合物的化学性质与铁相似。
(1)镍易溶于稀的无机酸中,并放出氢气,写出镍与盐酸反应的化学方程式:_____________。
(2)在隔绝空气的条件下,加热NiC2O4使其分解,就能得到暗绿色的氧化亚镍,写出该反应的化学方程式: _____________。
(3)Ni2O3不溶于水,可溶于盐酸并放出氯气,写出该反应的离子方程式: _____________。
(4)氢镍电池是一种碱性可充电电池,污染小,比能量较大。氢镍电池的总反应式是:H2+2NiO(OH) ![]() 2Ni(OH)2。写出放电时的正极反应式: _____________。
2Ni(OH)2。写出放电时的正极反应式: _____________。
(5)纳米材料镍粉(Ni)是一种高性能电极材料,其制备过程如下:
步骤I:取0.2mol/L的硝酸亚镍溶液,调节pH除铁后,加入活性炭过滤。
步骤Ⅱ:向所得滤液中滴加1.5mol/L的NaHCO3溶液使Ni2+完全沉淀,生成:xNiCO3·yNi(OH)2·zH2O。
步骤Ⅲ:将产生的沉淀用大量高纯水清洗并用离心机甩干。
步骤Ⅳ:加入稍过量的肼溶液(N2H4·H2O),使上述沉淀还原完全,将生成的Ni水洗后,再用95%的乙醇浸泡后晾干。为测定xNiCO3·yNi(OH)2·zH2O的组成,进行如下实验:
①准确称取7.54g样品与过量的肼溶液(N2H4·H2O)充分反应,共收集到1.12LN2和CO2的混合气体(已换算成标准状况)。
②另取等质量的样品充分灼烧,冷却后称得残留固体NiO的质量为4.5g。
通过计算确定xNiCO3·yNi(OH)2·zH2O的化学式_______________。
【答案】 Ni+2HCl=NiCl2+H2↑ NiC2O4![]() NiO+CO↑+CO2↑ Ni2O3+6H++2Cl-=2Ni2++Cl2↑+3H2O 2NiO(OH)+2e-+2H2O=2Ni(OH)2+2OH-或NiO(OH)+e-+H2O=Ni(OH)2+OH- NiCO3·2Ni(OH)2·4H2O
NiO+CO↑+CO2↑ Ni2O3+6H++2Cl-=2Ni2++Cl2↑+3H2O 2NiO(OH)+2e-+2H2O=2Ni(OH)2+2OH-或NiO(OH)+e-+H2O=Ni(OH)2+OH- NiCO3·2Ni(OH)2·4H2O
【解析】(1)镍单质及其化合物的化学性质与铁相似,镍与盐酸反应生成NiCl2和氢气,反应的化学方程式为:Ni+2HCl=NiCl2+H2↑;(2)在隔绝空气的条件下,加热NiC2O4使其分解,就能得到暗绿色的氧化亚镍,NiC2O4中Ni的化合价为+2价,碳的化合价为+3,生成NiO中Ni的化合价为+2价不变,根据氧化还原反应原理,则若产生气体为CO2同时应该还产生CO,反应的化学方程式为:NiC2O4![]() NiO+CO↑+CO2↑;(3)Ni2O3不溶于水,可溶于盐酸并放出氯气,反应的离子方程式为:Ni2O3+6H++2Cl-=2Ni2++Cl2↑+3H2O;(4)氢镍电池的总反应式是:H2+2NiO(OH)
NiO+CO↑+CO2↑;(3)Ni2O3不溶于水,可溶于盐酸并放出氯气,反应的离子方程式为:Ni2O3+6H++2Cl-=2Ni2++Cl2↑+3H2O;(4)氢镍电池的总反应式是:H2+2NiO(OH) ![]() 2Ni(OH)2。放电时为原电池,正极上NiO(OH)得电子被还原生成2Ni(OH)2,电极反应式为:2NiO(OH)+2e-+2H2O=2Ni(OH)2+2OH-或NiO(OH)+e-+H2O=Ni(OH)2+OH-;(5)n(CO2)+n(N2)=
2Ni(OH)2。放电时为原电池,正极上NiO(OH)得电子被还原生成2Ni(OH)2,电极反应式为:2NiO(OH)+2e-+2H2O=2Ni(OH)2+2OH-或NiO(OH)+e-+H2O=Ni(OH)2+OH-;(5)n(CO2)+n(N2)= ![]() =0.05mol,1molxNiCO3·yNi(OH)2·zH2O生成二氧化碳xmol,生成氮气的物质的量由Ni被还原进行求算,为
=0.05mol,1molxNiCO3·yNi(OH)2·zH2O生成二氧化碳xmol,生成氮气的物质的量由Ni被还原进行求算,为![]() mol,n(NiO)=
mol,n(NiO)= ![]() =0.06mol,设7.54g样品中含有NiCO3、Ni(OH)2的物质的量分别为a、b,则有:a +
=0.06mol,设7.54g样品中含有NiCO3、Ni(OH)2的物质的量分别为a、b,则有:a + ![]() =0.05mol,x+y=0.06mol ;解得:a=0.02 mol、b=0.04 mol。7.54g样品中含有结晶水的物质的量:n(H2O)=
=0.05mol,x+y=0.06mol ;解得:a=0.02 mol、b=0.04 mol。7.54g样品中含有结晶水的物质的量:n(H2O)= ![]() =0.08 mol,x:y:z=n(NiCO3):n[Ni(OH)2]:n (H2O)=0.02 mol:0.04 mol:0.08 mol =1:2:4 ,故该样品的化学式为NiCO3·2Ni(OH)2·4H2O。
=0.08 mol,x:y:z=n(NiCO3):n[Ni(OH)2]:n (H2O)=0.02 mol:0.04 mol:0.08 mol =1:2:4 ,故该样品的化学式为NiCO3·2Ni(OH)2·4H2O。


 直通贵州名校周测月考直通名校系列答案
直通贵州名校周测月考直通名校系列答案科目:高中化学 来源: 题型:
【题目】A,B,C,D,E都为短周期元素,A是相对原子质量最小的元素;B的+1价阳离子和C的﹣1价阴离子都与氖原子具有相同的电子层结构;D在C的下一周期,可与B形成BD型离子化合物;E和C为同一周期元素,其最高价氧化物对应的水化物为一种强酸.请根据以上信息回答下列问题:
(1)B元素在元素周期表中的位置是第周期族;
(2)画出C元素的原子结构示意图;
(3)与E的氢化物分子所含电子总数相等的分子是(举一例,填化学式,下同)、阳离子是;
(4)A与D形成的化合物中含有化学键的类型是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述中,不正确的是
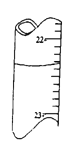
A. 用0.1026mol/L的盐酸滴定25.00mL未知浓度的氢氧化钠溶液,滴定达终点时,滴定管中的液面如图所示,正确的读数为22.35mL
B. 用标准烧碱溶液滴定待测的醋酸溶液,应以酚酞为指示剂
C. 若200mLc(H+)=1×10-3mol/L的某一元酸和100mLc(OH-)=1×10-3mol/L的某一元碱相混合后,溶液呈碱性。则所用的酸和碱可能是等浓度的弱酸和强碱
D. 25℃时,若pH=a的10体积某强酸溶液与pH=b的1体积某强碱溶液混合后溶液呈中性,则a+b=15
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】元素是构成我们生活的世界中一切物质的“原材料”.
(1)自18世纪以来,科学家们不断探索元素之谜.通过从局部到系统的研究过程,逐渐发现了元素之间的内在联系.下面列出了几位杰出科学家的研究工作.
序号 | ① | ② | ③ | ④ |
科学家 | 纽兰兹 | 道尔顿 | 德贝莱纳 | 尚古尔多 |
工作 | 发现“八音律”,指出从某一指定的元素起,第八个元素是第一个元素的某种重复 | 创立 近代原子论,率先开始相对原子质量的测定工作 | 发现了5组性质相似的“三元素组”,中间元素的相对原子质量为前后两种元素相对原子质量的算术平均值 | 认为 各元素组之间并非毫不相关,可以用相对原子质量把它们按从小到大的顺序串联 |
上述科学家的研究按照时间先后排序合理的是(填数字序号).
(2)1869年,门捷列夫在前人研究的基础上制出了第一张元素周期表,如图1所示. 
①门捷列夫将已有元素按照相对原子质量排序,同一(填“横行”或“纵列”)元素性质相似.结合表中信息,猜想第4列方框中“?=70”的问号表达的含义是 , 第5列方框中“Te=128?”的问号表达的含义是 .
②到20世纪初,门捷列夫周期表中为未知元素留下的空位逐渐被填满.而且,随着原子结构的逐渐揭秘,科学家们发现了元素性质不是随着相对原子质量递增呈现周期性变化,而是随着原子序数(核电荷数)递增呈现周期性变化.其本质原因是(填字母序号).
A.随着核电荷数递增,原子核外电子排布呈现周期性变化
B.随着核电荷数递增,原子半径呈现周期性变化
C.随着核电荷数递增,元素最高正化合价呈现周期性变化
(3)在现有的元素周期表中有A,B,D,E,X、Y、Z七种短周期元素.X与Y处于同一周期,Y的最高价氧化物的水化物与强酸、强碱均能反应.Z的单质常温下为气态,同条件下相对于氢气的密度比为35.5.其余信息如图2所示: ①上述七种元素中,处于第二周期的有(用元素符号表示,下同),X在周期表中的位置是 .
②E的原子结构示意图为 , 写出Z元素气态氢化物的电子式: .
③B单质与E的最高价氧化物的水化物在一定条件下发生反应的化学方程式为;Y单质与X的最高价氧化物的水化物溶液反应的离子方程式为 .
④B和D的最高价氧化物的水化物的化学式分别为、 , 二者酸性前者(填“强于”或“弱于”)后者,原因是B和D的非金属性有差异,利用原子结构解释产生差异的原因: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法中不正确的是( )
A. 用过滤法除去食盐水中的少量泥沙
B. 用水溶解可除去氢氧化钠中的碳酸钠
C. 用蒸发结晶的方法从食盐水中提取氯化钠
D. 用加热法除去水中溶解的少量氧气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E均是短周期主族元素,其原子序数依次增大,A和B同周期,A和D同主族,A原子最外层电子数是内层电子数的二倍,B元素族序数是周期数的三倍,B的阴离子与C的阳离子电子层结构相同,C的单质与B的单质在不同条件下反应,可生成C2B或C2B2,E是所在周期中原子半径最小的元素,请回答:
(1)D在元素周期表中的位置是___________。
(2)C2B2的电子式是________
(3)B、C、E的离子半径由大到小的顺序为________(用离子符号回答); A、D、E元素最高价氧化物对应水化物的酸性由强到弱为_________(用化学式回答,下同),B的气态氢化物与H2S相比沸点高的是_____
(4)写出D的氧化物与氢氟酸反应的化学方程式____________
(5)水中锰含量超标容易使洁具和衣物染色,使水产生异味,EB2可以用来除去水中超标的Mn2+,生成黑色沉淀MnO2,当消耗13.50g EB2时,共转移了lmol电子,则反应的离子方程式__________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列说法正确的是
A. 2.4 g镁原子变成离子时,失去的电子数为0.3NA
B. 常温常压下,28 g氮气所含的原子数为2NA
C. 18 g H218O中含有的原子总数为3NA
D. 32 g氧气和4 g氦气所含原子数目相等,均为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由U形管、质量为mg的铁棒、质量为mg的碳棒和1L0.2mol·L-1CuCl2溶液组成如图所示装置,下列说法不正确的是( )

A. 打开K,铁棒上有紫红色物质析出
B. 闭合K,碳棒上有紫红色固体析出
C. 闭合K,碳棒表面发生的电极反应为Cu2++2e-=Cu
D. 闭合K,当电路中有0.3NA个电子通过时,理论上碳棒与铁棒的质量差为9.6g
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com