
【题目】一种合成囧烷(E)的路线如下:

⑴ A中所含官能团的名称是_______________;E的分子式为_________。
⑵ A→B、B→C的反应类型分别是___________、___________。
⑶ 在一定条件下,B与足量乙酸可发生酯化反应,其化学方程式为______________。
⑷ F是一种芳香族化合物,能同时满足下列条件的F的同分异构体有_____种。
① 1个F分子比1个C分子少两个氢原子
② 苯环上有3个取代基
③ 1molF能与2molNaOH反应
写出其中核磁共振氢谱图有5组峰,且面积比为3∶2∶2∶2∶1的一种物质的结构简式:__________。
⑸ 1,2-环己二醇(  )是一种重要的有机合成原料,请参照题中的合成路线,以
)是一种重要的有机合成原料,请参照题中的合成路线,以 和
和![]() 为主要原料,设计合成1,2-环己二醇的合成路线。______________
为主要原料,设计合成1,2-环己二醇的合成路线。______________
【答案】羟基、碳碳双键 C12H18 加成反应 氧化反应 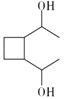 +2CH3COOH
+2CH3COOH![]()
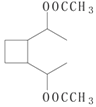 +2H2O 6
+2H2O 6 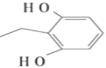 或
或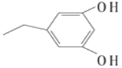
【解析】
⑴ 根据A(![]() )的结构结合常见官能团的结构判断;根据E(
)的结构结合常见官能团的结构判断;根据E(![]() )确定其分子式;
)确定其分子式;
(2)对比A、B结构,2个A分子中碳碳双键中一个键断裂,碳原子相互连接成环得到B;B中羟基转化为C中羰基,据此判断反应类型;
⑶ B中含有羟基,在一定条件下,能够与乙酸发生酯化反应,结合酯化反应的机理书写与乙酸反应的方程式;
⑷ C为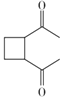 ,分子式为C8H12O2,1个F分子比1个C分子少两个氢原子,则F的分子式为C8H10O2,其不饱和度=4,F是一种芳香族化合物,说明除了苯环外,不存在不饱和结构,1molF能与2molNaOH反应,并且苯环上有3个取代基,说明苯环上含有2个羟基和1个乙基,据此书写满足条件的同分异构体;
,分子式为C8H12O2,1个F分子比1个C分子少两个氢原子,则F的分子式为C8H10O2,其不饱和度=4,F是一种芳香族化合物,说明除了苯环外,不存在不饱和结构,1molF能与2molNaOH反应,并且苯环上有3个取代基,说明苯环上含有2个羟基和1个乙基,据此书写满足条件的同分异构体;
⑸以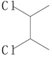 和
和![]() 为主要原料合成1,2-环己二醇(
为主要原料合成1,2-环己二醇( ![]() ),根据题干流程图C→D的提示,需要合成
),根据题干流程图C→D的提示,需要合成![]() ,再由
,再由![]() 与乙二醛反应生成
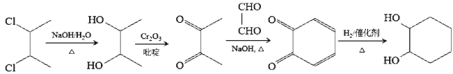
与乙二醛反应生成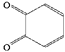 ,最后将
,最后将 转化为
转化为![]() 即可。
即可。
⑴ A(![]() )中所含官能团有羟基和碳碳双键;E(
)中所含官能团有羟基和碳碳双键;E(![]() )的分子式为C12H18,故答案为:羟基、碳碳双键;C12H18;
)的分子式为C12H18,故答案为:羟基、碳碳双键;C12H18;
(2)对比A、B结构,2个A分子中碳碳双键中一个键断裂,碳原子相互连接成环得到B,属于加成反应;B中羟基转化为C中羰基,发生氧化反应,故答案为:加成反应;氧化反应;
⑶ B中含有羟基,在一定条件下,能够与乙酸发生酯化反应,反应的化学方程式为 +2CH3COOH
+2CH3COOH![]()
 +2H2O,故答案为:
+2H2O,故答案为: +2CH3COOH
+2CH3COOH![]()
 +2H2O;
+2H2O;
⑷ C为 ,分子式为C8H12O2,1个F分子比1个C分子少两个氢原子,则F的分子式为C8H10O2,不饱和度=
,分子式为C8H12O2,1个F分子比1个C分子少两个氢原子,则F的分子式为C8H10O2,不饱和度=![]() =4,F是一种芳香族化合物,说明除了苯环外,不存在不饱和结构,1molF能与2molNaOH反应,并且苯环上有3个取代基,说明苯环上含有2个羟基和1个乙基,满足条件的同分异构体有6种(羟基位于邻位的2种,羟基位于间位的3种,羟基位于对位的1种);其中核磁共振氢谱图有5组峰,且面积比为3∶2∶2∶2∶1的结构简式为
=4,F是一种芳香族化合物,说明除了苯环外,不存在不饱和结构,1molF能与2molNaOH反应,并且苯环上有3个取代基,说明苯环上含有2个羟基和1个乙基,满足条件的同分异构体有6种(羟基位于邻位的2种,羟基位于间位的3种,羟基位于对位的1种);其中核磁共振氢谱图有5组峰,且面积比为3∶2∶2∶2∶1的结构简式为 或
或 ,故答案为:6;
,故答案为:6; 或
或 ;
;
⑸以 和
和![]() 为主要原料合成1,2-环己二醇(
为主要原料合成1,2-环己二醇( ![]() ),根据题干流程图C→D的提示,可以首先由
),根据题干流程图C→D的提示,可以首先由 合成
合成![]() ,再由
,再由![]() 与乙二醛反应生成
与乙二醛反应生成 ,最后将
,最后将 转化为
转化为![]() 即可;其中由
即可;其中由 合成
合成![]() 可以将氯原子水解后氧化得到;将
可以将氯原子水解后氧化得到;将 转化为
转化为![]() 只需要与氢气加成得到,因此合成路线为
只需要与氢气加成得到,因此合成路线为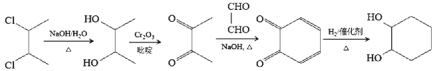 ,故答案为:
,故答案为: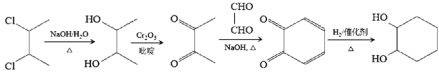 。
。


科目:高中化学 来源: 题型:
【题目】I.在恒温恒压下,向密闭容器中充入4 mol SO2和2 mol O2混合气体,2 min后,反应达到平衡,生成SO3气体0.5 mol,同时放出热量Q kJ。回答下列问题
(1)写出该反应的热化学方程式为______________________________________。
(2)在该条件下,反应前后容器的体积之比为______________。
(3)①若把“恒温恒压下”改为“恒压绝热条件下”反应,平衡后n(SO3)______0.5mol(填 “大于”、“小于”或“等于”);
②若把“恒温恒压下”改为“恒温恒容下”反应,达平衡时放出热量_______Q kJ(填 “大于”、“小于”或“等于”)。
II. 用焦炭还原NO2的反应为:2NO2(g)+2C(s )![]() N2(g)+2CO2(g),在恒温条件下,1 mol NO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:
N2(g)+2CO2(g),在恒温条件下,1 mol NO2和足量C发生该反应,测得平衡时NO2和CO2的物质的量浓度与平衡总压的关系如图所示:

(1)A、B两点的浓度平衡常数关系:Kc(A)_____Kc(B) (填 “﹥”、“<”或“﹦”)。
(2)A、B、C三点中NO2的转化率最高的是_____(填“A”或“B”或“C”)点。
(3)计算C点时该反应的压强平衡常数Kp(C)=______(Kp是用平衡分压代替平衡浓度计算,分压=总压物质的量分数)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物环丙叉环丙烷(![]() )具有特殊结构,倍受化学家关注.下列关于该化合物的说法错误的是
)具有特殊结构,倍受化学家关注.下列关于该化合物的说法错误的是
A. 与苯互为同分异构体B. 二氯代物超过两种
C. 所有碳原子均处于同一平面D. 生成1molC6H14至少需要3molH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25 ℃时,NaCN溶液中CN-、HCN浓度所占分数(δ)随pH变化的关系如下图甲所示。
向10 mL 0.01 mol·L-1 NaCN溶液中逐滴加入0.01 mol·L-1的盐酸,其pH变化曲线如下图乙所示[其中a点的坐标为(9.5,0.5)]。

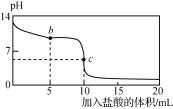
甲 乙
下列溶液中的关系中一定正确的是
A. 图甲中pH=7的溶液:c(Cl-)=c(HCN)
B. 常温下,NaCN的水解平衡常数:Kh(NaCN)=10-4.5mol/L
C. 图乙中b点的溶液:c(CN-)>c(Cl-)>c(HCN)>c(OH-)>c(H+)
D. 图乙中c点的溶液:c(Na+)+c(H+)=c(HCN)+c(OH-)+c(CN-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由含碘废水制取碘酸钾的一种工艺如下:
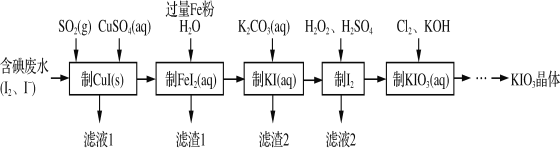
⑴ 写出KIO3在日常生活中的一个重要应用________________________。
⑵ 检验“含碘废水”中是否含有单质I2的常用试剂是________(写试剂名称)。
⑶ 通入SO2的目的是将I2还原为I-,该反应的离子方程式为______________________。
⑷ 工艺中五种物质的制备反应中,不涉及氧化还原反应的步骤是“制________”。
⑸ “制KI(aq)”时,该温度下水的离子积为Kw=1.0×10-13,Ksp[Fe(OH)2]=9.0×10-15。
为避免0.9 mol·L-1 FeI2溶液中Fe2+水解生成胶状物吸附I-,起始加入K2CO3必须保持溶液的pH不大于______。
⑹ “制KIO3溶液”反应的离子方程式为__________________。

⑺ KCl、KIO3的溶解度曲线如图所示。流程中由“KIO3(aq)”得到KIO3晶体的操作步骤为_____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】锂锰电池结构如图所示,其中电解质![]() 溶于混合有机溶剂中,
溶于混合有机溶剂中,![]() 通过电解质迁移入
通过电解质迁移入![]() 晶格中生成
晶格中生成![]() 。下列有关说法正确的是
。下列有关说法正确的是

A. 外电路电流方向:a→b
B. 电池正极反应式为:![]()
C. 可以用水代替电池中的混合有机溶剂
D. 用该电池给铅蓄电池充电,a极与Pb电极相连
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有金属单质A、B、C和气体甲、丙以及物质D、E、F、G、H,它们之间的相互转化关系如下图所示(图中有些反应的生成物和反应的条件没有标出)。

请回答下列问题:
(1)写出下列物质的化学式:B_____________、丙____________;
(2)写出下列反应的化学方程式;
反应①_________________________________________________________________;
反应③_________________________________________________________________;
反应⑤_________________________________________________________________;
(3)向F的溶液中加入D溶液后产生的现象是________________________________,并用化学反应方程式解释产生此现象的原因____________________、_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】草酸亚铁晶体(FeC2O4·2H2O,相对分子质量为180)呈淡黄色,可用作照相显影剂。某实验小组对其进行了一系列探究。
I.纯净草酸亚铁晶体热分解产物的探究。
(1)气体产物成分的探究。小组成员采用如下装置(可重复选用)进行实验:

①装置D的名称为___________。
②按照气流从左到右的方向,上述装置的连接顺序为___________→尾气处理装置(填仪器接口的字母编号)。
③实验前先通入一段时间N2,其目的为______________________。
④实验证明了气体产物中含有CO,依据的实验现象为______________________。
(2)固体产物成分的探究。充分反应后,A处反应管中残留黑色固体。查阅资料可知,黑色固体可能为Fe或FeO。小组成员设计实验证明了其成分只有FeO,其操作及现象为___________。
(3)依据(1)和(2)结论,可知A处反应管中发生反应的化学方程式为___________。
Ⅱ.草酸亚铁晶体样品纯度的测定
工业制得的草酸亚铁晶体中常含有FeSO4杂质,测定其纯度的步骤如下:
步骤1:称取m g草酸亚铁晶体样品并溶于稀H2SO4中,配成250mL溶液。
步骤2:取上述溶液25.00mL,用c mol· L -1KMnO4标准液滴定至终点,消耗标准液V1mL;
步骤3:向反应后溶液中加入适量锌粉,充分反应后,加入适量稀H2SO4,再用cmol·L-1KMnO4标准溶液滴定至终点,消耗标准液V2mL。
(4)步骤3中加入锌粉的目的为____________________________________________。
(5)草酸亚铁晶体样品的纯度为____________________________________________;若步骤1配制溶液时部分Fe2+被氧化,则测定结果将___________(填“偏高”、“偏低”或“不变”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上,从精制黑钨矿(FeWO4、MnWO4)中提取金属钨的一种流程如下图所示,该流程同时获取副产物Fe2O3和MnCl2。

已知:I.过程①~④中,钨的化合价均不变;
Ⅱ.常温下钨酸难溶于水;
Ⅲ.25℃时,Ksp[Fe(OH)3]=1.0×10-38,Ksp [Mn(OH)2]=4.0×10-14
回答下列问题:
(1)上述流程中的“滤渣1”除MnO2外还有_____、“气体”除水蒸气、HCl外还有____(均填化学式);
(2)过程①中MnWO4参与反应的化学方程式为______;FeWO4参与的反应中氧化剂与还原剂的物质的量之比为___________;
(3)已知WO3(s)+3H2(g)=W(s)+3H2O(g) ΔH=a kJ·mol-1
WO3(s)=WO3(g) ΔH=b kJ·mol-1
写出WO3(g)与H2(g)反应生成W(s)的热化学方程式:_______;
(4)过程⑦在25℃时调pH,至少应调至_______(当离子浓度等于1.0×10-5mol·L-1时,可认为其已沉淀完全);
(5)过程⑧要获得MnCl2固体,在加热时必须同时采取的一项措施是__________;
(6)钠钨青铜是一类特殊的非化学计量比化合物,其通式为NaxWO3,其中0<x<1,这类化合物具有特殊的物理化学性质,是一种低温超导体。应用惰性电极电解熔融的Na2WO4和WO2混合物可以制备钠钨青铜,写出WO42-在阴极上放电的电极反应式:___________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com