
【题目】下列因素中,对发生在溶液中且无气体参加的反应的速率不产生显著影响的是( )
A.浓度
B.温度
C.压强
D.反应物的性质
 举一反三期末百分冲刺卷系列答案
举一反三期末百分冲刺卷系列答案科目:高中化学 来源: 题型:
【题目】已知甲醇的燃烧热数值为726.51kJmol﹣1 . 下列热化学方程式书写正确的是( )
A.CH4O+ ![]() O2═CO2+2H2O△H=﹣726.51 kJ?mol﹣1
O2═CO2+2H2O△H=﹣726.51 kJ?mol﹣1
B.CH4O(l)+ ![]() O2(g)═CO2(g)+2H2O(g)△H=+726.51 kJ?mol﹣1
O2(g)═CO2(g)+2H2O(g)△H=+726.51 kJ?mol﹣1
C.2CH4O(l)+3O2(g)═2CO2(g)+4H2O(l)△H=+1453.12 kJ?mol﹣1
D.CH4O(l)+ ![]() O2(g)═CO2(g)+2H2O(l)△H=﹣726.51 kJ?mol﹣1
O2(g)═CO2(g)+2H2O(l)△H=﹣726.51 kJ?mol﹣1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有常温下pH=2的盐酸甲和pH=2的CH3COOH溶液乙,请根据下列操作回答问题:
(1)取10mL的乙溶液,加入少量无水醋酸钠固体(假设加入固体前后,溶液体积保持不变),醋酸的电离平衡(填“向左”、“向右”或“不”)移动;常温下,另取10mL的乙溶液,加水稀释过程中,下列表达式的数据一定增大的是 .
A.c(H+) B. ![]() C.c(H+)c(OH﹣) D.
C.c(H+)c(OH﹣) D. ![]()
(2)取等体积的甲、乙两溶液,分别用等浓度的NaOH稀溶液中和,则消耗的NaOH溶液的体积大小关系为:V(甲)V(乙)( 填“>”、“<”或“=”).
(3)已知25℃时,两种酸的电离平衡常数如下:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数K1 | 1.8×10﹣5 | 4.3×10﹣7 | 3.0×10﹣8 |
K2 | ﹣﹣ | 5.6×10﹣11 | ﹣﹣ |
下列四种离子水解程度最大的是 .
A.HCO3﹣
B.CO32﹣
C.ClO﹣
D.CH3COO﹣
(4)常温下,取99mL甲溶液与1mL1mol/L的NaOH溶液混合(忽略溶液体积变化),恢复至常温时其pH= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将物质的量浓度相等的CuSO4溶液和NaCl溶液等体积混合后,用石墨电极进行电解,电解过程中,溶液的pH随时间t变化的曲线如图所示,则下列说法中不正确的是( ) 
A.A点pH小于7是因为Cu2+水解使溶液显酸性
B.BC段阳极产物是Cl2
C.整个过程中阳极先产生Cl2 , 后产生O2
D.CD段电解的物质是水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】卤族元素的单质和化合物很多,我们可以利用所学物质结构与性质的相关知识去认识和理解它们.
(1)卤族元素位于元素周期表的区; 溴的价电子排布式为 .
(2)在一定浓度的溶液中,氢氟酸是以二分子缔合(HF) 2 形式存在的.使氢氟酸分子缔合的作用力是 .
(3)请根据下表提供的第一电离能数据判断,最有可能生成较稳定的单核阳离子的卤素原子是(填名称).
氟 | 氯 | 溴 | 碘 | |
第一电离能(kJ/mol) | 1681 | 1251 | 1140 | 1008 |
(4)已知碘酸(HIO3)和高碘酸(H5IO6)的结构分别如图I、II 所示: 
请比较二者酸性强弱:HIO3H5IO6(填“>”、“<”或“=”).
(5)试分析 ClO2﹣中心氯原子的杂化类型 , 试写出一个 ClO3﹣的等电子体 .
(6)图1为碘晶体晶胞结构.有关说法中正确的是 .
A.碘分子的排列有2种不同的取向,2种取向不同的碘分子以4配位数交替配位形成层结构
B.用均摊法可知平均每个晶胞中有4个碘原子
C.碘晶体为无限延伸的空间结构,是原子晶体
D.碘晶体中存在的相互作用有非极性键和范德华力
(7)已知CaF2晶体(见图2)的密度为ρg/cm3 , NA为阿伏加德罗常数,棱上相邻的两个Ca2+的核间距为a cm,则CaF2的相对分子质量可以表示为 . 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是( )
A.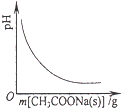
向CH3COOH溶液中逐步加入CH3COONa固体后,溶液pH的变化
B.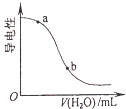
向CH3COOH溶液中加水时溶液的导电性变化,则CH3COOH溶液的pH:a>b
C.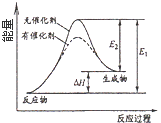
催化剂能改变化学反应的焓变
D.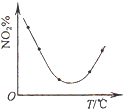
等量NO2在容积相同的恒容密闭容器中,不同温度下分别发生反应:2NO2(g)N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某一反应体系中有反应物和生成物共五种物质:O2、H2CrO4、Cr(OH)3、H2O、H2O2。已知该反应中H2O2只发生如下过程:H2O2→O2。
(1)该反应中的还原剂是 。
(2)该反应中,发生还原反应的过程是 → 。
(3)写出该反应的化学方程式,并用双线桥法标出电子转移的方向和数目: 。
(4)若反应转移了0.3 mol电子,则产生的气体在标准状况下体积为 L。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水的综合利用包括很多方面,下图是从海水中通过一系列工艺流程提取产品的流程图. 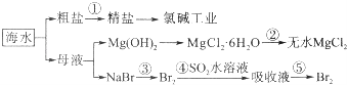
海水中主要含有Na+、K+、Mg2+、Ca2+、Cl﹣、Br﹣、SO42﹣、HCO3﹣等离子.
已知:MgCl26H2O受热生成Mg(OH)Cl和HCl气体等.回答下列问题:
(1)海水pH约为8的原因主要是天然海水含上述离子中的 .
(2)除去粗盐溶液中的杂质(Mg2+、SO42﹣、Ca2+),加入药品的顺序可以为(填序号)
①NaOH溶液 ②BaCl2溶液 ③过滤后加盐酸 ④Na2CO3溶液
(3)过程②中由MgCl26H2O制得无水MgCl2 , 应如何操作 .
(4)从能量角度来看,氯碱工业中的电解饱和食盐水是一个将转化为的过程.采用石墨阳极,不锈钢阴极电解熔融的氯化镁,发生反应的化学方程式为
(5)从第③步到第④步的目的是 . 采用“空气吹出法”从浓海水中吹出Br2 , 并用SO2吸收.主要反应的化学方程式为 .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com