
【题目】将物质的量浓度相等的CuSO4溶液和NaCl溶液等体积混合后,用石墨电极进行电解,电解过程中,溶液的pH随时间t变化的曲线如图所示,则下列说法中不正确的是( ) 
A.A点pH小于7是因为Cu2+水解使溶液显酸性
B.BC段阳极产物是Cl2
C.整个过程中阳极先产生Cl2 , 后产生O2
D.CD段电解的物质是水
科目:高中化学 来源: 题型:
【题目】在基态多电子原子中,关于核外电子能量的叙述错误的是( )
A.最易失去的电子能量最高
B.电离能最小的电子能量最高
C.p轨道电子能量一定高于s轨道电子能量
D.在离核最近区域内运动的电子能量最低
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】乳酸亚铁{[CH3CH(OH)COO]2Fe}广泛应用于乳制品、营养液等,能溶于水,可由乳酸与FeCO3反应制得.
Ⅰ.制备碳酸亚铁:装置如图所示.
(1)装置B中可观察到的现象是铁粉逐渐溶解,
(2)将B中生成的FeCl2溶液压入装置C的操作是
(3)Ⅱ.制备乳酸亚铁:将制得的FeCO3加入乳酸溶液中,加入少量铁粉,在75℃下搅拌使之充分反应,然后再加入适量乳酸.
加入少量铁粉的作用是
(4)从所得溶液中获得乳酸亚铁晶体所需的实验操作是、、洗涤、干燥.
(5)设计实验证明乳酸亚铁中含 Fe2+: .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是Zn和Cu形成的原电池,下列描述合理的是( )
①Cu为阳极,Zn为阴极
②Cu极上有气泡产生
③SO42﹣向Cu极移动
④若有0.5mol电子流经导线,则可产生0.25mol气体
⑤电子的流向是:Cu→导线→Zn ⑥正极反应式:Cu+2e﹣═Cu2+ . 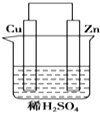
A.①②③
B.②④
C.④⑤⑥
D.③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某烃的分子式为C10H14,能使高锰酸钾酸性溶液褪色,不能使溴水褪色,分子结构中含两个相同的烷基,则此烃可能的结构有
A.2种B.3种C.4种D.5种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)根据反应8NH3+3Cl2![]() 6NH4Cl+N2,回答下列问题:
6NH4Cl+N2,回答下列问题:
①该反应中氧化剂是 ,氧化产物是 。
②该反应中被氧化的物质与被还原的物质物质的量之比为 。
(2)某一反应体系中存在下列6种物质:NO、FeSO4、Fe(NO3)3、HNO3、Fe2(SO4)3和H2O。已知存在下列转化关系:HNO3→NO,请完成下列各题:
①该反应的氧化剂是 ,还原剂是 。
②该反应中1 mol氧化剂 (填“得到”或“失去”) mol电子。
③当有0.1 mol HNO3被还原,此时生成标准状况下NO的体积是 L。
④请把各物质填在下面空格处,需配平:
______+□______![]() □______+□______+□______+□
□______+□______+□______+□
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列变化过程中,△S<0的是( )
A.NH3(g)与HCl(g)反应生成NH4Cl(s)
B.氯化钠溶于水中
C.CaCO3(S)分解为CaO(S)和CO2(g)
D.干冰(CO2)的升华
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com