
【题目】甲状腺激素和血红蛋白中含有的重要元素依次是
A.I、FeB.Cu、MgC.I、MgD.Fe、Mg
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组欲对含少量硫酸亚铁和硫酸铁的硫酸铜溶液进行综合实验:
(1)除去Fe2+和Fe3+并制备CuSO45H2O,请根据以下流程回答问题:
有关氢氧化物开始沉淀和沉淀完全的pH如下表:
氢氧化物 | Fe(OH)3 | Fe(OH)2 | Cu(OH)2 |
开始沉淀的pH | 1.9 | 6.5 | 4.7 |
沉淀完全的pH | 3.7 | 9.7 | 6.7 |
①试剂X的化学式为 , 加入试剂Y调节溶液pH的范围是;
②操作a用到的玻璃仪器为烧杯,玻璃棒和;操作b的名称为;
(2)已知:5Fe2++MnO4﹣+8H+=5Fe3++Mn2++4H2O,欲测定混合溶液中的Fe2+的浓度,取待测液20.00mL,用浓度为0.01molL﹣1的酸性KMnO4溶液滴定,下列滴定方式中,最合理的是(填字母序号,夹持部分已略去)
达到终点时用去酸性KMnO4溶液12.00mL,请计算c(Fe2+)= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在0.5molCl2中含有( )
A. 0.5个Cl2 B. 1个Cl原子
C. 3.01×1023个Cl原子 D. 6.02×1023个Cl原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一个容积固定为2L的密闭容器中,发生反应:aA(g)+bB(g)pC(g)△H=?,反应情况记录如表:
时间(min) | n(A)(mol) | n(B)(mol) | n(C)(mol) |
0 | 1 | 3 | 0 |
第2min | 0.8 | 2.6 | 0.4 |
第4min | 0.4 | 1.8 | 1.2 |
第6min | 0.4 | 1.8 | 1.2 |
第8min | 0.1 | 2.0 | 1.8 |
第9min | 0.05 | 1.9 | 0.3 |
请根据表中数据仔细分析,回答下列问题:
(1)第2min到第4min内A的平均反应速率v(A)=molL﹣1min﹣1
(2)由表中数据可知反应在第4min到第6min时处于平衡状态,若在第2min、6min时分别改变了某一个反应条件,则改变的条件分别可能是:①第 2min;②第 6min;
(3)反应在第4min建立平衡,此温度下该反应的化学平衡常数 K= .
(4)判断第9min时(是/否)达平衡,说明理由 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有常温下pH=2的盐酸甲和pH=2的CH3COOH溶液乙,请根据下列操作回答问题:
(1)取10mL的乙溶液,加入少量无水醋酸钠固体(假设加入固体前后,溶液体积保持不变),醋酸的电离平衡(填“向左”、“向右”或“不”)移动;常温下,另取10mL的乙溶液,加水稀释过程中,下列表达式的数据一定增大的是 .
A.c(H+) B. ![]() C.c(H+)c(OH﹣) D.
C.c(H+)c(OH﹣) D. ![]()
(2)取等体积的甲、乙两溶液,分别用等浓度的NaOH稀溶液中和,则消耗的NaOH溶液的体积大小关系为:V(甲)V(乙)( 填“>”、“<”或“=”).
(3)已知25℃时,两种酸的电离平衡常数如下:
化学式 | CH3COOH | H2CO3 | HClO |
电离平衡常数K1 | 1.8×10﹣5 | 4.3×10﹣7 | 3.0×10﹣8 |
K2 | ﹣﹣ | 5.6×10﹣11 | ﹣﹣ |
下列四种离子水解程度最大的是 .
A.HCO3﹣
B.CO32﹣
C.ClO﹣
D.CH3COO﹣
(4)常温下,取99mL甲溶液与1mL1mol/L的NaOH溶液混合(忽略溶液体积变化),恢复至常温时其pH= .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外兴趣小组欲测定某NaOH溶液的浓度,其操作步骤如下:
①将碱式滴定管用蒸馏水洗净后,用待测溶液润洗后,再注入待测溶液,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数;将锥形瓶用蒸馏水洗净后,用待测溶液润洗锥形瓶2~3次;从碱式滴定管中放入25.00mL待测溶液到锥形瓶中.
②将酸式滴定管用蒸馏水洗净后,用标准溶液润洗后,向其中注入0.1000mol/L标准盐酸,调节滴定管的尖嘴部分充满溶液,并使液面处于“0“刻度以下的位置,记下读数.
③向锥形瓶中滴入酚酞作指示剂,进行滴定.滴定至指示剂刚好变色,且并不马上变色为止,测得所耗盐酸的体积为V1mL.
④重复以上过程,但在滴定过程中向锥形瓶加入5mL的蒸馏水,测得所耗盐酸的体积为V2mL.试回答下列问题:
(1)锥形瓶中的溶液时,达到滴定终点.
(2)该小组在步骤①中的错误是
由此造成的测定结果(偏高、偏低或无影响)
(3)如图,是某次滴定时的滴定管中的液面,其读数为Ml 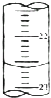
(4)请根据下表数据计算待测烧碱溶液的浓度mol/L.
滴定次数 | 待测液体积(mL) | 标准盐酸体积(mL) | |
滴定前度数(mL) | 滴定后度数(mL) | ||
第一次 | 25.00 | 0.50 | 20.40 |
第二次 | 25.00 | 4.00 | 24.10 |
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将物质的量浓度相等的CuSO4溶液和NaCl溶液等体积混合后,用石墨电极进行电解,电解过程中,溶液的pH随时间t变化的曲线如图所示,则下列说法中不正确的是( ) 
A.A点pH小于7是因为Cu2+水解使溶液显酸性
B.BC段阳极产物是Cl2
C.整个过程中阳极先产生Cl2 , 后产生O2
D.CD段电解的物质是水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列图示与对应的叙述相符的是( )
A.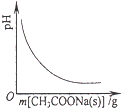
向CH3COOH溶液中逐步加入CH3COONa固体后,溶液pH的变化
B.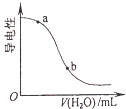
向CH3COOH溶液中加水时溶液的导电性变化,则CH3COOH溶液的pH:a>b
C.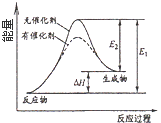
催化剂能改变化学反应的焓变
D.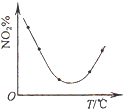
等量NO2在容积相同的恒容密闭容器中,不同温度下分别发生反应:2NO2(g)N2O4(g),相同时间后测得NO2含量的曲线,则该反应的△H<0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组物质中,按单质、化合物、混合物的顺序排序正确的是
A. 稀有气体、尿素、冰与水混合 B. 白磷、浓硫酸、胆矾
C. 金刚石、漂白粉、大理石 D. 水银、干冰、盐酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com