
����Ŀ������ع㷺Ӧ���ڻ�϶�������ϵͳ���缫������NiO2��Fe��̼��Ϳ���������Ƴɡ��ŵ�����в���Ni��OH��2��Fe��OH��2��Fe��OH��2������������ˮ���������������ڵ��ʹ�ú�缫���϶Ի�����Σ����ij��ȤС��Ըõ�ص缫���Ͻ��л����о���
��֪����NiCl2������ˮ��Fe3����������Ni2����
��ij�¶���һЩ�������������Ksp����ʼ��������ȫ����ʱ������pH�����ʾ��
M��OH��n | Ksp | pH | |
��ʼ���� | ������ȫ | ||
Al��OH��3 | 2.0��10��32 | 3.8 | ���� |
Fe��OH��3 | 4.0��10��38 | 1.9 | 3.2 |
Fe��OH��2 | 8.0��10��16 | 6.95 | 9.95 |
Ni��OH��2 | 6.5��10��18 | 5.9 | 8.9 |
�ش��������⣺
��1���õ�صĸ���������___________________��������ӦʽΪ_________________��
��2������������ѹΪ3V����2W���ݹ��磬���������0.02gFe�������ϵ�ع���__________min��С�������2λ��������֪F=96500C/mol��
��3������ص缫�����������ܽ���������˫��ˮ����Ŀ����_____________�����ˣ�����Һ����������NiO���壬��ʼ��������ʱ�����ӷ���ʽ��_______________��___________________�������������������Ӷ�����������pHӦ������___________������Ũ��С�ڻ����1��10-5mol/LΪ��ȫ������lg2=0.3��lg3=0.5������ƽ������ij���������е��������ʷ��뿪����ʵ�鷽��_____________��
��4��������NiO���˺����Һ����Na2C2O4���õ�NiC2O4��2H2O����ҺA��A����Ҫ�ɷ���_____________�������ҺA����������������B______�������ʽ������������������C______�������ʽ������NiC2O4��2H2O���뵽�������Һ����ͨ����ʱij�����������壬���ɵõ����ղ�ƷNi��OH��3����ͨ������Ϊ______���B������C���������壬�ж�������_________��
���𰸡� Fe NiO2+2H2O+2e-=Ni��OH��2+2OH- 1.72 ����Һ�е�Fe2+����ΪFe3+ NiO+2H+=Ni2++H2O Fe3++3H2O=Fe��OH��3��+3H+ 5.1~5.9֮�� ����������NaOH��Һ�г���ܽ⣬���ˡ�ϴ�ӣ�����ΪFe��OH��3������Һͨ������CO2�����ˡ�ϴ�ӣ��ó�����Al��OH��3�� NaCl��Һ H2 Cl2 C ������������Cl2����Ni��OH��2��Ni��OH��3��NiԪ�ػ��ϼ����ߣ���Ҫ��������������ѡ�õ�������������Cl2��
����������1�����⿼��ԭ������������ж��Լ��缫��Ӧʽ����д��ԭ��ع���ԭ���У������Ϸ���������Ӧ�����ϼ����ߣ�������Ŀ��������Ϣ��Fe��Fe(OH)2��Fe�Ļ��ϼ����ߣ��������������ԭ��ص������Ϸ�����ԭ��Ӧ�����ϼ۽��ͣ�������Ϣ��NiO2��Ni(OH)2��Ni�Ļ��ϼ۽��ͣ�NiO2�������ϵõ��ӣ����缫��ӦʽΪNiO2��2H2O��2e��=Ni(OH)2��2OH������2�����⿼��绯ѧ�ļ��㣬����0.02gFe�����ĵ�����0.02��2��96500/56=68.93C������I=P/U=2/3=0.67A������ʱ��Ϊ68.93/(0.67��60)=1.71min����3�����⿼��Ԫ�ؼ��仯��������ʣ��缫������Al��Ni(OH)2��Fe2O3�������������Һ�е�������Ni2����Al3����Fe2�����������������Һ����Fe2��������Fe3������������NiO���壬��H����Ӧ��ʹpH�����ɱ������ݿ�֪����ʼ���ֳ���ΪFe(OH)3�������ֳ���ͬʱ������pHӦ������Al3����ȫ������Ni2��������֮�䣬Al3������Ũ��С�ڻ����1��10��5mol��L��1������Ksp[Al(OH)3]=c(Al3��)��c3(OH��)=2.0��10��32��������ֵ�����c(OH��)= ![]() mol��L��1��pOH=8.9����pH=14��8.9=5.1�����pHӦ������5.1��5.9֮�䣬�����������Fe(OH)3��Al(OH)3��������������������Һ�У��Ƚ�Al(OH)3����ܽ⡢���ˡ�ϴ�ӣ�����ΪFe(OH)3��������Һͨ������CO2�����ˡ�ϴ�ӣ��õ�������Al(OH)3����4�����⿼����ԭ����������NiO���˺����Һ��Ҫ�ɷ���NiCl2������Na2C2O4���õ�NiC2O4��2H2O����ҺA��Ҫ�ɷ���NaCl�����NaCl��Һ��2Cl����2H2O
mol��L��1��pOH=8.9����pH=14��8.9=5.1�����pHӦ������5.1��5.9֮�䣬�����������Fe(OH)3��Al(OH)3��������������������Һ�У��Ƚ�Al(OH)3����ܽ⡢���ˡ�ϴ�ӣ�����ΪFe(OH)3��������Һͨ������CO2�����ˡ�ϴ�ӣ��õ�������Al(OH)3����4�����⿼����ԭ����������NiO���˺����Һ��Ҫ�ɷ���NiCl2������Na2C2O4���õ�NiC2O4��2H2O����ҺA��Ҫ�ɷ���NaCl�����NaCl��Һ��2Cl����2H2O ![]() H2������������Cl2������������2OH������NiC2O4��2H2O���뵽�����NaOH��Һ���ɵõ����ղ�ƷNi(OH)3��NiԪ�صĻ��ϼ����ߣ����ͨ������ΪCl2���������������塣
H2������������Cl2������������2OH������NiC2O4��2H2O���뵽�����NaOH��Һ���ɵõ����ղ�ƷNi(OH)3��NiԪ�صĻ��ϼ����ߣ����ͨ������ΪCl2���������������塣



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����CO2�У�Mgȼ������MgO��C������˵����ȷ����
A. Ԫ��C�ĵ���ֻ���ڽ��ʯ��ʯī����ͬ��������
B. Mg��MgO��þԪ�����İ뾶��r(Mg2+)>r(Mg)
C. �ڸ÷�Ӧ�����£�Mg�Ļ�ԭ��ǿ��C�Ļ�ԭ��
D. �÷�Ӧ���ڷ�������ԭ��Ӧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijԭ�ӵ�һ�ּ���̬Ϊ1s22s12p1�����Ԫ�������ڱ��е�λ��Ϊ
A. �ڶ�������A�� B. �ڶ�������A��
C. �ڶ�������A�� D. �ڶ�������A��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���F��������������������������·�ߺϳɡ�

�ش��������⣺
��1��![]() �����п��ܹ����ԭ�������_____����
�����п��ܹ����ԭ�������_____����
��2������A��������______��
��3������D�к��������ŵ�������_______��
��4������Ӧ�����ķ�Ӧ������______��
��5��д������Ӧ�����Ļ�ѧ����ʽ��________��
��6��C�ж���ͬ���칹������C�������еĹ�������ͬ����_____�������к˴Ź�������Ϊ�����Ľṹ��ʽΪ ��_______��
��_______��
��7�����������ϳ�·�ߣ���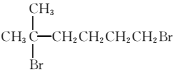 Ϊԭ�������Լ���ѡ���������Ʊ�
Ϊԭ�������Լ���ѡ���������Ʊ�![]() ���ϳ�·�ߣ�_______________��
���ϳ�·�ߣ�_______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����A��B��C��D��E���ֶ�����Ԫ�أ���֪���ڵ�A��B��C��D����Ԫ��ԭ�Ӻ����56�����ӣ������ڱ��е�λ����ͼ��ʾ��E�ĵ��ʼȿ��������ᷴӦ���ֿ�����NaOH��Һ��Ӧ�ų�H2����E����������A�������Ӻ�����Ӳ�ṹ��ȫ��ͬ��

�ش��������⣺
��1��A��E�γɵĻ�����Ļ�ѧʽ�� __________________��
��2��B����������ﻯѧʽΪ_____________��C��Ԫ������Ϊ __________��D�ĵ�����ˮ��Ӧ�ķ���ʽΪ___________________��
��3����D��E�γɵĻ������ˮ��Һ�е����ռ���Һֱ���������۲쵽��������________________________���йط�Ӧ�����ӷ���ʽΪ________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ħ������[(NH4)2Fe(SO4)2]������ˮ�����л�ԭ�ԡ����������÷���м��ϡ����������Ϊԭ����ȡĦ���ε�����ͼ��

�ش��������⣺
��1����������l���м�Na2CO3��Һ��Ϊ��ϴ�ӳ�ȥ����м��������ۣ����ȵ�Ŀ����______�����ü�Ҫ���ֺͱ�Ҫ�����ӷ���ʽ˵����������100g10����Na2CO3��Һ��Ҫ��������ҩ�ס���Ͳ���ձ�����������_______��
��2��������2�������÷���м���������ԭ����______________��
��3��������3������(NH4)2SO4�����ֽ����ܽ�����ν��е�ʵ������ǣ�����Ũ����______�����ˡ�ϴ�ӡ����
��4��һ����õζ�������Ħ���β�Ʒ��Fe2���ĺ�������ȡ4.0gĦ������Ʒ������ˮ����������ϡ���ᣬ��0.2 mol/LKMnO4��Һ�ζ����ﵽ�յ�ʱ������10.00 mL KMnO4��Һ��
�� �ζ������з�����Ӧ�����ӷ���ʽΪ___________��
�� ��Ʒ��Fe2������������Ϊ_________��
�� �ζ������У����ֿ���________������ҡ����ƿ��ֱ��_________ʱֹͣ�ζ�����������ʱ�����Ӷ������ⶨ�����ƫ________����������������������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����һ���¶��£��ݻ��̶����ܱ������У�ͨ��һ������N2O4��������ӦN2O4(g)![]() 2NO2(g)����ϵ�и�����Ũ����ʱ��仯��ͼ��ʾ�������������������
2NO2(g)����ϵ�и�����Ũ����ʱ��仯��ͼ��ʾ�������������������

A. ���¶����ߣ�����������ɫ����
B. �ڸ��¶��·�Ӧ2NO2(g)![]() N2O4(g)��ƽ�ⳣKΪ25/9
N2O4(g)��ƽ�ⳣKΪ25/9
C. ��Ӧ��ƽ�����Ӧ�������ݻ�����һ�룬ƽ��������Ӧ�����ƶ�
D. ��Ӧ��ƽ������������ͨ��NO2���壬��c(NO2)����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ڣ����ǰ�����Ⱦ��������ʳƷ������ɫʳƷ���������ר�Ұ���ɫֲ��ͨ���������ת����ʳƷ������ɫʳƷ�������ṩ��ʳƷ������ɫʳƷ��ͨ��������Ƶõ�ʳƷ������ɫʳƷ�����������˵��������������ɫʳƷ���ǣ� ��
A. ���� B. ���� C. ʳ�� D. ʳ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ϳɰ���ҵΪ��������ʳ���������˾��ף�һ�������£����ܱ������н��кϳɰ���Ӧ��N2��g��+3H2��g��2NH3��g�����������淴Ӧ��������Ҳ�������ʱ������˵������ȷ���ǣ� ��
A. N2��H2��ȫת��ΪNH3 B. N2��H2��NH3�������й���
C. ��Ӧ�Ѵﵽ��ѧƽ��״̬ D. N2��H2��NH3��Ũ�Ȳ��ٸı�
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com