
【题目】(1)在标准状况下,体积为6.72L的CO质量为___,CO物质的量为____,CO分子数为____,CO摩尔质量为____。
(2)在标准状况下,体积为8.96 L的CO和CO2的混合气体共14.4g。CO的质量为____g。CO的体积为___L。混合气体的平均摩尔质量为___g·mol-1。
【答案】8.4g 0.3mol 0.3NA 28g·mol-1 5.6 4.48 36
【解析】
(1)根据n=m/M=V/Vm=N/NA计算;
(2)设CO和CO2的物质的量分别为x、y,结合质量关系、物质的量关系计算。
(1)在标准状况下,体积为6.72L的CO质量为28g·mol-1×6.72L/22.4L·mol-1=8.4g,CO物质的量为6.72L/22.4L·mol-1=0.3mol,CO分子数为0.3mol×NA=0.3NA,CO摩尔质量为28g·mol-1。
(2)设CO和CO2的物质的量分别为x、y,则
28x+44y=14.4g
x+y=8.96L/22.4L·mol-1,解得x=0.2mol、y=0.2mol,
CO的质量为0.2mol×28g·mol-1=5.6g。CO的体积为0.2mol×22.4L·mol-1=4.48L。混合气体的平均摩尔质量为 =36g·mol-1。
=36g·mol-1。


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】VmLFe2(SO4)3溶液中含有Fe3+ag,取![]() mL溶液稀释到5VmL,则稀释后溶液中SO42﹣的物质的量浓度是
mL溶液稀释到5VmL,则稀释后溶液中SO42﹣的物质的量浓度是
A.![]() mol/LB.
mol/LB.![]() mol/L
mol/L
C.![]() mol/LD.
mol/LD.![]() mol/L
mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】a,b,c,d为四种由短周期元素构成的中性粒子,它们都有14个电子,且除a外都是共价型分子。回答下列问题:
(1)a是单核粒子,a单质可用作半导体材料,a原子核外电子排布式为______________。
(2)b是双核化合物,常温下为无色无味气体。b的化学式为________。人一旦吸入b气体后,就易引起中毒,是因为__________而中毒。
(3)c是双核单质,写出其电子式____________。c分子中所含共价键的类型为_______(填“极性键”或“非极性键”)。c单质常温下性质稳定,不易起反应,原因是________________________。
(4)d是四核化合物,其结构式为______________;d分子内所含共价键有________个σ键,________个π键;σ键与π键的强度大小关系为σ___π(填“>”、“<”或“=”),原因是:__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】大阳能路灯蓄电池是磷酸铁锂电池,其工作原理如图。M电极材料是金属锂和碳的复合材料(碳作为金属锂的载体),电解质为一种能传导Li+的高分子材料,隔膜只允许Li+通过,电池反应式为LixC6+Li1-x FePO4![]() LiFePO4+6C。下列说法正确的是
LiFePO4+6C。下列说法正确的是

A. 放电时Li+从左边移向右边,PO43-从右边移向左边
B. 放电时,正极反应式为:Li1-xFePO4+xLi++xe-= LiFePO4
C. 充电时M极连接电源的负极,电极反应为6C+xe-=C6x-
D. 充电时电路中通过2.0mol电子,产生7.0gLi
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室现有一包NaCl、FeCl3、Al2(SO4)3组成的粉末,某课外小组同学为测定其中NaCl的含量,取13.69 g样品进行如下实验(所加试剂均为过量)。

请回答:
(1)①~③所涉及的实验操作方法中,用到过滤的是______(填序号)。
(2)生成沉淀C的离子方程式是_________________________________。
(3)根据上述实验,判断下列说法正确的是______(填字母)。
a.溶液D是无色的碱性溶液
b.溶液D中至少含有5种离子
c.向溶液D中加入过量稀硫酸,产生白色沉淀
d.仅用硝酸银一种试剂不能检验溶液D中的氯离子
(4)样品中NaCl的物质的量为______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2.48 g铁铜合金完全溶解于80 mL 4.0 mol·L-1稀硝酸中,得到标准状况下672 mL NO气体(假设此时无其他气体产生),下列说法正确的是
A. 取反应后溶液,滴入几滴KSCN溶液,无血红色出现
B. 该合金中铁与铜的物质的量之比是1∶2
C. 反应后溶液(忽略溶液体积变化)中c(H+)=2.5 mol·L-1
D. 向反应后的溶液中加入2.0 mol·L-1NaOH溶液至金属离子恰好全部沉淀时,需加入NaOH溶液的体积是120 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
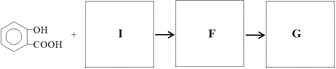
【题目】按下列路线合成新抗凝(抗血栓药物)
新抗凝

已知:I:
II:
III:![]()
(1) 所需的试剂是__________。
所需的试剂是__________。
(2) B→C分两步进行,反应类型分别是 __________、__________。
(3)下列说法不正确的是_________。
a.化合物B能使Br2/CCl4褪色
b. 化合物C能发生银镜反应
c.F遇FeCl3溶液显色
d. 新抗凝的分子式C19H15NO6
(4)E+H→新抗凝的化学方程式是_______________________。
(5)已知:![]() ,写出有关化合物的结构简式I ________F________G________。
,写出有关化合物的结构简式I ________F________G________。
(6)写出一种符合下列条件的A的同分异构体的结构简式_____________________。
① 红外光谱表明分子中含有-COO-、苯环结构
② 1H-NMR谱显示苯环上有三种不同环境的H原子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化铬(CrN)是一种良好的耐磨材料,实验室可用无水氯化铬(CrCl3)与氨气在高温下反应制备,反应原理为CrCl3+NH3![]() CrN+3HCl.回答下列问题:
CrN+3HCl.回答下列问题:
(1)制备无水氯化铬。氯化铬有很强的吸水性,通常以氯化铬晶体(CrCl3·6H2O)的形式存在。直接加热脱水往往得到Cr2O3,有关反应的化学方程式为______________,以氯化铬晶体制备无水氯化铬的方法是_____________________________。
(2)制备氮化铬。某实验小组设计制备氮化铬的装置如下图所示(夹持与加热装置省略):

①装置A中发生反应的化学方程式为_____________________。
②实验开始时,要先打开装置A中活塞,后加热装置C,目的是___________________。
③装置B中盛放的试剂是____________,装置D的作用是_____________________。
④有同学认为该装置有一个缺陷,该缺陷是_______________________。
(3)氯化铬的纯度测定。制得的CrN中含有Cr2N杂质,取样品14.38g在空气中充分加热,得固体残渣(Cr2O3)的质量为16.72g,则样品中CrN的质量分数为_____________(结果保留3位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】取10.6g Na2CO3溶于水配成100ml溶液,求:
(1)Na2CO3物质的量_______。
(2)Na2CO3溶液的物质的量浓度_______。
(3)取出20ml该溶液用蒸馏水稀释,使Na2CO3溶液物质的量浓度变为0.4mol/L,求加入蒸馏水的体积(设稀释时,对溶液体积的影响忽略不计)_______。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com