
【题目】已知下列反应的热化学方程式:
6C(s)+5H2(g)+3N2(g)+9O2(g)= 2C3H5(ONO2)3(l) △H1;
H2(g)+ ![]() O2(g)=H2O(g) △H2 ; C(s)+O2(g)=CO2(g) △H3
O2(g)=H2O(g) △H2 ; C(s)+O2(g)=CO2(g) △H3
则反应4C3H5(ONO2)3(l)=12CO2(g)+10H2O(g)+O2(g)+6N2(g)的△H为( )
A.12△H3+10△H2﹣2△H1B.2△H1﹣10△H2﹣12△H3
C.12△H3﹣10△H2﹣2△H1D.△H1﹣10△H2﹣12△H3
科目:高中化学 来源: 题型:
【题目】请按要求填空:
(1)写出![]() 中的官能团的名称_____;
中的官能团的名称_____;
(2)![]() 的名称是___________;
的名称是___________;
(3)CH2=CH—CH3在催化剂加热条件下生成聚合物的反应方程式为__________ ;
(4)写出实验室制乙烯的化学反应方程式____________;
(5)①称取34g某有机化合物A,完全燃烧后生成18gH2O和88gCO2,已知该有机物的蒸气对氢气的相对密度为68,则该有机物的分子式为_____________;
②该有机物A的核磁共振氢谱和红外光谱如下:
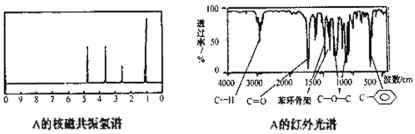
试推测有机物A的结构简式为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A(C2H4)是基本的有机化工原料,由A制备聚丙烯酸甲酯(有机玻璃主要成分)和肉桂酸的合成路线(部分反应条件略去)如图所示:
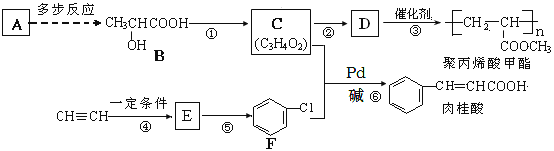
已知:①E的相对分子质量在70~80之间,步骤④的反应类型是加成反应
②![]() +CH2=CH2
+CH2=CH2![]() +HX (X为卤原子,R为取代基)
+HX (X为卤原子,R为取代基)
回答下列问题:
(1)F的名称是________;反应①的反应试剂和反应条件是________;⑥的反应类型是________。
(2)反式肉桂酸的结构简式为_________。
(3)由C制取D的化学方程式为_________。
(4)肉桂酸的同分异构体中能同时满足下列条件的共有_______种(不考虑立体异构);
①能与FeCl3溶液发生显色反应;
②能使溴的四氯化碳溶液褪色;
③能发生银镜反应。
其中苯环上只有两个取代基,核磁共振氢谱为6组峰、且峰面积比为2:2:1:1:1:1的是:________(写结构简式)。
(5)请运用所学知识并结合信息: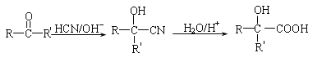 ,设设计由A(C2H4)制备B的合成路线(无机试剂任选):____________。
,设设计由A(C2H4)制备B的合成路线(无机试剂任选):____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是部分短周期元素原子半径与原子序数的关系如图,则下列说法正确的是( )

A . Z、N两种元素形成的化合物熔融状态下可以导电
B.X、N两种元素的气态氢化物的沸点相比,前者较低
C.Z的氧化物能分别溶解于Y的氢氧化物和N的氢化物的水溶液中
D.由X与M两种元素组成的化合物能与水反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组拟实验探究锡及锡的化合物的部分性质。经查阅资料知:Sn的熔点为![]() ;
;![]() 易被氧化,且易水解;
易被氧化,且易水解;![]() 常温下易分解,
常温下易分解,![]() 常温下为无色液体,熔点为
常温下为无色液体,熔点为![]() ,沸点为
,沸点为![]() ,回答下列问题:
,回答下列问题:
(1)该小组用以下流程制备![]() 晶体:
晶体:
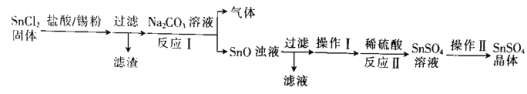
![]() 加入锡粉的作用为______________________________________。
加入锡粉的作用为______________________________________。
![]() 反应Ⅰ的离子方程式为______________________________。
反应Ⅰ的离子方程式为______________________________。
![]() 操作Ⅰ为沉淀的洗涤,请简述如何判断沉淀是否洗涤干净:_____________________。
操作Ⅰ为沉淀的洗涤,请简述如何判断沉淀是否洗涤干净:_____________________。
(2)用熔融的锡与干燥的氯气制备![]() ,实验装置如下:
,实验装置如下:
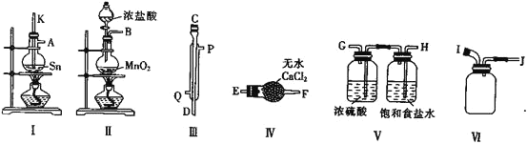
![]() 装置Ⅲ为冷凝管,则水流从__________
装置Ⅲ为冷凝管,则水流从__________![]() 填“Q”或“P”
填“Q”或“P”![]() 口进入。
口进入。
![]() 请用大写英文字母表示的接口按从左到右顺序组装仪器:__________________________。
请用大写英文字母表示的接口按从左到右顺序组装仪器:__________________________。
![]() 整个装置存在的不足之处为_________________________。
整个装置存在的不足之处为_________________________。
(3)该小组通过下列方法测定所用锡粉的纯度:取产品![]() 溶于稀硫酸中,加入过量的
溶于稀硫酸中,加入过量的![]() 溶液,再用
溶液,再用![]() 的
的![]() 溶液滴定
溶液滴定![]() ,消耗
,消耗![]() 溶液
溶液![]() 。已知
。已知![]() ,
,![]() ,
,![]() 。则锡粉的质量分数为
。则锡粉的质量分数为![]() 杂质不参与反应
杂质不参与反应![]() ______________
______________![]() 结果保留三位有效数字
结果保留三位有效数字![]() 。
。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用如右图所示实验装置(夹持仪器已略去)探究铜丝与过量浓硫酸的反应。下列实验不合理的是( )
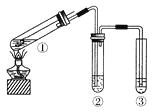
A. 上下移动①中铜丝可控制SO2的量
B. ②中选用品红溶液验证SO2的生成
C. ③中选用NaOH溶液吸收多余的SO2
D. 为确认CuSO4生成,向①中加水,观察颜色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,pH=2的盐酸和醋酸各1mL分别加水稀释,pH随溶液体积变化的曲线如下图所示。下列说法不正确的是( )

A. 曲线Ⅰ代表盐酸的稀释过程 B. a溶液的导电性比c溶液的导电性强
C. a溶液中和氢氧化钠的能力强于b溶液 D. 将a、b两溶液加热至30℃, 变小
变小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】亚硫酸盐是一种常见的食品添加剂,用如图实验可检验某食品中亚硫酸盐含量(含量通常以1kg样品中含SO2的质量计;所加试剂均足量)。下列说法不正确的是
![]()
A. 葡萄酒酿造时通入SO2起到了杀菌和增酸的作用
B. 反应①中若不通入N2则测得的SO2含量偏低
C. 反应①中煮沸的目的是加快亚硫酸的分解,降低SO2的溶解度
D. 若仅将②中的氧化剂“H2O2溶液”替换为“溴水”,对测定结果无影响
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温下用H2还原CuCl制备活性铜,反应原理如下:
2Cu(s)+Cl2(g) ![]() 2CuCl(s) ΔH1=-36 kJ·mol-1①
2CuCl(s) ΔH1=-36 kJ·mol-1①
H2(g)+2CuCl(s) ![]() 2Cu(s)+2HCl(g) ΔH2②
2Cu(s)+2HCl(g) ΔH2②
有关物质的键能数据如下表:
物质 | H2 | Cl2 | HCl |
键能/kJ·mol-1 | 436 | 243 | 432 |
(1)ΔH2=________kJ·mol-1。
(2)经测定反应②制备活性铜的反应趋势大,原因是__________。
(3)在某温度下,反应①达到平衡状态,在tl时,增加压强到原来的2倍(Cu的量足够),在图中画出Cl2浓度的变化趋势线。________________________

(4)白色不溶于水的CuCl可以由电解法制得,如图所示:

①装置中用的交换膜为________。
A.阳离子交换膜 B.阴离子交换膜
C.质子交换膜 D.氢氧根离子交换膜
②阳极的电极反应式为______________________________________________。
(5)已知CuCl可溶解于稀硝酸,写出该反应的化学方程式:
________________________________________________________________________。
(6)根据已学知识写出制取CuCl的一种方法,用化学方程式表示:____________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com