
【题目】(题文)某研究小组用如图装置进行SO2与FeCl3溶液反应的相关实验(夹持装置已略去)。
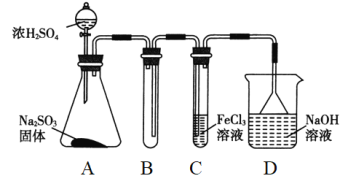
(1)通入足量SO2时C中观察到的现象是______________________。
(2)根据以上现象,该小组同学认为SO2与FeCl3溶液发生氧化还原反应。
①写出SO2与FeCl3溶液反应的离子方程式:_______________________;
②请设计实验方案检验有Fe2+生成:_________________________;
③该小组同学向C试管反应后的溶液中加入硝酸酸化的BaCl2溶液,若出现白色沉淀,即可证明反应生成了SO42-。该做法_____(填“合理”或“不合理”),理由是______。
(3)D装置中倒置漏斗的作用是__________________________。
(4)为了验证SO2具有还原性,实验中可以代替FeCl3的试剂有________(填字母)。
a.浓H2SO4 b.酸性KMnO4溶液 c.碘水 d.NaCl溶液
【答案】溶液由棕黄色变为浅绿色2Fe3++SO2+2H2O===SO42-+4H++2Fe2+取C中反应后的溶液,向其中滴人KSCN溶液,不变红,再加入新制的氯水,溶液变红不合理硝酸可以将溶解的SO2氧化为H2SO4,干扰实验防止溶液倒吸bc
【解析】
装置A中的分液漏斗中的浓硫酸滴入锥形瓶中反应生成二氧化硫气体,通过装置B为安全瓶,通过装置C中的氯化铁溶液具有氧化性能氧化二氧化硫为硫酸,氯化铁被还原为氯化亚铁,最后过量的二氧化硫被氢氧化钠溶液吸收,据此判断。
(1)通入足量SO2时C中发生二氧化硫与氯化铁的氧化还原反应,生成硫酸亚铁,则观察到溶液由棕黄色变为浅绿色;
(2)①二者发生氧化还原反应,生成硫酸根离子、亚铁离子,离子反应方程式为2Fe3++SO2+2H2O=SO42-+4H++2Fe2+;
②亚铁离子易被氧化为铁离子,可以用KSCN溶液检验铁离子,则检验有Fe2+生成的实验方法为取C中反应后的溶液,向其中滴入KSCN溶液,不变红,再加入新制的氯水,溶液变红;
③由于硝酸具有强氧化性,则硝酸可以将溶解的SO2氧化为硫酸,干扰试验,所以做法不合理;
(3)因尾气易溶于NaOH溶液,则倒置漏斗的作用为防止NaOH溶液倒吸;
(4)验证SO2具有还原性,可与高锰酸钾或碘水发生氧化还原反应,S元素的化合价升高,而与浓硫酸、NaCl不反应,答案为b、c。


科目:高中化学 来源: 题型:
【题目】CO和H2在一定条件下合成甲醇的反应为;CO(g)+2H2(g)![]() CH3OH(g) △H1。现在容积均为1L的a、b、c、d、e五个密闭容器中分别充入1molCO和2molH2的混合气体,控制温度,进行实验,测得相关数据如图(图1:温度分别为300℃ 、500℃的密闭容器中,甲醇的物质的量:图2:温度分别为Tl~T5的密闭容器中,反应均进行到5min时甲醇的体积分数)。下列叙述正确的是
CH3OH(g) △H1。现在容积均为1L的a、b、c、d、e五个密闭容器中分别充入1molCO和2molH2的混合气体,控制温度,进行实验,测得相关数据如图(图1:温度分别为300℃ 、500℃的密闭容器中,甲醇的物质的量:图2:温度分别为Tl~T5的密闭容器中,反应均进行到5min时甲醇的体积分数)。下列叙述正确的是
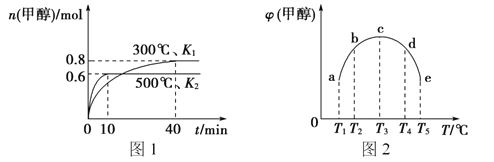
A. 该反应的△H1>0,且K1>K2
B. 将容器c中的平衡状态转变到容器d中的平衡状态,可采取的措施有升温或加压
C. 300℃时,向平衡后的容器中再充入0.8molCO, 0.6molH2,0.2molCH3OH,平衡正向移动
D. 500℃时,向平衡后的容器中再充入1molCH3OH,重新平衡后,H2浓度和百分含量均增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学小组欲进行如下的实验探究金属与浓硫酸反应。试回答下列问题:
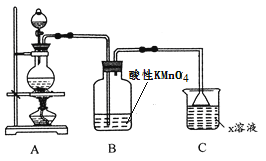
(1)利用上图装置研究铜与浓硫酸反应,反应的化学方程式为____________。C装置的作用_____________。
(2)将上述实验中的铜改为铁,在常温下进行,无明显现象,其原因是__________。在加热条件下,实验的后阶段可观察到倒立的漏斗边沿有气体冒出,该气体可能为_______。
验证该气体的实验方案如下:
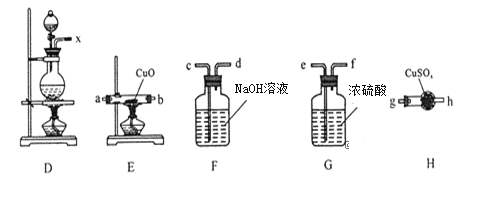
①装置连接顺序:X→ ___→___→___→___→a→b→_____;
②能证明上述假设成立的实验现象是_____________。
③某学习小组经过讨论认为该实验方案还不够严谨,你认为是否合理,若合理,则不作答,若不合理,请指出不严谨之处__________________________。
④若把D中的反应液倾倒入盛水的烧杯中,为氧化其中的某离子,可供选用的试剂: a、Cl2;b、Br2;c、稀硫酸和H2O2,从无污染角度考虑,你认为合适试剂是______(填字母),反应的离子反应方程式为_________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知25℃时有关弱酸的电离平衡常数:
弱酸化学式 | HSCN | CH3COOH | HCN | H2CO3 |
电离平衡常数 | 1.3×10-1 | 1.8×10-5 | 4.9×10-10 | K1=4.3×10-7,K2=5.6×10-11 |
(1)等物质的量浓度的a.CH3COONa、b.NaCN、c.Na2CO3、d.NaHCO3溶液的pH由大到小的顺序为______________(填序号)。
(2)25℃时,将20mL0.1mol/LCH3COOH溶液和20mL0.1mol/LHSCN溶液分别与20mL0.1mol/LNaHCO3溶液混合,实验测得产生的气体体积(V)随时间(t)的变化如右图所示,反应初始阶段两种溶液产生CO2气体的速率存在明显差异的原因是________。反应结束后所得两溶液中,c(CH3COO-)____c(SCN-)(填“>”、“<”或“=")。

(3)若保持温度不变,在醋酸溶液中加少量盐酸,下列量会变小的是___(填序号)。
a.c(CH3COO-) b.c(H+) c.Kw d.醋酸电离平衡常数
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列递变规律不正确的是
A.Na、Mg、Al原子的失电子能力逐渐减弱
B.Si、P、S元素的最高正化合价依次降低
C.C、N、O的原子半径依次减小
D.Cl、Br、I的气态氢化物的稳定性依次减弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A.需要加热才能发生的反应一定是吸热反应
B.放热反应在常温条件下一定能进行
C.NaOH固体溶于水是放热反应
D.A+B=C+D是放热反应,说明A和B物质的总能量高于C和D的总能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据热化学方程式2H2(g)+O2(g)===2H2O(g) ΔH=-483.6 kJ·mol-1,下列说法或表达正确的是( )
A. 2 mol水蒸气分解生成2 mol氢气与1 mol氧气需吸收483.6 kJ的热量
B. 2H2(g)+O2(g)===2H2O(l) ΔH>-483.6 kJ·mol-1
C. H2(g)+![]() O2(g)===H2O(g) ΔH=241.8 kJ·mol-1
O2(g)===H2O(g) ΔH=241.8 kJ·mol-1
D. 1 mol氢气与0.5 mol 氧气总能量小于1 mol水蒸气的总能量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com