
【题目】短周期元素W、X、Y、Z的原子序数依次增大,W、Z位于同主族,四种元素组成的一种化合物的结构式为 。下列说法不正确的是
。下列说法不正确的是
A. W的最简单氢化物的稳定性比X的弱
B. X.Y形成的化合物水溶液显碱性
C. W与Y形成的化合物中一定含有离子键
D. 原子半径:Y>Z>X>W
科目:高中化学 来源: 题型:
【题目】硅是人类文明发展的重要元素之一,从传统材料到信息材料的发展过程中创造了一个又一个奇迹。
(1)工业生产粗硅的反应有:
SiO2+2C![]() Si(粗)+2CO↑
Si(粗)+2CO↑
SiO2+3C![]() SiC+2CO↑
SiC+2CO↑
两个反应的氧化剂分别为____、___。若产品中单质硅与碳化硅的物质的量之比为1:1,则参加反应的C和SiO2的质量之比为___。
(2)工业上可以通过如下图所示的流程制取纯硅:
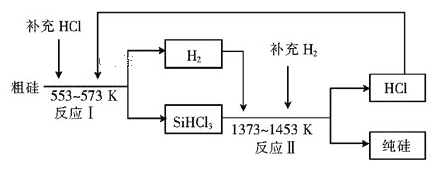
①若反应I为Si(粗)+3HCl![]() SiHCl3+H2,则反应II的化学方程式为____。
SiHCl3+H2,则反应II的化学方程式为____。
②整个制备过程必须严格控制无水无氧。SiHCl3遇水剧烈反应生成H2SiO3、HCl和另一种物质,写出该反应的化学方程式:_____。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关实验方案或说法正确的是
A.  实验室制取乙酸乙酯
实验室制取乙酸乙酯
B.  比较NaHCO3和Na2CO3的热稳定性
比较NaHCO3和Na2CO3的热稳定性
C.  脱脂棉燃烧证明过氧化钠与水反应放热
脱脂棉燃烧证明过氧化钠与水反应放热
D.  a处有红色物质生成,b处变蓝,证明X一定是H2
a处有红色物质生成,b处变蓝,证明X一定是H2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】饮用水中的NO3对人类健康会产生危害,为了降低饮用水中NO3的浓度,可以在碱性条件下用铝粉将NO3还原为N2,其化学方程式为:
10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O。请回答下列问题:
(1)上述反应中,被氧化的元素_________,还原产物是________。
(2)用“双线桥法”表示反应中电子转移的方向和数目:_______________。
10Al+6NaNO3+4NaOH=10NaAlO2+3N2↑+2H2O
(3)反应中每生成标况下22.4L N2,转移_______mol电子。
(4)请配平下列离子方程式。
____Fe2++____H+ +____NO3=____Fe3+ +____N2O↑+____H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列热化学方程式中,正确的是( )
A.甲烷的燃烧热为890.3kJ·mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g) △H=-890.3kJ·mol-1
B.500℃、30MPa下,将0.5molN2和1.5molH2置于密闭容器中充分反应生成NH3放热19.3kJ,其热化学方程式为:N2(g)+3H2(g)![]() 2NH3(g) △H = -38.6kJ·mol-1
2NH3(g) △H = -38.6kJ·mol-1
C.HCl和NaOH 反应的中和热△H= -57.3kJ·mol-1,则H2SO4和Ba(OH)2反应的热化学方程式为:H2SO4(aq)+Ba(OH)2(aq)=BaSO4(s)+2H2O(l) △H=-114.6kJ·mol -1
D.在101kPa时,2gH2完全燃烧生成液态水,放出285.8kJ热量,H2燃烧的热化学方程式表示为:2H2(g)+O2(g)=2H2O(1) △H =-571.6kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化亚铜(CuCl)是一种应用较广的催化剂,有关物质的转化关系如下图所示(除B、E外,均为对应物质的溶液参加反应,部分生成物和反应条件已略去)。其中B为气体,能使品红溶液褪色;C为正盐,D为重要的调味剂,E为一种红色的金属氧化物,M的摩尔质量为34gmol-1,它的水溶液常作医用消毒液。

(1)E的化学式________________________。
(2)N的电子式为________________________。
(3)写出反应①的化学方程式:_________________________________________。
(4)写出反应②的离子方程式:_________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(Ⅰ)将下列物质进行分类:
①![]() 与
与![]() ②O2与O3③乙醇(C2H5OH)与甲醚(CH3—O—CH3)④正丁烷与异丁烷⑤C60与金刚石
②O2与O3③乙醇(C2H5OH)与甲醚(CH3—O—CH3)④正丁烷与异丁烷⑤C60与金刚石
(1)互为同位素的是__________________(填编号、下同);

(2)互为同素异形体的是___________________;
(3)互为同分异构体的是__________________;
(Ⅱ)反应Fe+H2SO4=FeSO4+H2↑的能量变化趋势如图所示:
(1)该反应为________反应(填“吸热”或“放热”)。
(2)若要使该反应的反应速率加快,下列措施可行的是________(填字母)。
A.改铁片为铁粉
B.改稀硫酸为98%的浓硫酸
C.升高温度
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为______(填“正”或“负”)极。该极上发生的电极反应为_____________________,外电路中电子由______极(填“正”或“负”,下同)向______极移动。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】溴苯是不溶于水的液体,常温下不与酸、碱反应,可用如图装置制取(该反应放出热量)。制取时观察到烧瓶中有大量红棕色蒸气,锥形瓶中导管口有白雾出现等现象。
![]()

下列说法错误的是
A.制备溴苯的反应属于取代反应
B.白雾出现是因为HBr易挥发且极易溶于水
C.装置图中长直玻璃导管仅起导气作用
D.溴苯中溶有少量的溴,可用NaOH溶液洗涤除去
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了研究碳酸钙与盐酸反应的反应速率,某同学通过实验测定碳酸钙固体与足量稀盐酸反应生成CO2的体积随时间的变化情况,绘制出下图所示的曲线。下列有关说法中不正确的是

A. 在0-t1、t1-t2、t2-t3中,t1-t2生成的CO2气体最多
B. 因反应放热,导致0-t1内的反应速率逐渐增大
C. t2-t3的速率V(CO2)= ![]() mL/s
mL/s
D. 将碳酸钙固体研成粉末,则曲线甲将变成曲线乙
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com