
【题目】PCl3主要用于制造敌百虫等有机磷农药和磺胺嘧啶(S.D)等医药的原料。如图为实验室中制取粗PCl3产品的装置,夹持装置略去。
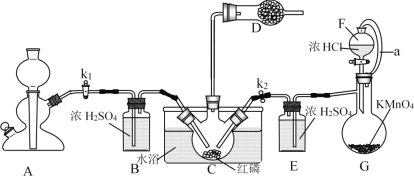
经查阅资料知:红磷与少量Cl2反应生成PCl3,与过量Cl2反应生成PCl5。PCl3遇水会强烈水解生成H3PO3。PCl3遇O2会生成POCl3(三氯氧磷),PCl3、POCl3的熔沸点见下表。
物质 | 熔点/℃ | 沸点/℃ |
PCl3 | -112 | 75.5 |
POCl3 | 2 | 105.3 |
回答下列问题:
(1)仪器G的名称是______。装置F与G由橡胶管a相连通,a的作用是_______。
(2)A是制取CO2装置,CO2的作用是_____,选择A中的药品是_____(填字母)。
a.稀盐酸 b.稀硫酸 c.NaHCO3粉末 d.块状石灰石
(3)装置D中盛有碱石灰,其作用是__________________。
(4)装置G中生成Cl2,反应的离子方程式为___________。
(5)装置C采用65-70℃水浴加热,制得的PCl3粗产品中常含有POCl3、PCl5等杂质,除杂的方法是:先加入红磷加热,除去PCl5,然后通过___________(填实验操作名称),即可得到较纯净的PCl3。
(6)通过实验测定粗产品中PCl3的质量分数,实验步骤如下(不考虑杂质的反应):
第一步:迅速移取20.0 g PCl3粗产品,加水完全水解后,再配成500mL溶液;
第二步:移取25.00mL溶液置于锥形瓶中;
第三步:加入0. 5molL-1碘溶液20mL,碘过量,H3PO3完全反应生成H3PO4;
第四步:加入几滴淀粉溶液,用1.0 molL-1Na2S2O3标准溶液滴定过量的碘,反应方程式为I2+2Na2S2O3=Na2S4O6+2NaI,滴至终点时消耗Na2S2O3标准溶液12mL。
①第三步中反应的化学方程式为_____________。
②根据上述数据,计算该产品中PCl3的质量分数为______%。
【答案】蒸馏烧瓶 使F与G压强相同,便于浓盐酸容易滴出 赶尽装置中空气,防止PCl3被氧化 ad 防止空气中水蒸气进入装置使PCl3水解,吸收未反应的氯气,防止污染空气 16H+ +10Cl-+2MnO4-=5Cl2↑+2Mn2++8H2O 蒸馏 H3PO3+H2O+I2=H3PO4+2HI 55
【解析】
首先A中利用稀盐酸和块状石灰石制取CO2,生成的CO2经过B获得干燥的CO2,CO2气流就会排尽装置内部的空气,以避免生成的PCl3被氧化,然后G中盐酸和高锰酸钾反应制取氯气,经过E中浓硫酸干燥获得干燥的氯气,并与C中红磷反应获得PCl3,另外D中碱石灰吸收空气中的水蒸气和吸收未反应的氯气。
(1)观察仪器G的结构特点知仪器G的名称是蒸馏烧瓶;装置F与G由橡胶管a相连通,a的作用是平衡F和G内部气体的压强,便于浓盐酸在重力作用下更容易滴出,即使F与G压强相同,便于浓盐酸容易滴出;
(2) PCl3遇O2会生成POCl3(三氯氧磷),所以需要排尽装置内部的空气,故A中制取CO2的作用是赶尽装置中空气,防止PCl3被氧化;NaHCO3粉末和酸反应生成CO2的速率过快,不易控制,因而选用块状石灰石与酸反应,而稀硫酸与石灰石反应生成微溶的硫酸钙,其附着在石灰石表面,阻碍反应进行,所以选用块状石灰石与稀盐酸反应制取CO2,故选ad;
(3) PCl3遇水会强烈水解生成H3PO3,同时氯气有剧毒,易与碱反应,因而装置D中盛有碱石灰的作用是防止空气中水蒸气进入装置使PCl3水解,吸收未反应的氯气,防止污染空气;
(4) 装置G中高锰酸钾将盐酸氧化得到氯气,其离子方程式为16H+ +10Cl-+2MnO4-=5Cl2↑+2Mn2++8H2O;
(5) 先加入红磷加热,除去PCl5,此时的杂质为POCl3,观察题给表格信息,PCl5和POCl3沸点相差30℃以上,然后通过蒸馏即可除去POCl3,即可得到较纯净的PCl3;
(6)①加入碘溶液,H3PO3完全反应生成H3PO4,P元素化合价由+3变为+5,H3PO3作还原剂,碘作氧化剂,被还原成HI,所以反应的化学方程式为H3PO3+H2O+I2=H3PO4+2HI;
②滴定剩余的I2消耗Na2S2O3物质的量为1.0×12×10-3mol=0.012mol,由I2+2Na2S2O3=Na2S4O6+2NaI,剩余的I2为![]() ×0.012mol=0.006mol,所以与H3PO3反应的I2为0.5×20×10-3mol-0.006mol=0.004mol,根据关系式PCl3~ H3PO3~ I2可知,20.0g产品中PCl3的质量为
×0.012mol=0.006mol,所以与H3PO3反应的I2为0.5×20×10-3mol-0.006mol=0.004mol,根据关系式PCl3~ H3PO3~ I2可知,20.0g产品中PCl3的质量为![]() g=11g,PCl3的质量分数为
g=11g,PCl3的质量分数为![]() ×100%=55%。
×100%=55%。


科目:高中化学 来源: 题型:
【题目】“太阳水”电池装置如图所示,该电池由三个电极组成,其中a为TiO2电极,b为Pt电极,c为WO3电极,电解质溶液为pH=3的Li2SO4-H2SO4溶液。锂离子交换膜将电池分为A、B两个区,A区与大 气相通,B区为封闭体系并有N2保护。下列关于该电池的说法错误的是( )
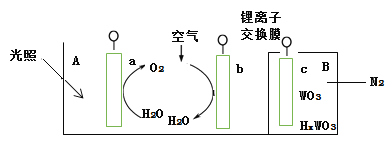
A.若用导线连接a、c,则a为负极,该电极附近pH减小
B.若用导线连接a、c,则c电极的电极反应式为HxWO3 - xe- =WO3 + xH+
C.若用导线先连接a、c,再连接b、c,可实现太阳能向电能转化
D.若用导线连接b、c, b电极的电极反应式为O2+4H++4e-=2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】功能高分子P的合成路线如下:
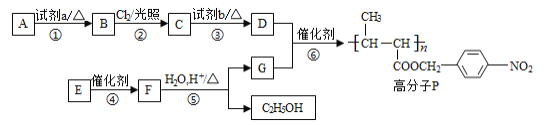
(1)A的分子式是C7H8,其结构简式是________。
(2)试剂a是_______。
(3)反应③的化学方程式:________。
(4)E的分子式是C6H10O2。E中含有的官能团:_________。
(5)反应④的反应类型是________。
(6)反应⑤的化学方程式:________。
(7)已知:2CH3CHO ![]() 。以乙烯为起始原料,选用必要的无机试剂合成E,合成路线如下,写出 I,J 的结构简式:________、________
。以乙烯为起始原料,选用必要的无机试剂合成E,合成路线如下,写出 I,J 的结构简式:________、________
CH2=CH2![]() CH3CH2Br
CH3CH2Br![]() CH3CH2OH
CH3CH2OH![]() CH3CHO
CH3CHO![]() (I)
(I)![]()
![]()
![]()
![]()
![]() (J)
(J)![]() E
E
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关说法中正确的是
A.干粉灭火器和泡沫灭火器的工作原理相同
B.实验室配制1.0 molL-1的NaOH溶液定容时俯视刻度线,配制溶液浓度偏低
C.国产大飞机C919发动机使用的氮化硅属于无机非金属材料
D.冰水混合物、四氧化三铁、纯净矿泉水都不是混合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是元素周期表的一部分,按要求回答问题:
① |
| ||||||||||||||||
|
|
| ② | ③ | ④ |
|
| ||||||||||
⑤ | ⑥ |
|
|
|
|
|
|
|
|
|
| ⑦ |
|
| ⑧ | ⑨ |
|
(1)元素④在周期表中位置是_______。元素③的最高价氧化物的化学式为________。
(2)元素①⑤组成化合物电子式为___________。
(3)元素②的单质与⑧的最高价氧化物的水化物热的浓溶液反应的化学方程式为___。
(4)元素⑦与⑨形成的化合物与元素③的氢化物的水溶液反应的离子方程式为_____。
(5)元素④⑤⑥⑧形成的简单离子,其离子半径由小到大的顺序为_____(用离子符号表示)。
(6)A—F发生如图所示的转化,A、B、C、D为①—⑨中某种元素形成的单质,E、F、G为B、C、D与A形成的二元化合物,G是一种常见温室气体,与B可以反应生成E,E中B元素的质量分数为60%,F为两性物质。

①A和F的化学式分别为_______、_______。
②B与G反应的化学方程式为____________________。
③C与NaOH溶液反应的离子方程式为______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E是五种短周期主族元素,其中A是元素周期表中原子半径最小的元素;B是形成化合物种类最多的元素;C是地壳中含量最多的元素;D的气态氢化物的水溶液显碱性;E金属制成金属板后,经加工可制成一种高质量的反光镜,该金属粉末和氧化铁混合常用于焊接钢轨.
(1)写出C、E的元素符号______、______。
(2)B元素位于周期表中的位置为______,BC2的电子式为______(用元素符号表示)。
(3)A、B、C、D的原子半径由大到小的顺序为______(用元素符号表示)。
(4)E的最高价氧化物对应的水化物与短周期元素中最高价氧化物对应水化物碱性最强的物质在溶液中反应的离子方程式______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素a、b、c、d的原子序数依次增大,在下列转化关系中,甲、乙、丙、丁、戊为上述四种元素组成的二元或三元化合物。其中A为d元素组成的单质,常温下乙为液体,丁物质常用于消毒、漂白。下列说法错误的是
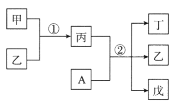
A.简单离子半径:c>b
B.丙中既有离子键又有极性键
C.b、c形成的化合物中阴、阳离子数目比为1:2
D.a、b、d形成的化合物中,d的杂化方式是sp3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高温下超氧化钾晶体呈立方体结构,晶体中氧的化合价部分为0价,部分为2价.如图所示为超氧化钾晶体的一个晶胞(晶体中最小的重复单元),则下列说法中正确的是( )
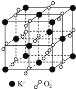
A. 超氧化钾的化学式为KO2,每个晶胞含有4个K+和4个O2-
B. 晶体中每个K+周围有8个O2-,每个O2-周围有8个K+
C. 晶体中与每个K+距离最近的K+有8个
D. 晶体中,0价氧与2价氧的数目比为2:1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿克他利M(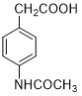 )是一种抗风湿性关节炎药物,其合成路线如下:
)是一种抗风湿性关节炎药物,其合成路线如下:

(1)反应1的类型为______________________________。
(2)反应2的试剂为______________________________。
(3)写出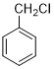 的所有含苯环结构的同分异构体的结构简式______________。
的所有含苯环结构的同分异构体的结构简式______________。
(4)写出由对硝基苯乙酸(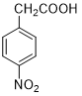 )得到对硝基苯乙酸乙酯的试剂和条件______。
)得到对硝基苯乙酸乙酯的试剂和条件______。
(5)A的分子式为C7H8,写出由A合成苯甲醛的合成路线。
(合成路线常用的表示方式为: )
)
_________________________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com