
【题目】处处留心皆知识.生活中遇到下列问题,不涉及到化学变化的是( )
A.食物腐败变质
B.浓硫酸在空气中体积增大
C.铝表面形成致密的薄膜
D.食醋洗掉水垢
科目:高中化学 来源: 题型:
【题目】尿素[CO(NH2)2]是首个由无机物人工合成的有机物。
(1)工业上尿素由CO2和NH3在一定条件下合成,其反应方程式为_______________。
(2)当氨碳比 ![]() =4,时CO2的转化率随时间的变化关系如图1所示。
=4,时CO2的转化率随时间的变化关系如图1所示。
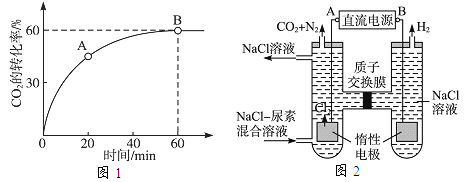
①A点的逆反应速率v逆(CO2)_______B点的正反应速率v正(CO2)(填“<”、“>”或“=”)。
②反应达到平衡后,NH3的转化率为_____________。
(3)人工肾脏可采用间接电化学方法除去代谢产物中的尿素,原理如图2。
①电源的负极为_____(填“A”或“B”)。
②阳极室中发生的电极反应为_________,_________________。
③若两极共收集到气体13.44L(标准状况),则除去的尿素为________g(忽略气体的溶解)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲醚(CH3OCH3)被称为21世纪的新型燃料,它清洁、高效、具有优良的环保性能,甲醚是一种无色气体,具有轻微的醚香味,其燃烧热为1455 kJ·mol﹣1,甲醚可作燃料电池的燃料.
(1)写出甲醚燃烧的热化学方程式 ;已知H2(g)和C(s)的燃烧热分别是285.8kJ·mol﹣1、393.5kJ·mol﹣1;计算反应4C(s)+6H2(g)+O2(g)═2CH3OCH3(g)的反应热△H= kJ·mol﹣1;
(2)工业上利用H2和CO2合成二甲醚的反应如下:6H2(g)+2CO2(g)![]() CH3OCH3(g)+3H2O(g)△H<0
CH3OCH3(g)+3H2O(g)△H<0
①一定温度下,在一个固定体积的密闭容器中进行该反应.下列能判断反应达到化学平衡状态的是 (选填编号,注意大小写)。
a.c(H2)与c(H2O)的比值保持不变
b.单位时间内有2mol H2消耗时,有1mol H2O生成
c.容器中气体密度不再改变
d.容器中气体压强不再改变
②温度升高,该化学平衡移动后,达到新的平衡,CH3OCH3的产率将 (填“变大”、“变小”或“不变”,下同)。
(3)以甲醚、空气、氢氧化钾溶液为原料,石墨为电极可构成燃料电池.该电池的负极反应式的其中一个产物是CO32﹣,请写出该反应的负极反应式 ;
(4)用(3)中的燃料电池为电源,以石墨为电极电解500mL NaCl溶液,装置如图所示,请写出电解过程中Y电极附近观察到的现象是 ;当燃料电池消耗2.8LO2(标准状况下)时,计算此时:NaCl溶液中C(OH-)= mol/L(假设溶液的体积不变,气体全部从溶液中逸出).

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】I.实验室需配制100mL2 mol/LNaOH溶液,请回答下列问题
(1)配制过程中不需要使用的化学仪器有_______(填选项的字母)。
A.烧杯. B.100mL容量瓶 C.漏斗 D.胶头滴管 E.玻璃棒
(2)用托盘天平称取所需氢氧化钠固体,质量为______g。
Ⅱ.某校化学兴趣小组利用右图装置来制取氨气
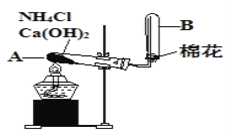
(1)写出用此方法制NH3的化学反应方程式___________________。
(2)图中收集氨气的方法为___________。
(3)若将有浓盐酸的玻璃棒靠近收集氨气的导管口,能观察到的实验现象为___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三草酸合铁酸钾晶体K3[Fe(C2O4)3]·3H2O可用于摄影和蓝色印刷。某化学兴趣小组将无水三草酸合铁酸钾按如图所示装置进行实验。请利用实验室常用仪器、用品和以下限选试剂完成验证和探究过程。
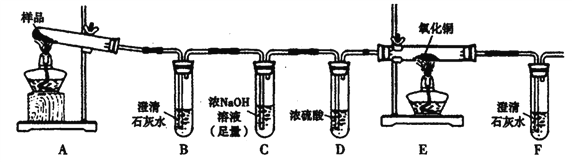
限选试剂:浓硫酸、1.0mol/L HNO3、1.0mol/L盐酸、1.0 mol/L NaOH.3% H2O2、0.1 mol/LKI、0.1mol/LCuSO4、20% KSCN、澄清石灰水、氧化铜、蒸馏水。
I.若实验中,观察到B、F中溶液均变浑浊,则E中的现象是____,推测三草酸合铁酸钾分解的气体产物是____。该小组同学查阅资料后推知,固体产物中,铁元素不可能以三价形式存在,而盐只有K2CO3。
Ⅱ.探究固体产物中铁元素的存在形式。
(1)提出合理假设:假设l____;假设2____;假设3____。
(2)设计实验方案并验证
①取适量固体产物于试管中,加入足量蒸馏水溶解,过滤分离出不溶固体。
②取少量上述不溶固体放入试管中,加入足量____溶液,充分振荡。若溶液颜色及加入的不溶固体无明显变化,则假设____成立。若溶液颜色明显改变,且有暗红色固体生成,则证明有____存在。
③取②所得暗红色固体于试管中,滴加过量____,振荡后静置。取上层清液于试管中,滴加适量____,再滴加____,若溶液基本无色,则假设____成立;若溶液呈____,则假设_____成立。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某溶液中可能含有下列6种离子中的某几种:Cl、SO42—、NH4+、CO32—、K+、Na+。为确认溶液组成进行如下实验:
①200 mL上述溶液,加入足量BaCl2溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀4.30 g,向沉淀中加入过量的盐酸,有2.33 g沉淀不溶。
②向①的滤液中加入足量的NaOH溶液,加热,产生能促使湿润红色石蕊试纸变蓝的气体1.12 L(已换算成标准状况,假定产生的气体全部逸出)。
(1)溶液一定存在的离子有____,可能存在的离子有______;
(2)原溶液中c(CO32—)为____,c(NH4+)____c(SO42—) (填“>、<或=”);
(3)如果上述6种离子都存在,则c(Cl)__c(SO42—) (填“>、<或=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种生物电化学方法脱除水体中NH4+的原理如下图所示:
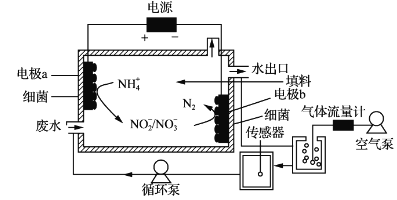
下列说法正确的是
A. 装置工作时,化学能转变为电能
B. 装置工作时,a极周围溶液pH降低
C. 装置内工作温度越高。NH4+脱除率一定越大
D. 电极b上发生的反应之一是:2NO3--2e-=N2↑+3O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】全钒氧化还原电池是一种新型可充电池,不同价态的含钒离子作为正极和负极的活性物质,分别储存在各自的酸性电解液储罐中。其结构原理如图所示,该电池放电时,右槽中的电极反应为:V2+-e-=V3+,下列说法正确的是 ( )
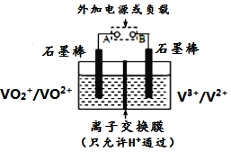
A. 放电时,右槽电解液pH不变
B. 充电时,阴极电解液pH升高
C. 放电时,左槽的电极反应式:VO2++2H++e-=VO2++H2O
D. 充电时,每转移1mol电子,右槽中n(H+)的变化量为1mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】次磷酸(H3PO2)与足量的氢氧化钠溶液反应生成的盐只有NaH2PO2一种。等浓度的次磷酸(H3PO2)溶液与盐酸,前者导电能力弱。下列说法错误的是( )
A.H3PO2中,P元素的化合价为+1价
B.H3PO2为一元弱酸,NaH2PO2溶液呈碱性。
C.次磷酸在水中的电离方程式为H3PO2+H2O![]() H2PO2—+ H3O+
H2PO2—+ H3O+
D.NaH2PO2属于酸式盐
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com