
【题目】某溶液中可能含有下列6种离子中的某几种:Cl、SO42—、NH4+、CO32—、K+、Na+。为确认溶液组成进行如下实验:
①200 mL上述溶液,加入足量BaCl2溶液,反应后将沉淀过滤、洗涤、干燥,得沉淀4.30 g,向沉淀中加入过量的盐酸,有2.33 g沉淀不溶。
②向①的滤液中加入足量的NaOH溶液,加热,产生能促使湿润红色石蕊试纸变蓝的气体1.12 L(已换算成标准状况,假定产生的气体全部逸出)。
(1)溶液一定存在的离子有____,可能存在的离子有______;
(2)原溶液中c(CO32—)为____,c(NH4+)____c(SO42—) (填“>、<或=”);
(3)如果上述6种离子都存在,则c(Cl)__c(SO42—) (填“>、<或=”)。
【答案】CO32—、SO42—、NH4+ Cl、K+、Na+0.05 mol/L>>
【解析】
①取少量该溶液加入BaCl2溶液有白色沉淀生成,再加入足量盐酸后,沉淀部分溶解,并有气体生成,说明白色沉淀为BaCO3和BaSO4,质量一共是4.3 g,则溶液中含有![]() 、
、![]() ,向沉淀中加入过量的盐酸,有2.33 g沉淀不溶,则硫酸钡的质量是2.33 g,所以硫酸根离子的物质的量是
,向沉淀中加入过量的盐酸,有2.33 g沉淀不溶,则硫酸钡的质量是2.33 g,所以硫酸根离子的物质的量是![]() ="0.01" mol,所以碳酸钡的质量是4.3 g2.33 g="1.97" g,
="0.01" mol,所以碳酸钡的质量是4.3 g2.33 g="1.97" g,![]() 的物质的量是
的物质的量是![]() ="0.01" mol;②向①的滤液中加入足量的NaOH溶液,加热,产生能使湿润红色石蕊试纸变蓝的气体是氨气,物质的量是
="0.01" mol;②向①的滤液中加入足量的NaOH溶液,加热,产生能使湿润红色石蕊试纸变蓝的气体是氨气,物质的量是![]() ="0.05" mol,说明溶液中有
="0.05" mol,说明溶液中有![]() 的物质的量是0.05 mol;综合以上
的物质的量是0.05 mol;综合以上
(1)溶液一定存在的离子有:![]() 、
、![]() 、
、![]() ;可能存在的离子有:Cl、K+、Na+。
;可能存在的离子有:Cl、K+、Na+。
(2)依据计算得出c(![]() )=
)=![]() ="0.05" mol/L,
="0.05" mol/L,![]() 为0.01 mol,
为0.01 mol,![]() 为0.05 mol,故c(
为0.05 mol,故c(![]() )>c(
)>c(![]() )。
)。
(3)依据溶液电中性原则,假设都存在,那么0.05 mol+n(Na+)+n(K+)="2×0.01" mol+2×0.01 mol+n(Cl),据此得出n(Cl)=n(Na+)+n(K+)+0.01 mol>0.01 mol。


 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案科目:高中化学 来源: 题型:
【题目】毒重石的主要成分BaCO3(含Ca2+、Mg2+、Fe3+等杂质),实验室利用毒重石制备BaCl22H2O的流程如下:
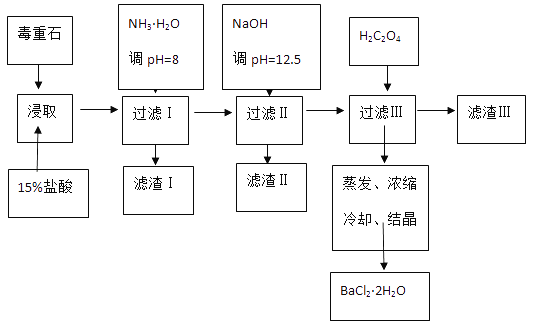
(1)实验室用37%的盐酸配置15%的盐酸,除量筒外还需使用下列仪器中的_________。
a.烧杯 b.容量瓶 c.玻璃棒 d.滴定管
(2)加入NH3H2O调节pH=8可除去_______(填离子符号),滤渣Ⅱ中含________(填化学式)。加入H2C2O4时应避免过量,原因是___________。
Ca2+ | Mg2+ | Fe3+ | |
开始沉淀时的pH | 11.9 | 9.1 | 1.9 |
完全沉淀时的pH | 13.9 | 11.1 | 3.2 |
向BaC2O4悬浊液中加入CaCl2,可发生沉淀的部分转化,请写出反应过程中的离子方程式___________________,计算该反应的平衡常数K=___________(Ksp(BaC2O4)=1.6×10-7,Ksp(CaC2O4)=2.3×10-9,保留一位小数)
(3)利用间接酸碱滴定法可测定Ba2+的含量,实验分两步进行。已知:2CrO42-+2H+=Cr2O72-+H2O Ba2++CrO42-=BaCrO4↓
步骤Ⅰ:移动x mL一定浓度的Na2CrO4溶液于锥形瓶中,加入酸碱指示剂,用b molL-1盐酸标准液滴定至终点,测得滴加盐酸体积为V0mL。
步骤Ⅱ:移取y mL BaCl2溶液于锥形瓶中,加入x mL与步骤Ⅰ相同浓度的Na2CrO4溶液,待Ba2+完全沉淀后,再加入酸碱指示剂,用b molL-1盐酸标准液滴定至终点,测得滴加盐酸的体积为V1mL。根据上述数据,可计算出BaCl2溶液浓度为_________molL-1(用含字母的式子表示)。若步骤Ⅱ中滴加盐酸时有少量待测液溅出,则Ba2+浓度的测量值将_______(填“偏大”或“偏小”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定量的CO2与足量的碳在体积可变的恒压密闭容器中反应:C(s) + CO2(g)![]() 2CO(g),平衡时,体系中气体体积分数与温度的关系如下图所示:
2CO(g),平衡时,体系中气体体积分数与温度的关系如下图所示:
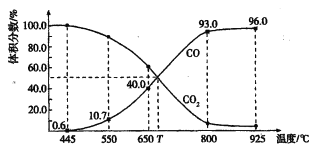
已知:气体分压(P分)=气体总压(p总)×体积分数。下列说法正确的是
A. 550℃时,若充入惰性气体,V正、V逆均减小,平衡不移动
B. 650℃时,反应达平衡后CO2的转化率为40.0%
C. T℃时,若充入等体积的CO2和CO,平衡向逆反应方向移动
D. 925℃时,用平衡分压代替平衡浓度表示的化学平衡常数Kp= 23. 04p总
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】阿伏加德罗常数的值为NA,下列说法正确的是( )
A. 用惰性电极电解1 L 1mol/L CuSO4溶液,阴极得到的铜原子的数目一定为NA
B. 将2.3g钠投入到100ml 0.8mol/L的稀盐酸中,完全反应后可得到H2的数目为0.01NA
C. 1molCl2溶于水后溶液中Cl2、HClO、ClO-、Cl-四种粒子总数为2NA
D. 标准状况下,2molNa2O2与44.8LSO2完全反应,转移的电子数目为4NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】处处留心皆知识.生活中遇到下列问题,不涉及到化学变化的是( )
A.食物腐败变质
B.浓硫酸在空气中体积增大
C.铝表面形成致密的薄膜
D.食醋洗掉水垢
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,下列各组离子在指定溶液中能大量共存的是( )
A. 无色透明溶液中: Ca2+、Cu2+、Br-、Cl-
B. 能使酚酞变红的溶液中: K+、Na+、CO![]() 、AlO
、AlO![]()
C. c(ClO-)=1mol·L-1的溶液中: Fe2+、Al3+、NO![]() 、I-
、I-
D. ![]() =0.1 mol·L-1的溶液中: NH
=0.1 mol·L-1的溶液中: NH![]() 、Mg2+、SO
、Mg2+、SO![]() 、CH3COO-
、CH3COO-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在1L的密闭容器中通入2molNH3,在一定温度下发生下列反应:2NH3![]() N2+3H2,达到平衡时,容器内N2的百分含量为a%。若维持容器的体积和温度都不变,分别通入下列初始物质,达到平衡时,容器内N2的百分含量也为a%的是( )
N2+3H2,达到平衡时,容器内N2的百分含量为a%。若维持容器的体积和温度都不变,分别通入下列初始物质,达到平衡时,容器内N2的百分含量也为a%的是( )
A. 3molH2+2molN2 B. 2molNH3+1molN2
C. 2molH2+3molN2 D. 0.1molNH3+0.95molN2+2.85molH2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫酸锰铵晶体可用作织物和木材加工的防火剂等。由二氧化锰等作原料制取硫酸锰铵晶体步骤如下:
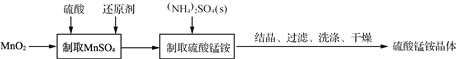
(1)实验前,需称量MnO2的质量,这是因为____________________________。
(2) “制取MnSO4”时,可用C6H12O6(葡萄糖)、H2C2O4(草酸)等物质作还原剂。
①用C6H12O6作还原剂(被氧化为CO2)时,发生反应的n(MnO2)/n(C6H12O6)=________。
②用H2C2O4作还原剂,发生反应的化学方程式为____________________________。
(3)一种测定硫酸锰铵晶体[设为: (NH4)xMny(SO4)z·wH2O]组成的方法如下:
①称取一定量的硫酸锰铵晶体配成250 mL溶液A。
②取25.00 mL溶液A加入足量的BaCl2溶液得BaSO4 0.512 6 g。
③另取25.00 mL溶液A加入10 mL 20%的中性甲醛溶液,摇匀、静置5 min[4NH![]() +6HCHO===3H++6H2O+(CH2)6N4H+,滴定时,1 mol(CH2)6N4H+与1 mol H+相当],加入1~2滴酚酞溶液,用0.100 0 mol·L-1 NaOH标准溶液滴定至终点(在该过程中Mn2+不沉淀),消耗NaOH溶液22.00 mL。
+6HCHO===3H++6H2O+(CH2)6N4H+,滴定时,1 mol(CH2)6N4H+与1 mol H+相当],加入1~2滴酚酞溶液,用0.100 0 mol·L-1 NaOH标准溶液滴定至终点(在该过程中Mn2+不沉淀),消耗NaOH溶液22.00 mL。
④取一定量样品在空气中加热,样品的固体残留率(固体样品的剩余质量/固体样品的起始质量×100%)随温度的变化如右图所示(样品在371 ℃时已完全失去结晶水)。根据以上实验数据计算确定硫酸锰铵晶体的化学式(写出计算过程)。__________________
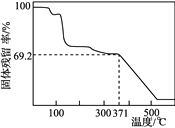
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验可达到实验目的的是( )
A. 将 ![]() 与 NaOH 的水溶液共热制备CH3CH=CH2
与 NaOH 的水溶液共热制备CH3CH=CH2
B. 用甲苯与稀硝酸、稀硫酸的混合酸相混制取 TNT
C. 甲苯在溴化铁催化作用下与液溴反应生成 2,4,6-三溴甲苯
D. 向 CH3CH2Br 中滴入 AgNO3 溶液就可以检验溴元素
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com