
| �¶ȣ� T �� | K1 | K2 |
| 973 | 1.47 | 2.38 |
| 1173 | 2.15 | 1.67 |
| ||
| [CO]?[H2O] |
| [CO2]?[H2] |
| [CO] |
| [CO2] |
| [H2] |
| [H2O] |
| K1 |
| K2 |
| K1 |
| K2 |
| K1 |
| K2 |
| ||


 ͨ��ѧ��Ĭд����ϵ�д�
ͨ��ѧ��Ĭд����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
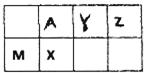 ���ֶ�����Ԫ�������ڱ��е�λ����ͼ������M��X��Z�ڵؿ��еĺ�����ǰ��λ��
���ֶ�����Ԫ�������ڱ��е�λ����ͼ������M��X��Z�ڵؿ��еĺ�����ǰ��λ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��0.80 | B��0.70 |
| C��0.60 | D��0.40 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A��
| ||||
| B��CH4��g��+2O2��g��=CO2��g��+2H2O��g����H=-802.3kJ/mol | ||||
| C��2H2��g��+O2��g��=2H2O��l����H=-571.6kJ/mol | ||||
D��CO��g��+
|
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��2 L������̼�ֽ�����2 Lһ����̼��1 L��������566 kJ���� |
| B����ѹ����������������ʴ��ڷ�Ӧ������� |
| C������ͬ�����£�2 molһ����̼��1 mol�����������ܺʹ���2 mol������̼������ |
| D��һ����̼��ȼ������566 kJ/mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���о���ѧ��������ת����װ�á����̺�Ч�ʵĿ�ѧ�������绯ѧ |
| B����ѧ�������ܡ���ѧ������ܶ�����ͨ����ѧ��Ӧֱ��ת�� |
| C���绯ѧ��Ӧ���̿��Է�Ϊ���������ķ�Ӧ�ͽ��������������ķ�Ӧ���� |
| D���绯ѧ��Ӧ�ð�����⡢��ơ���ұ�𡢵������ȷ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��N2 |
| B��N2O |
| C��NO |
| D��NO2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���Ҽ��Ȧм��ص��̶ȴ��γɵĹ��ۼ�ǿ |
| B���Ҽ������Ƽ�����ת���м������Ƽ�����ת |
| C��N2�����ЦҼ��ͦм���Ŀ��Ϊ1��2 |
| D��CH3-CH3��CH2=CH2��CH��CH�ЦҼ�������ȣ��м�����Ҳ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A����2mol/LAlCl3��Һ��7mol/LNaOH��Һ�������ϣ�2Al3++7OH?=Al��OH��3��+AlO2?+2H2O |
| B��������Һ��ˮ���е�CaCO3��Ӧ��CaCO3+2CH3COOH=Ca2++2CH3COO-+CO2��+H2O |
| C��������������ͨ�����������Һ��SO2+2ClO-+H2O=SO32-+2HClO |
| D������������ϡ���FeS+2H+=H2S��+Fe2+ |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com