
| A、0.80 | B、0.70 |
| C、0.60 | D、0.40 |
| m |
| M |
| 12g |
| 80g/mol |
| 1 |
| 2 |
| 1 |
| 2 |


 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
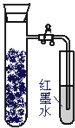 如图,向还原铁粉中加入少量的炭粉,混合均匀后,撒入内壁用NaCl溶液润湿过的具支试管中,塞紧橡皮塞.几分钟后,打开止水夹,观察到导管中水柱上升.对此过程所作的分析正确的是( )
如图,向还原铁粉中加入少量的炭粉,混合均匀后,撒入内壁用NaCl溶液润湿过的具支试管中,塞紧橡皮塞.几分钟后,打开止水夹,观察到导管中水柱上升.对此过程所作的分析正确的是( )| A、碳粉在电化学腐蚀过程中作负极 |
| B、炭粉被氧化 |
| C、发生了吸氧腐蚀 |
| D、发生了析氢腐蚀 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、除去BaSO4中少量BaCO3:加入足量盐酸,充分反应后,过滤、洗涤、干燥 |
| B、除去KCl溶液中的少量MgCl2:加入适量NaOH溶液,过滤 |
| C、除去CO2气体中混有的CO气体:混合气通过灼热的铜网 |
| D、除去CO2气体中混有的HCl气体:通入氢氧化钠溶液洗气 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、蒸发操作中应使水分完全蒸干后,才能停止加热 |
| B、萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |
| C、分液操作时,下层液体从分液漏斗下口放出后,再将上层液体从下口放出到另一个烧杯中 |
| D、蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 生活处处有化学.
生活处处有化学.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、SO2是电解质,其水溶液能导电 |
| B、酸式盐的水溶液一定呈酸性 |
| C、常温时水电离出的c(H+)=10-4mol/L的溶液,不可能是稀盐酸 |
| D、常温时纯水的电离平衡常数为1.0×10-14 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| 温度( T ) | K1 | K2 |
| 973 | 1.47 | 2.38 |
| 1173 | 2.15 | 1.67 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com