
【题目】现有分子式分别为CH4、C2H4、C3H4、C2H6、C3H6的五种有机物。相同质量的以上物质中,在相同状况下气体体积最大的是________;相同质量的以上物质完全燃烧时消耗O2的量最多的是________;相同状况、相同体积的以上五种物质完全燃烧时消耗O2的量最多的是________;相同质量的以上五种物质完全燃烧时,生成CO2最多的是________,生成H2O最多的是________;在120 ℃、1.01×105 Pa状态下,以任意比混合的三种气态烃和足量的氧气混合点燃,相同条件下测得反应前后气体体积没有发生变化,这三种气体是 ________。
【答案】CH4;CH4;C3H6;C3H4;CH4;CH4、C2H4、C3H4
【解析】
试题分析:CH4、C2H4、C2H6、C3H4、C3H6的摩尔质量依次增大,根据n=![]() 可知,相同质量情况下,摩尔质量越小,物质的量越大,相同条件下,体积之比等于物质的量之比,故甲烷的体积最大;相同质量情况下,氢元素质量分数越大,燃烧时消耗氧气越多,CH4、C2H4、C3H4、C2H6、C3H6分子中C、H原子数目之比分别为:1:4、1:2、3:4、1:3、1:2,故甲烷中氢元素质量分数最大,消耗氧气最多;同状况同体积时,气体的物质的量相等,1mol烃的耗氧量为(x+
可知,相同质量情况下,摩尔质量越小,物质的量越大,相同条件下,体积之比等于物质的量之比,故甲烷的体积最大;相同质量情况下,氢元素质量分数越大,燃烧时消耗氧气越多,CH4、C2H4、C3H4、C2H6、C3H6分子中C、H原子数目之比分别为:1:4、1:2、3:4、1:3、1:2,故甲烷中氢元素质量分数最大,消耗氧气最多;同状况同体积时,气体的物质的量相等,1mol烃的耗氧量为(x+![]() )mol,1mol CH4、C2H4、C3H4、C2H6、C3H6耗氧量分别为2mol、3mol、4mol、3.5mol、4.5mol,故C3H6耗氧量最多;CH4、C2H4、C2H6、C3H4、C3H6分子中C、H原子数目之比分别为:1:4、1:2、3:4、1:3、1:2,故C3H4中碳元素质量分数最大,甲烷中氢元素质量分数最大,相同质量时,C元素质量分数越大,生成二氧化碳越多,H元素质量分数越大,生成水的量越多,故C3H4生成二氧化碳最多,甲烷生成水最多。当温度大于100℃时,水为气态,当烃分子中氢原子个数y=4时,燃烧前后体积不变,故相同条件下测得反应前后气体体积没有发生变化的三种烃是CH4、C2H4、C3H4。
)mol,1mol CH4、C2H4、C3H4、C2H6、C3H6耗氧量分别为2mol、3mol、4mol、3.5mol、4.5mol,故C3H6耗氧量最多;CH4、C2H4、C2H6、C3H4、C3H6分子中C、H原子数目之比分别为:1:4、1:2、3:4、1:3、1:2,故C3H4中碳元素质量分数最大,甲烷中氢元素质量分数最大,相同质量时,C元素质量分数越大,生成二氧化碳越多,H元素质量分数越大,生成水的量越多,故C3H4生成二氧化碳最多,甲烷生成水最多。当温度大于100℃时,水为气态,当烃分子中氢原子个数y=4时,燃烧前后体积不变,故相同条件下测得反应前后气体体积没有发生变化的三种烃是CH4、C2H4、C3H4。
故答案为:CH4;CH4;C3H6;C3H4;CH4;CH4、C2H4、C3H4。


 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源: 题型:
【题目】下列关于物质分类的说法正确的是
A.盐酸和硫酸都属于化合物 B.SO2、SiO2、CO均为酸性氧化物
C.硝酸铵和醋酸都属于弱电解质 D.淀粉和蛋白质都属于高分子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在国际环境问题中,一次性使用的聚苯乙烯材料带来的“白色污染”甚为突出。这种材 料难以分解,处理麻烦。最近研究制出一种新型的材料能替代聚苯乙烯。它是由乳酸缩 聚而生成的,该种材料可在乳酸菌作用下发生降解,下列关于聚乳酸的说法正确的是
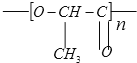
A.聚乳酸是一种纯净物
B.其聚合方式与聚苯乙烯相似
C.其单体为CH3-CH(OH)-COOH
D.聚乳酸是一种线型高分子材料
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:HCN(aq)与NaOH(aq)反应的△H=-12.1kJ /mol;HCl(aq)与NaOH(aq)反应的△H =-55.6kJ/ mol。则HCN在水溶液中电离的ΔH等于
A. -67.7 kJ /mol B. -43.5kJ /mol C. +43.5 kJ/ mol D. +67.7 kJ/ mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以硅藻土为载体的五氧化二钒(V2O5)是接触法生成硫酸的催化剂。从废钒催化剂中回收V2O5既避免污染环境又有利于资源综合利用。废钒催化剂的主要成分为:
物质 | V2O5 | V2O4 | K2SO4 | SiO2 | Fe2O3 | Al2O3 |
质量分数/% | 2.2~2.9 | 2.8~3.1 | 22~28 | 60~65 | 1~2 | <1 |
以下是一种废钒催化剂回收工艺路线:
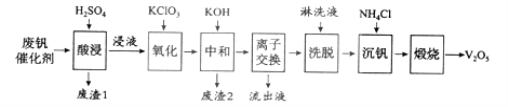
回答下列问题:
(1)“酸浸”时V2O5转化为VO2+,反应的离子方程式为___________,同时V2O4转成VO2+。“废渣1”的主要成分是__________________。
(2)“氧化”中欲使3 mol的VO2+变为VO2+,则需要氧化剂KClO3至少为______mol。
(3)“中和”作用之一是使钒以V4O124形式存在于溶液中。“废渣2”中含有_______。
(4)“离子交换”和“洗脱”可简单表示为:4ROH+ V4O124![]() R4V4O12+4OH(以ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈_____性(填“酸”“碱”“中”)。
R4V4O12+4OH(以ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈_____性(填“酸”“碱”“中”)。
(5)“流出液”中阳离子最多的是________。
(6)“沉钒”得到偏钒酸铵(NH4VO3)沉淀,写出“煅烧”中发生反应的化学方程式____________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】【2016届邯郸一模】【化学选修3:物质结构与性质】
新型储氢材料是开发利用氢能的重要研究方向。
(1)Ti(BH4)3是一种储氢材料,可由TiCl4和LiBH4反应制得。
①基态Cl原子中,电子占据的最高能层符号为_________,该能层具有的原子轨道数为________。
②LiBH4由Li+和BH4-构成,BH4-的立体结构是_________,B原子的杂化轨道类型是________。
Li、B、H元素的电负性由大到小排列顺序为________。
(2)金属氢化物是具有良好发展前景的储氢材料。
①LiH中,离子半径Li+_______H-(填“>”、“=”或“<”).②某储氢材料是第三周期金属元素M的氢化物.M的部分电离能如表所示:
I1/kJmol-1 | I2/kJmol-1 | I3/kJmol-1 | I4/kJmol-1 | I5/kJmol-1 |
738 | 1451 | 7733 | 10540 | 13630 |
M是________ (填元素符号)。
(3)NaH具有NaCl型晶体结构,已知NaH晶体的晶胞参数a=488pm(棱长),Na+半径为102pm,H-的半径为________,NaH的理论密度是___________g·cm-3(只列算式,不必计算出数值,阿伏加德罗常数为NA)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按照一定标准,根据物质与水反应的不同情况,对下列物质进行分类,如图所示,请填空:

(1)上图中分类标准1(分成A、B组的依据)为______________________________。
(2)工业上常用D组中________(填化学式)来消除C组中物质对大气的污染,涉及反应的化学方程式为______________________________ 。
(3)实验室由Al3+制备Al(OH)3时,应选择D组中________(填化学式)的水溶液,
离子方程式为______________________________________。
(4)F组中有两种物质,在工业上均有重要的用途,请各写出一个化学方程式表示其用途:
__________________________________、__________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NA为阿伏加德罗常数的值。下列说法正确的是( )
A.由 D和18O所组成的水11g,所含中子数为4NA
B.1 L 0.4 mol·L-1稀硝酸与Fe完全反应,转移电子数为0.3NA
C.标准状况下,2.24LCHCl3所含分子数为 0.1NA
D.密闭容器中2 mol NO与1 mol O2充分反应,产物的分子数为2NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】二甲醚和乙醇是同分异构体,其鉴别可采用化学方法及物理方法,下列鉴别方法中不能对二者进行鉴别的是 ( )
A. 利用质谱法
B. 利用红外光谱法
C. 利用核磁共振氢谱
D. 利用金属钠或者金属钾
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com